Clear Sky Science · zh
RB缺失通过调节依赖cohesin的环结构和增强子-启动子相互作用来改变染色质组织
为什么细胞的“包装经理”很重要
你体内的每个细胞都必须将大约两米长的DNA塞进比灰尘颗粒还小的细胞核里。DNA如何折叠——不仅仅是它携带哪些基因——也决定了哪些基因会被开启或关闭。本文研究了一种著名的抗癌蛋白RB,揭示它不仅仅阻止细胞失控分裂。RB还参与管理DNA的三维折叠,微调哪些基因可以被近旁的调控开关触及。理解这一隐藏的作用为解释肿瘤在丧失RB后为何变得更具侵袭性提供了新线索。
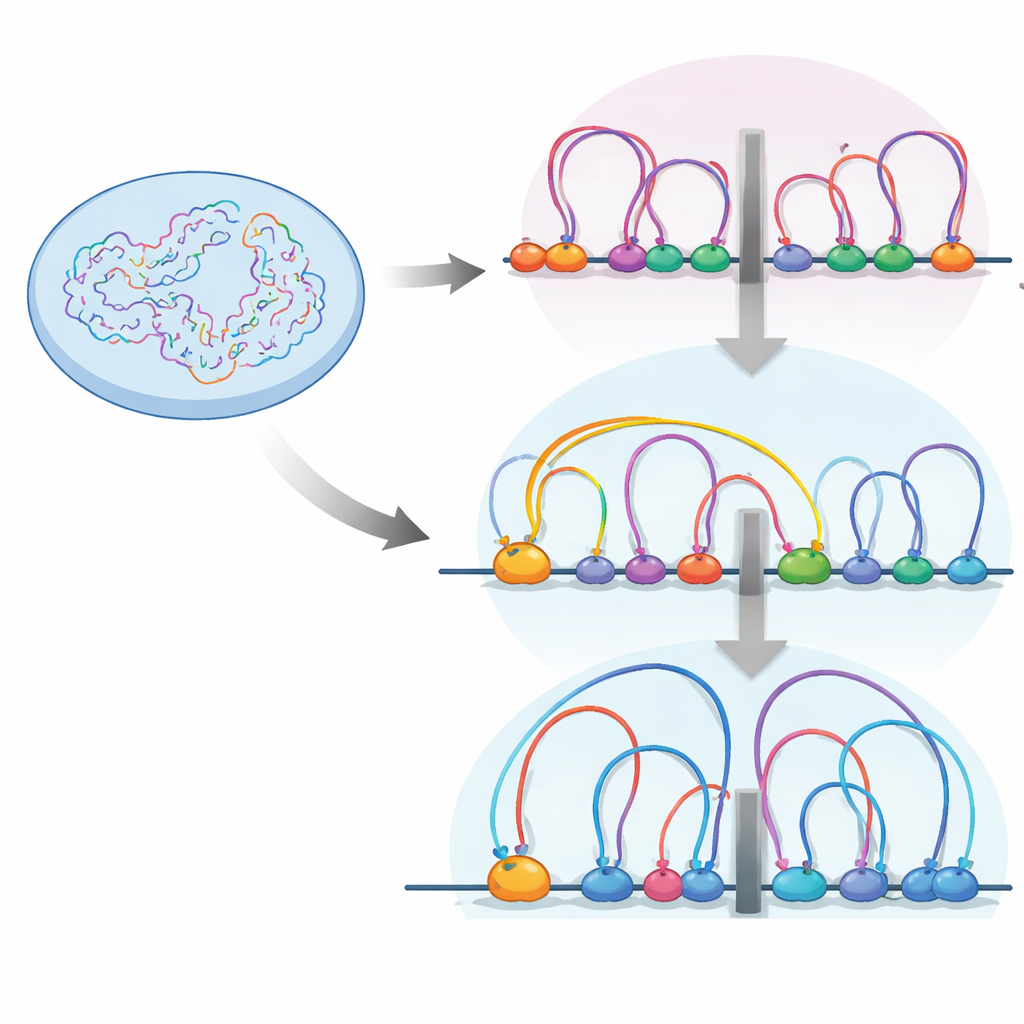
一位具有隐蔽职责的守护者
RB(视网膜母细胞瘤蛋白)最为人所知的是作为细胞周期的刹车。它通常将一组促进生长的基因抑制,直到细胞准备好分裂为止。许多肿瘤通过失活RB来使细胞不受控制地增殖。然而,缺失RB的癌症还表现出一些令人困惑的变化——例如侵袭性增强和能切换细胞类型——这些无法仅用失去细胞周期抑制来解释。早期研究提示RB不仅结合于基因起始区(启动子),还结合于远端调控区(增强子)和作为DNA活性邻域边界的特殊“绝缘子”位点。这提出了RB可能还充当基因组折叠组织者的可能性。
环、边界与交通管控
在细胞核内,DNA纤维通过一种叫cohesin的蛋白机器折成环。这些环有助于将基因及其调控元件归组为称为拓扑关联域(TADs)的单元——本质上是基因和开关在其中更自由相互作用的“社区”。这些社区之间的边界常由一种称为CTCF的绝缘蛋白标记,cohesin常在此处停滞。作者使用高分辨率的染色体接触图谱(Micro-C)和一系列其他基因组学工具,观察在人体视网膜细胞中开启或关闭RB如何重塑这种环状景观。
他们发现,当缺失RB时,DNA环的数量和平均大小都会增加,TAD边界变得更强。同时,RB与cohesin在基因组许多可及区域共存,尤其是在绝缘子位点。对不同细胞周期阶段cohesin位置的详尽绘图显示,RB在有丝分裂期间(染色体凝缩然后重新展开的阶段)帮助将cohesin从这些绝缘子位点移除。没有RB时,cohesin在绝缘子处堆积,强化了边界并改变了DNA邻域之间的隔离方式。
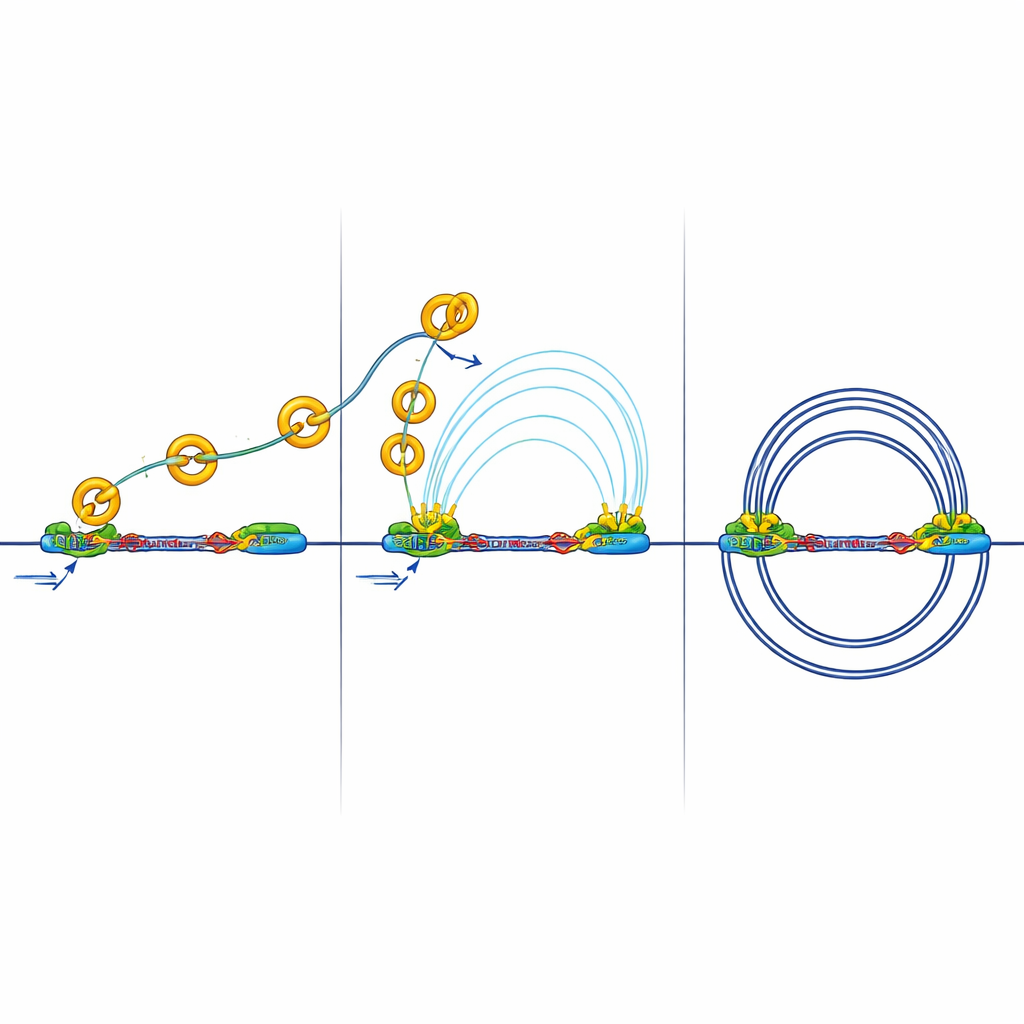
当绝缘阻断基因对话时
更强的边界会产生连锁反应。绝缘子可以阻断增强子与启动子之间的“长距离通话”,而这些通话对于基因激活是必需的。研究团队测量了由化学标记H3K27ac标识的活性DNA区域之间的物理接触。在缺失RB的细胞中,他们观察到增强子与启动子之间的接触更少且更弱,尽管许多激活标记仍然存在。换句话说,开关是打开的,但它们的信号难以越过被强化的边界。额外实验显示,通常帮助增强子与启动子沟通的关键介导复合体的招募减少,支持了是三维连线被扰动,而不仅仅是基本开/关标记改变的观点。
从DNA折叠到细胞行为
为了将这些结构性变化与真实基因及性状联系起来,作者关注那些启动子并未直接被RB或其常见伴侣因子结合,但位于绝缘子之外且在RB丢失时cohesin水平发生变化的基因。对于位于获得cohesin(因此绝缘更强)的绝缘子旁的基因,其表达在缺失RB的细胞中往往下降,尽管RB被移除时在全局范围内常常提高许多与生长相关基因的表达。这些受影响的基因富集于维持上皮特征和组织细胞外基质组织的功能——这些性状与细胞黏附程度和迁移容易性有关。
与这些基因变化一致,缺乏RB的细胞更容易从培养基底脱落,并且在人工“伤口”愈合实验中闭合得更快,这两者都是迁移性增强的信号。当作者按细胞周期将RB调控的基因进行分组时,鉴别出一小部分基因是由RB以激活而非抑制的方式调控的,这种激活依赖于RB在附近边界上放松绝缘的能力。这表明RB不仅仅作为增殖的刹车;它还作为特定基因组群的正调控因子,帮助维持正常组织结构。
这对癌症意味着什么
对非专业读者来说,核心信息是:RB守护细胞不仅通过阻止错误时机的分裂发挥作用,还通过塑造它们DNA的折叠和连线来发挥作用。通过促进从边界元件上移除cohesin,RB削弱了某些屏障,使重要的调控开关能够触及其目标基因。RB丢失时,这些边界变得过于强大,一些维持正常细胞身份的基因被沉默,细胞更容易脱落并迁移——这些性状可以助长肿瘤扩散和治疗抵抗。把RB视为基因组三维结构的“建筑师”这一扩展视角,有助于解释为何其丧失常常标志着肿瘤向更危险、难治方向的转折点。
引用: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
关键词: 视网膜母细胞瘤蛋白, 染色质环, cohesin, 三维基因组组织, 癌症进展