Clear Sky Science · pl
Utrata RB modyfikuje organizację chromatyny poprzez regulację pętli zależnych od cohesin i interakcji enhancer-promotor
Dlaczego menedżer opakowań komórki ma znaczenie
Każda komórka w twoim ciele musi upakować około dwóch metrów DNA w jądrze mniejszym niż drobinka kurzu. To, w jaki sposób DNA jest składane — nie tylko jakie geny zawiera — wpływa na to, które geny są włączane, a które wyłączane. Artykuł ten bada znane białko przeciwnowotworowe zwane RB i pokazuje, że robi ono znacznie więcej niż tylko hamuje niekontrolowane dzielenie komórek. RB pomaga także zarządzać trójwymiarowym składaniem DNA, precyzując, które geny mogą być osiągnięte przez pobliskie przełączniki kontrolne. Zrozumienie tej ukrytej roli daje nowe wskazówki, dlaczego nowotwory stają się agresywne po utracie RB.
Strażnik z ukrytą pracą
RB (skrót od retinoblastoma protein) jest najbardziej znany jako hamulec cyklu komórkowego. Zwykle utrzymuje grupę genów napędzających wzrost w stanie uśpienia, dopóki komórka nie będzie gotowa do podziału. Wiele nowotworów unieszkodliwia RB, co pozwala komórkom mnożyć się bez kontroli. Jednak nowotwory pozbawione RB wykazują też zagadkowe zmiany — takie jak zwiększona inwazyjność i zdolność do zmiany typu komórkowego — które nie wynikają jedynie z utraty hamulca cyklu komórkowego. Wcześniejsze badania sugerowały, że RB wiąże się nie tylko z inicjatorami genów (promotorami), ale także z odległymi elementami kontrolnymi (enhancerami) oraz specjalnymi miejscami „izolatorowymi”, które wyznaczają granice między sąsiedztwami aktywności DNA. To zasugerowało, że RB może pełnić funkcję organizatora składania genomu.
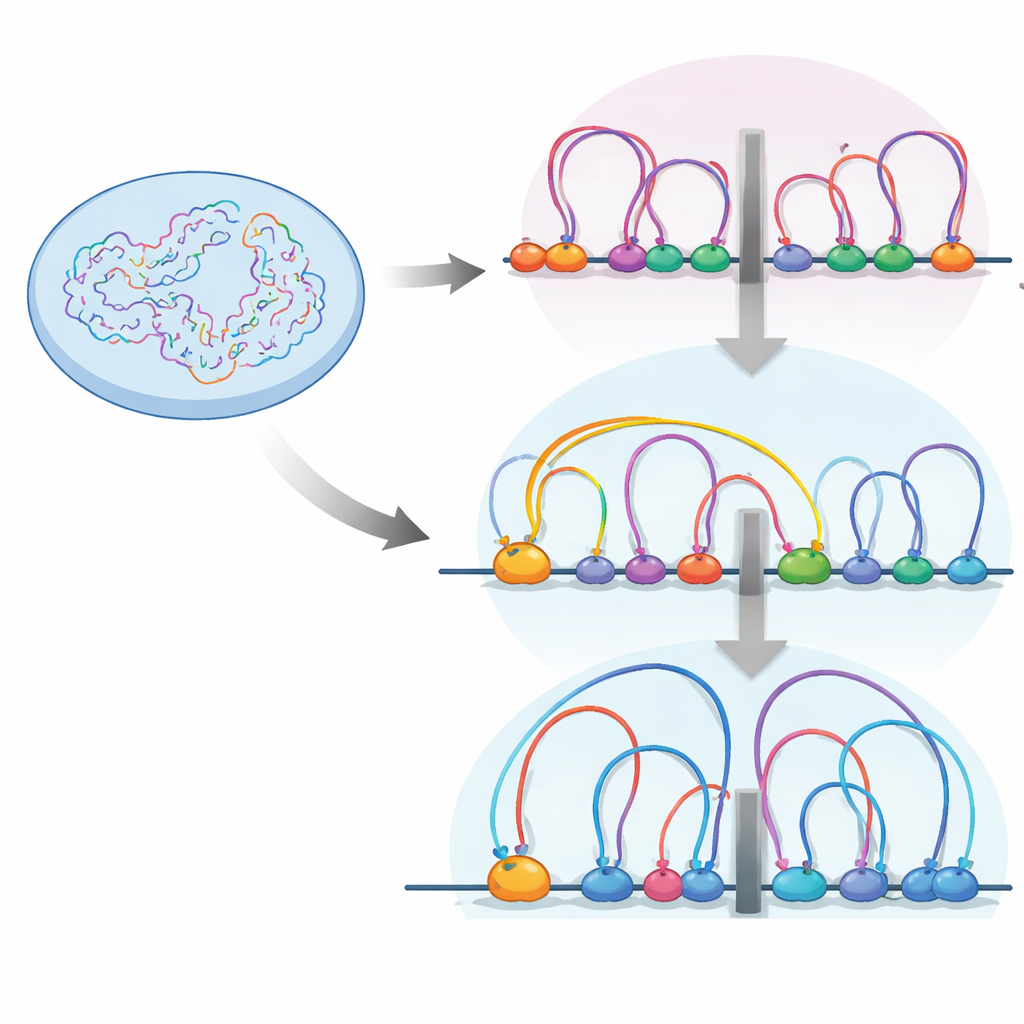
Pętle, granice i kontrola ruchu
W jądrze włókno DNA jest składane w pętle przez maszynę białkową zwaną cohesin. Te pętle grupują geny i ich elementy kontrolne w jednostki zwane topologicznie asocjującymi domenami, czyli TAD — w praktyce są to sąsiedztwa, w których geny i przełączniki łatwiej wchodzą ze sobą w interakcje. Granice między tymi sąsiedztwami często są oznaczone przez białko izolatorowe CTCF, gdzie cohesin ma tendencję do zatrzymywania się. Autorzy użyli wysokorozdzielczego mapowania kontaktów chromosomowych (Micro-C) oraz zestawu innych narzędzi genomowych, aby zobaczyć, jak włączanie lub wyłączanie RB przekształca krajobraz tych pętli w ludzkich komórkach siatkówki.
Stwierdzili, że gdy RB jest nieobecny, liczba i średni rozmiar pętli DNA wzrastają, a granice TAD stają się silniejsze. Jednocześnie RB i cohesin współwystępują w wielu dostępnych regionach genomu, zwłaszcza przy izolatorach. Szczegółowe mapowanie położenia cohesin w różnych fazach cyklu komórkowego wykazało, że RB jest potrzebny do usuwania cohesin z tych miejsc izolatorowych podczas mitozy, fazy, w której chromosomy kondensują się i ponownie rozluźniają. Bez RB cohesin akumuluje się przy izolatorach, wzmacniając granice i zmieniając sposób izolowania od siebie sąsiedztw DNA.
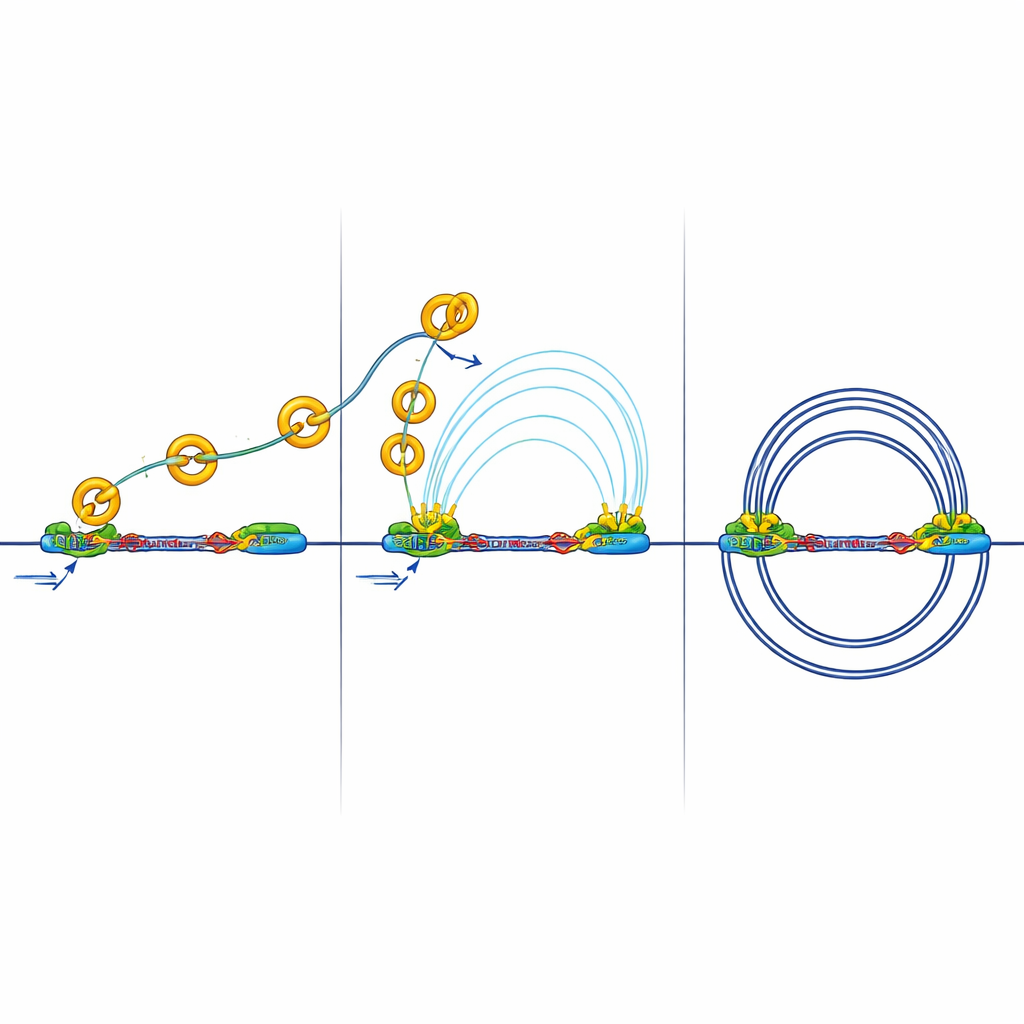
Gdy izolacja blokuje rozmowy genów
Mocniejsze granice mają konsekwencje. Izolatory mogą blokować „połączenia na duże odległości” między enhancerami a promotorami, które są potrzebne do aktywacji genów. Zespół mierzył fizyczne kontakty między aktywnymi regionami DNA oznaczonymi chemicznym znacznikiem H3K27ac. W komórkach pozbawionych RB zaobserwowali mniej i słabsze kontakty między enhancerami a promotorami, mimo że wiele znaczników aktywacji nadal było obecnych. Innymi słowy, przełączniki były włączone, ale ich sygnały miały trudności z przekroczeniem wzmocnionych granic. Dodatkowe eksperymenty wykazały zmniejszone rekrutowanie kluczowego kompleksu mediatorowego, który zwykle pomaga enhancerom komunikować się z promotorami, co wspiera tezę, że to okablowanie 3D, a nie podstawowe znaczniki włącz/wyłącz, zostało zaburzone.
Od składania DNA do zachowania komórek
Aby powiązać te zmiany architektoniczne z konkretnymi genami i cechami, autorzy skupili się na genach, których promotory nie są bezpośrednio związane z RB ani jego zwyczajowymi partnerami, lecz które leżą tuż poza izolatorami, gdzie poziomy cohesin zmieniają się po utracie RB. Dla genów znajdujących się przy izolatorach, które zyskały cohesin (a zatem silniejszą izolację), ekspresja miała tendencję do spadku w komórkach pozbawionych RB, chociaż ogólnie RB często podnosi wiele genów związanych z wzrostem po jego usunięciu. Te dotknięte geny były wzbogacone w funkcje związane z utrzymaniem cech nabłonka i organizacją macierzy zewnątrzkomórkowej — właściwości związane z tym, jak mocno komórki przylegają do siebie i jak łatwo się przemieszczają.
Zgodnie z tymi zmianami genowymi, komórki bez RB łatwiej odczepiały się od powierzchni hodowli i szybciej zamykały sztuczne „rany”, co jest sygnałem większej ruchliwości. Kiedy autorzy pogrupowali geny kontrolowane przez RB według zachowania w cyklu komórkowym, zidentyfikowali podzbiór genów, które RB rzeczywiście aktywuje, a nie hamuje, w sposób zależny od jego zdolności do rozluźniania izolacji przy pobliskich granicach. Sugeruje to, że RB nie działa tylko jako hamulec wzrostu; pełni też rolę pozytywnego regulatora dla określonych zestawów genów, które pomagają zachować normalną architekturę tkanek.
Co to znaczy dla nowotworów
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że RB chroni komórki nie tylko przez zatrzymywanie ich przed niewłaściwym dzieleniem, ale także przez kształtowanie sposobu, w jaki ich DNA jest składane i okablowane. Poprzez wspieranie usuwania cohesin z elementów granicznych, RB osłabia niektóre bariery i pozwala ważnym przełącznikom kontrolnym dotrzeć do docelowych genów. Gdy RB zostaje utracone, te granice stają się zbyt silne, niektóre geny utrzymujące normalną tożsamość komórkową zostają wyciszone, a komórki stają się bardziej skłonne do odłączania się i przemieszczania — cechy, które mogą napędzać rozprzestrzenianie się guza i oporność na leczenie. Poszerzone spojrzenie na RB jako architekta trójwymiarowej struktury genomu może pomóc wyjaśnić, dlaczego jego utrata często oznacza punkt zwrotny w kierunku bardziej niebezpiecznych, trudnych do leczenia nowotworów.
Cytowanie: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Słowa kluczowe: białko retinoblastoma, pętle chromatyny, cohesin, organizacja genomu 3D, progresja nowotworu