Clear Sky Science · ru
Потеря RB модулирует организацию хроматина через регуляцию когезин-зависимых петель и взаимодействий энхансер-промотор
Почему важен менеджер упаковки клетки
Каждая клетка вашего тела должна уместить около двух метров ДНК в ядре, меньшее по размеру, чем пылинка. То, как эта ДНК сложена — а не только какие гены она содержит — влияет на то, какие гены включаются или выключаются. В этой статье исследуется известный белок, защищающий от рака, RB, и показано, что он делает гораздо больше, чем просто останавливает неконтролируемое деление клеток. RB также помогает управлять трехмерной укладкой ДНК, тонко регулируя, какие гены доступны для соседних регуляторных переключателей. Понимание этой скрытой роли дает новые подсказки о том, как опухоли становятся агрессивными при утрате RB.
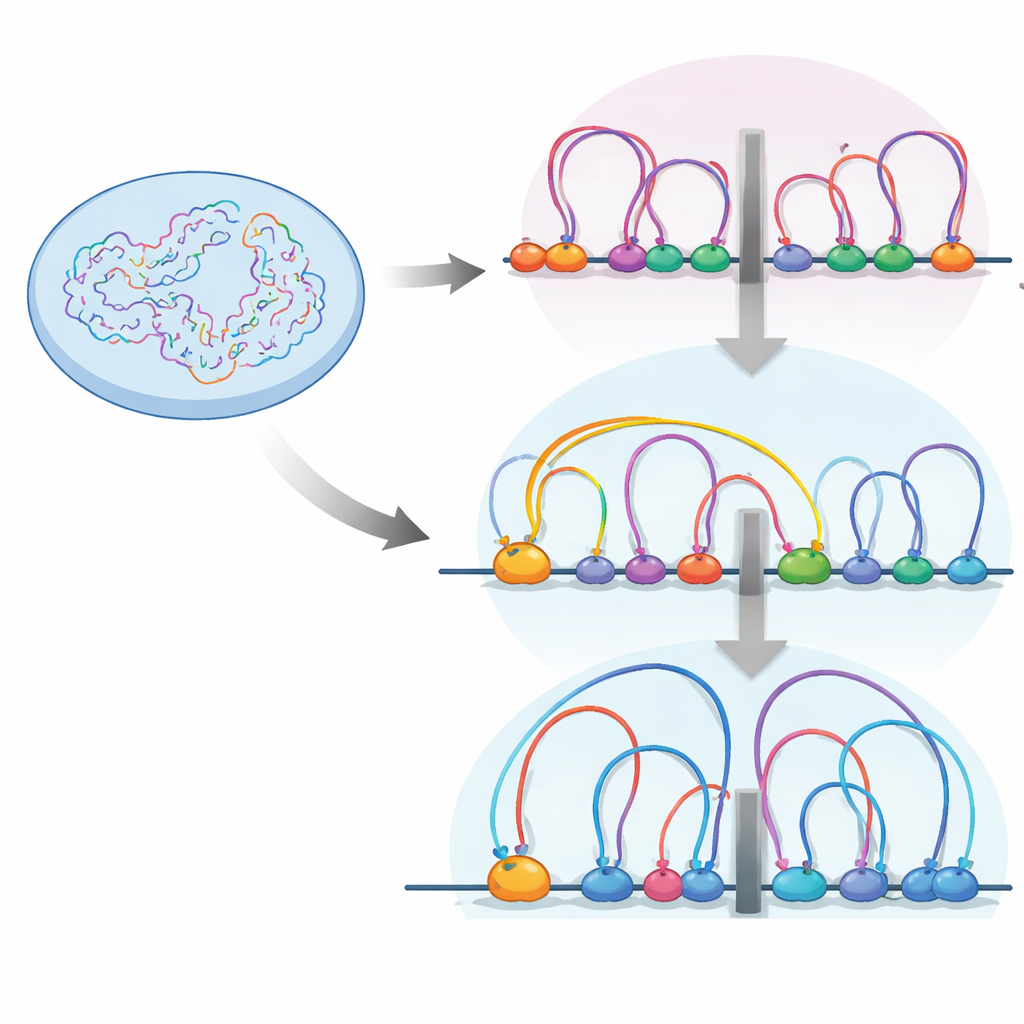
Хранитель с скрытой функцией
RB (сокращение от ретинобластомного белка) наиболее известен как тормоз клеточного цикла. Обычно он удерживает в «молчании» набор генов, стимулирующих рост, пока клетка не будет готова разделиться. Многие опухоли деактивируют RB, что позволяет клеткам бесконтрольно размножаться. Однако у раков с дефицитом RB наблюдаются и загадочные изменения — например, повышенная инвазивность и способность менять тип клетки — которые нельзя объяснить только потерей контроля за клеточным циклом. Ранее было показано, что RB связывается не только с стартовыми участками генов (промоторами), но и с удалёнными регуляторными областями (энхансерами) и специальными «изолирующими» сайтами, которые отмечают границы между районами активности ДНК. Это наводит на мысль, что RB может также выступать организатором укладки генома.
Петли, границы и регулирование движения
Внутри ядра ДНК складывается в петли при помощи белковой машины — когезина. Эти петли помогают сгруппировать гены и их регуляторы в единицы, называемые топологически ассоциированными доменами, или TAD — по сути соседства, внутри которых гены и переключатели взаимодействуют свободнее. Границы между такими соседствами часто отмечены белком-изолятором CTCF, где когезин имеет тенденцию останавливаться. Авторы использовали высокоразрешающее картирование контактов хромосом (Micro-C) и набор других геномных инструментов, чтобы увидеть, как включение или выключение RB перестраивает ландшафт петель в человеческих сетчаточных клетках.
Они обнаружили, что при отсутствии RB число петель и их средний размер увеличиваются, а границы TAD становятся более выраженными. В то же время RB и когезин совместно локализуются во многих доступных областях генома, особенно на изоляторах. Детальное картирование расположения когезина на разных стадиях клеточного цикла показало, что RB необходим для удаления когезина с этих изолирующих сайтов в митозе — фазе, когда хромосомы конденсируются, а затем снова раскрываются. Без RB когезин накапливается на изоляторах, укрепляя границы и меняя то, как соседства ДНК изолированы друг от друга.
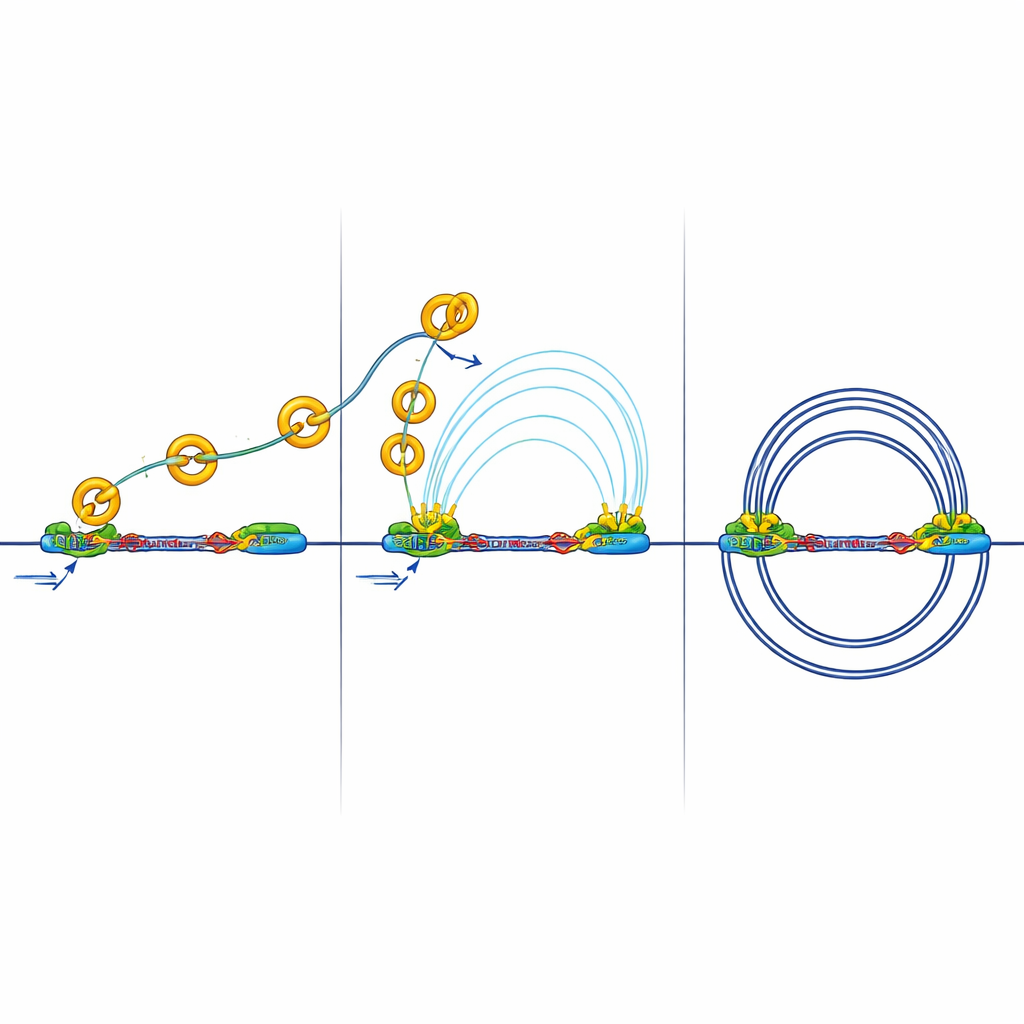
Когда изоляция блокирует «разговоры» генов
Усиленные границы имеют последствия. Изоляторы могут блокировать «дальние вызовы» между энхансерами и промоторами, необходимые для активации генов. Команда измеряла физические контакты между активными участками ДНК, помеченными химическим маркером H3K27ac. В клетках без RB они наблюдали меньше и слабее контакты между энхансерами и промоторами, хотя многие метки активации по-прежнему были присутствуют. Иными словами, переключатели были включены, но их сигналы сталкивались с трудностями при пересечении усиленных границ. Дополнительные эксперименты показали снижение привлечения ключевого медиаторного комплекса, который обычно помогает энхансерам общаться с промоторами, что поддерживает идею о том, что нарушается именно 3D-проводка, а не базовые метки вкл/выкл.
От укладки ДНК к поведению клетки
Чтобы связать архитектурные изменения с конкретными генами и чертами, авторы сосредоточились на генах, чьи промоторы напрямую не связаны с RB или его обычными партнёрами, но которые расположены сразу за изолятором, где уровни когезина меняются при потере RB. Для генов рядом с изоляторами, где когезина стало больше (и, следовательно, изоляция усилилась), экспрессия в RB-дефицитных клетках, как правило, снижалась, хотя в целом утрата RB часто повышает многие гены, связанные с ростом. Эти затронутые гены были обогащены функциями, связанными с поддержанием эпителиальных свойств и организацией внеклеточного матрикса — характеристиками, связанными с тем, насколько плотно клетки сцеплены друг с другом и как легко они могут передвигаться.
В соответствии с этими изменениями в экспрессии, клетки без RB легче отрывались от поверхности культуры и быстрее закрывали искусственные «раны» — оба признака повышенной подвижности. Когда авторы группировали гены, контролируемые RB, по поведению в клеточном цикле, они выделили подмножество, которые RB на самом деле активирует, а не репрессирует, и это зависит от его способности ослаблять изоляцию на близлежащих границах. Это говорит о том, что RB не только действует как тормоз роста; он также служит положительным регулятором для определённых наборов генов, которые помогают сохранять нормальную архитектуру тканей.
Что это значит для рака
Для неспециалистов ключевое сообщение заключается в том, что RB защищает клетки не только, останавливая их деление в неподходящее время, но и формируя, как их ДНК сложена и устроена в пространстве. Продвигая удаление когезина с элементов границы, RB ослабляет определённые барьеры и позволяет важным регуляторным переключателям достигать своих целевых генов. При потере RB эти границы становятся чрезмерно сильными, некоторые гены, поддерживающие нормальную клеточную идентичность, выключаются, и клетки становятся более склонными к отрыву и миграции — черты, которые могут способствовать распространению опухоли и устойчивости к лечению. Это расширённое видение RB как архитектора 3D-структуры генома может помочь объяснить, почему его утрата часто становится поворотным моментом на пути к более опасным, трудно лечимым формам рака.
Цитирование: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Ключевые слова: белок ретинобластомы, петли хроматина, когезин, 3D-организация генома, прогрессирование рака