Clear Sky Science · tr
RB kaybı, cohesin bağımlı döngüler ve enhanser-promotor etkileşimlerini düzenleyerek kromatin organizasyonunu değiştirir
Hücrenin Paketleyicisi Neden Önemli?
Vücudunuzdaki her hücre, yaklaşık iki metre uzunluğundaki DNA’yı toz tanesinden küçük bir çekirdeğe sıkıştırmak zorundadır. Bu DNA’nın nasıl katlandığı—taşıdığı genlerden öte—hangi genlerin açılıp kapandığını belirlemede önem taşır. Bu makale, RB adıyla bilinen ünlü bir kanserle savaşçı proteini inceliyor ve onun sadece kontrolsüz hücre bölünmesini durdurmaktan fazlasını yaptığını ortaya koyuyor. RB ayrıca DNA’nın üç boyutlu katlanmasını yönetmeye yardımcı olarak, hangi genlere komşu kontrol anahtarlarının (enhancer’ların) erişebileceğini ince ayarlıyor. Bu gizli rolün anlaşılması, kanserlerin RB’yi kaybettiklerinde neden daha agresif hâle geldiklerine dair yeni ipuçları sunuyor.
Gizli Görevli Bir Koruyucu
RB (retinoblastoma proteininin kısaltması) en çok hücre döngüsünde bir fren olarak bilinir. Normalde hücrenin bölünmeye hazır olana kadar bir dizi büyümeyi destekleyen geni susturur. Birçok tümör RB’yi devre dışı bırakır; bu da hücrelerin kontrolsüz çoğalmasına izin verir. Ancak RB eksikliği gösteren kanserler, yalnızca bu döngü freninin kaybıyla açıklanamayan artmış invazivlik ve hücre tipini değiştirme yeteneği gibi şaşırtıcı değişiklikler sergiler. Önceki çalışmalar RB’nin yalnızca gen başlatıcılarına (promoter’lara) değil, aynı zamanda uzak kontrol bölgelerine (enhancer’lara) ve DNA aktivite mahalleleri arasındaki sınırları işaretleyen özel “yalıtıcı” bölgelere de bağlandığını gösteriyordu. Bu da RB’nin genomun katlanmasının bir düzenleyicisi olma olasılığını gündeme getirdi.
Döngüler, Sınırlar ve Trafik Kontrolü
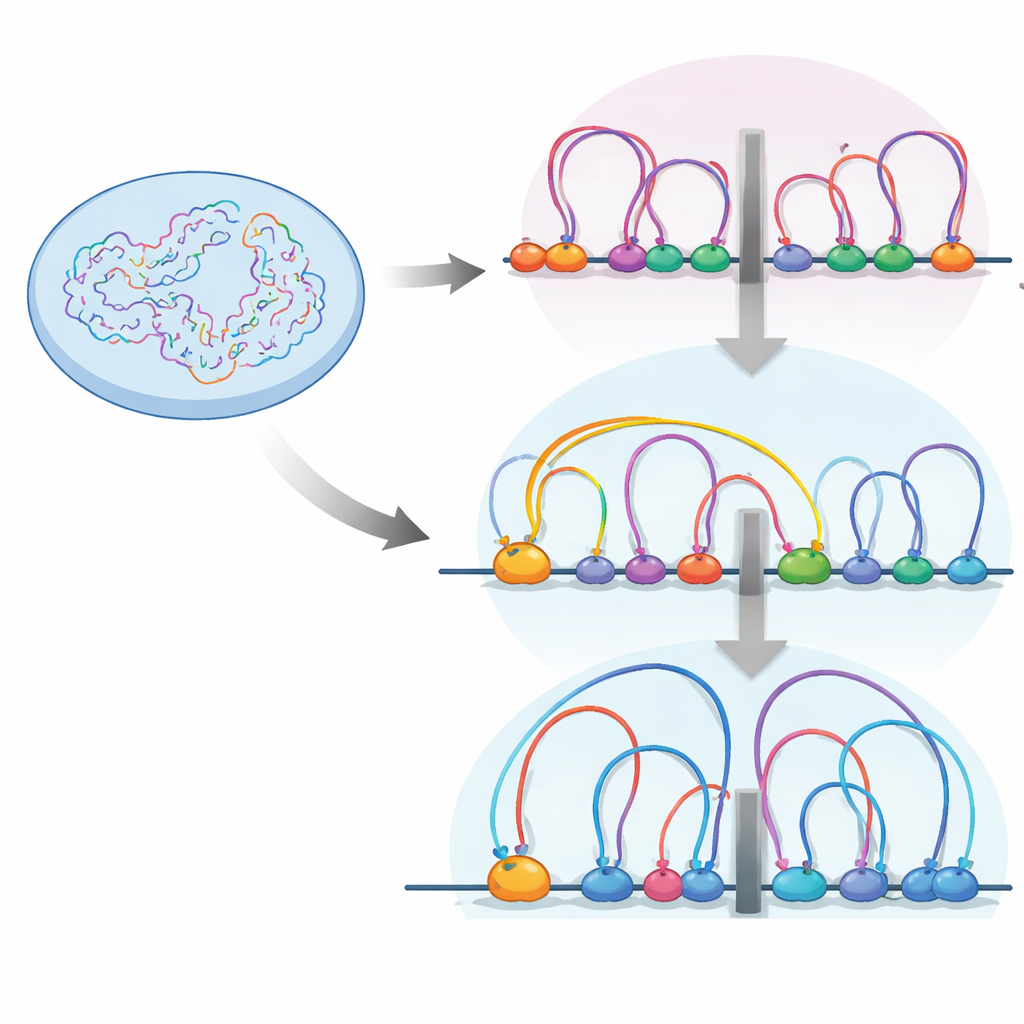
Çekirdek içinde DNA ipliği cohesin adlı bir protein makinesi tarafından döngülere katlanır. Bu döngüler, genleri ve kontrol elemanlarını topolojik ilişki alanları (TAD’ler) denilen birimler halinde gruplandırmaya yardımcı olur—temelde genlerin ve anahtarların daha serbestçe etkileşebildiği mahalleler. Bu mahalleler arasındaki sınırlar genellikle CTCF adlı bir yalıtıcı proteinle işaretlenir; cohesin burada duraklama eğilimindedir. Yazarlar, RB’nin açılıp kapatılmasının insan retina hücrelerinde bu döngü manzarasını nasıl yeniden şekillendirdiğini görmek için yüksek çözünürlüklü kromozom temas haritalama (Micro-C) ve bir dizi diğer genomik aracı kullandılar.
RB eksik olduğunda DNA döngülerinin sayısının ve ortalama boyutunun arttığını ve TAD sınırlarının güçlendiğini buldular. Aynı zamanda RB ve cohesin birçok genomik erişilebilir bölgeye, özellikle yalıtıcı noktalara birlikte oturuyordu. Farklı hücre döngüsü aşamalarında cohesin’in konumunun ayrıntılı haritalanması, RB’nin mitoz sırasında—kromozomların yoğunlaşıp yeniden açıldığı aşama—bu yalıtıcılardan cohesin’in uzaklaştırılmasına yardımcı olmak için gerekli olduğunu gösterdi. RB olmadan cohesin yalıtıcı bölgelerde birikiyor, sınırları güçlendiriyor ve DNA mahallelerinin birbirinden nasıl izole edildiğini değiştiriyordu.
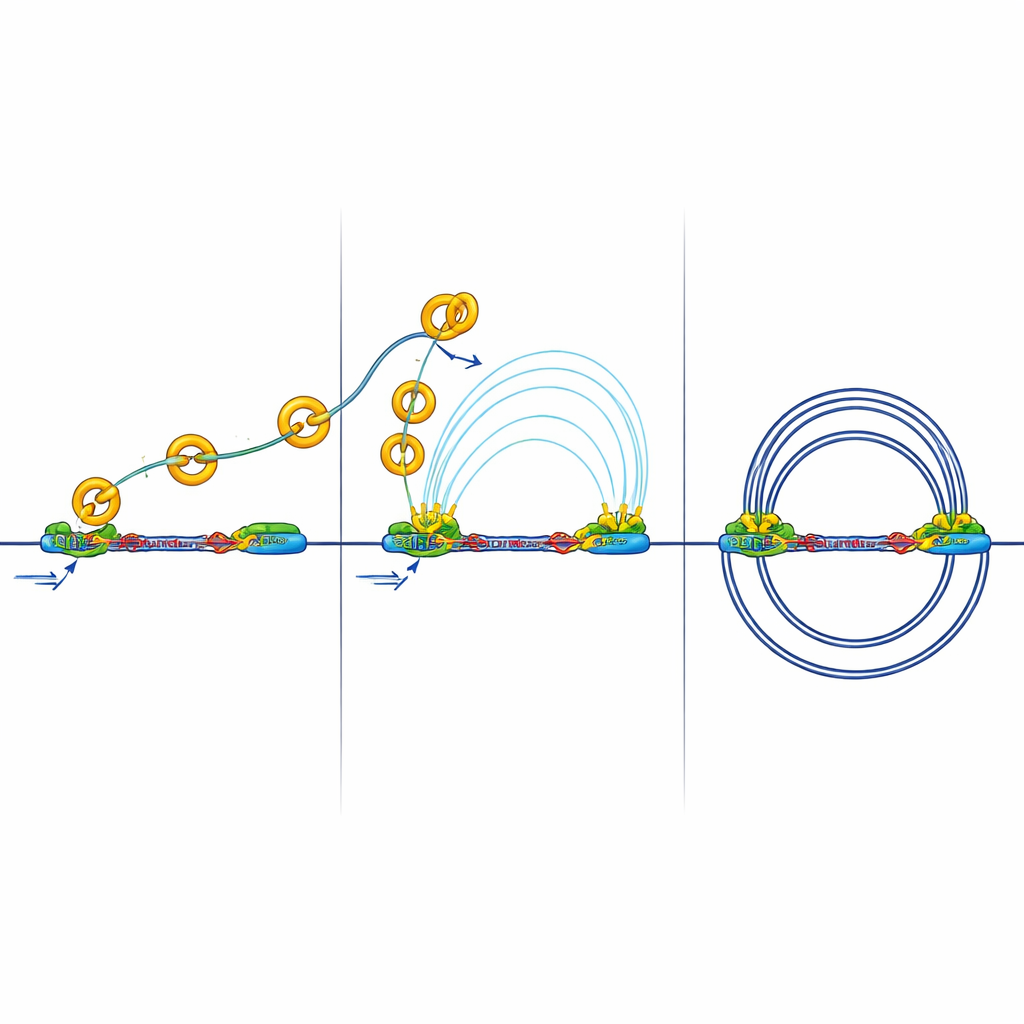
Yalıtma Gen Diyaloglarını Engellediğinde
Daha güçlü sınırların sonuçları vardır. Yalıtıcılar, genleri aktifleştirmek için gerekli olan enhancer’lar ile promoter’lar arasındaki “uzak çağrıları” engelleyebilir. Ekip, H3K27ac adlı kimyasal işaretle aktif bölgeler arasındaki fiziksel temasları ölçtü. RB eksik hücrelerde, birçok aktivasyon işareti hâlâ mevcut olmasına rağmen enhancer‑promoter arasındaki temasların daha az ve daha zayıf olduğunu gördüler. Başka bir deyişle, anahtarlar açıktı, ancak sinyaller güçlendirilmiş sınırları aşmakta zorlanıyordu. İlave deneyler, normalde enhancer’ların promoter’larla konuşmasına yardımcı olan önemli bir aracı kompleksin daha az çekildiğini gösterdi; bu da temel açma/kapama işaretlerinden ziyade üç boyutlu bağlantıların bozulduğunu destekliyor.
DNA Katlanmasından Hücre Davranışına
Bu mimari değişiklikleri gerçek genlere ve özelliklere bağlamak için yazarlar, promoter’ları doğrudan RB’ye veya onun olağan ortak faktörlerine bağlanmayan, ancak RB kaybı olduğunda cohesin düzeylerinin değiştiği bir yalıtıcının hemen ötesinde yer alan genlere odaklandılar. Cohesin kazanan (dolayısıyla daha güçlü yalıtım gösteren) yalıtıcıların yanındaki genlerin ifadesi, RB eksik hücrelerde genellikle düştü; oysa RB genelde kaldırıldığında birçok büyüme ile ilgili geni küresel olarak artırıyordu. Etkilenen bu genler, epitel özelliklerini sürdürme ve hücrenin çevresindeki matriksi organize etme rollerinde zenginleşmişti—hücrelerin ne kadar sıkı yapıştığı ve ne kadar kolay hareket ettiği ile bağlantılı özellikler.
Bu gen değişiklikleriyle tutarlı olarak, RB’siz hücreler kültür yüzeyinden daha kolay ayrıldı ve yapay “yaraları” daha hızlı kapattı; bunlar her ikisi de artmış hareketliliğin işaretleri. Yazarlar RB tarafından kontrol edilen genleri hücre döngüsü boyunca davranışlarına göre gruplayınca, RB’nin aslında baskılamaktan ziyade etkinleştirdiği bir alt küme tanımladılar; bu etkinleştirme RB’nin yakınlardaki sınırlarda yalıtımı gevşetme yeteneğine bağlıydı. Bu, RB’nin sadece büyümeyi frenleyen bir eleman olmadığını; aynı zamanda normal doku mimarisini korumaya yardımcı olan belirli gen kümeleri için pozitif bir düzenleyici görevi de gördüğünü öne sürer.
Bu Kanser İçin Ne Anlama Geliyor?
Uzman olmayanlar için temel mesaj şudur: RB, hücreleri sadece yanlış zamanda bölünmelerini durdurarak korumaz; aynı zamanda DNA’larının nasıl katlandığını ve kablolandığını biçimlendirir. Cohesin’in sınır elemanlarından uzaklaştırılmasını teşvik ederek RB, bazı bariyerleri zayıflatır ve önemli kontrol anahtarlarının hedef genlere ulaşmasına izin verir. RB kaybolduğunda bu sınırlar çok güçlenir, normal hücre kimliğini koruyan bazı genler susturulur ve hücreler kopmaya ve göç etmeye daha yatkın hâle gelir—bu özellikler tümör yayılımını ve tedavi direncini körükleyebilir. RB’nin genomun 3B yapısının bir mimarı olarak genişletilmiş bu görünümü, onun kaybının neden sıklıkla daha tehlikeli, tedavisi zor kanserlere geçişi işaretlediğini açıklamaya yardımcı olabilir.
Atıf: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Anahtar kelimeler: retinoblastoma proteini, kromatin döngüleri, cohesin, 3B genom organizasyonu, kanser ilerlemesi