Clear Sky Science · it
La perdita di RB modula l’organizzazione della cromatina regolando i loop dipendenti da cohesina e le interazioni enhancer-promotore
Perché conta il gestore del pacchetto della cellula
Ogni cellula del tuo corpo deve comprimere circa due metri di DNA in un nucleo più piccolo di un granello di polvere. Il modo in cui quel DNA è ripiegato — non solo i geni che contiene — contribuisce a decidere quali geni vengono attivati o silenziati. Questo articolo esplora una nota proteina oncosoppressiva chiamata RB e rivela che fa molto più che fermare la divisione cellulare incontrollata. RB aiuta anche a gestire il ripiegamento tridimensionale del DNA, modulando quali geni possono essere raggiunti dagli interruttori di controllo vicini. Comprendere questo ruolo nascosto offre nuovi indizi su come i tumori diventino più aggressivi quando perdono RB.
Un guardiano con un lavoro nascosto
RB (abbreviazione di proteina del retinoblastoma) è conosciuto soprattutto come freno del ciclo cellulare. Normalmente mantiene silenziosi un insieme di geni che promuovono la crescita finché la cellula non è pronta a dividersi. Molti tumori disabilitano RB, permettendo alle cellule di moltiplicarsi in modo incontrollato. Eppure i tumori privi di RB mostrano anche cambiamenti sorprendenti — come una maggiore invasività e la capacità di cambiare tipo cellulare — che non si spiegano solo con la perdita del freno sul ciclo cellulare. Lavori precedenti avevano suggerito che RB si lega non solo ai promotori dei geni ma anche a regioni di controllo distanti (enhancer) e a siti “isolatori” speciali che segnano i confini tra quartieri di attività del DNA. Questo ha sollevato la possibilità che RB agisca anche come organizzatore del ripiegamento del genoma.
Loop, confini e controllo del traffico
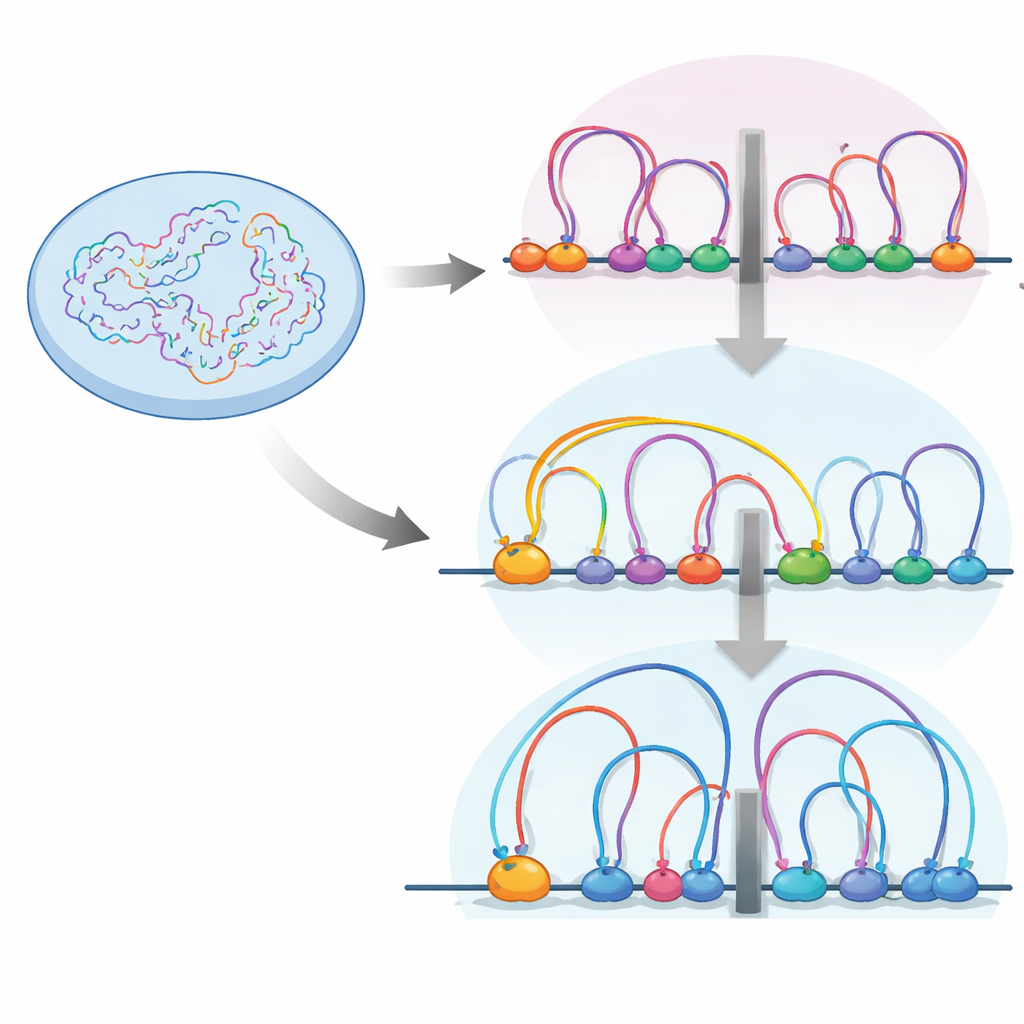
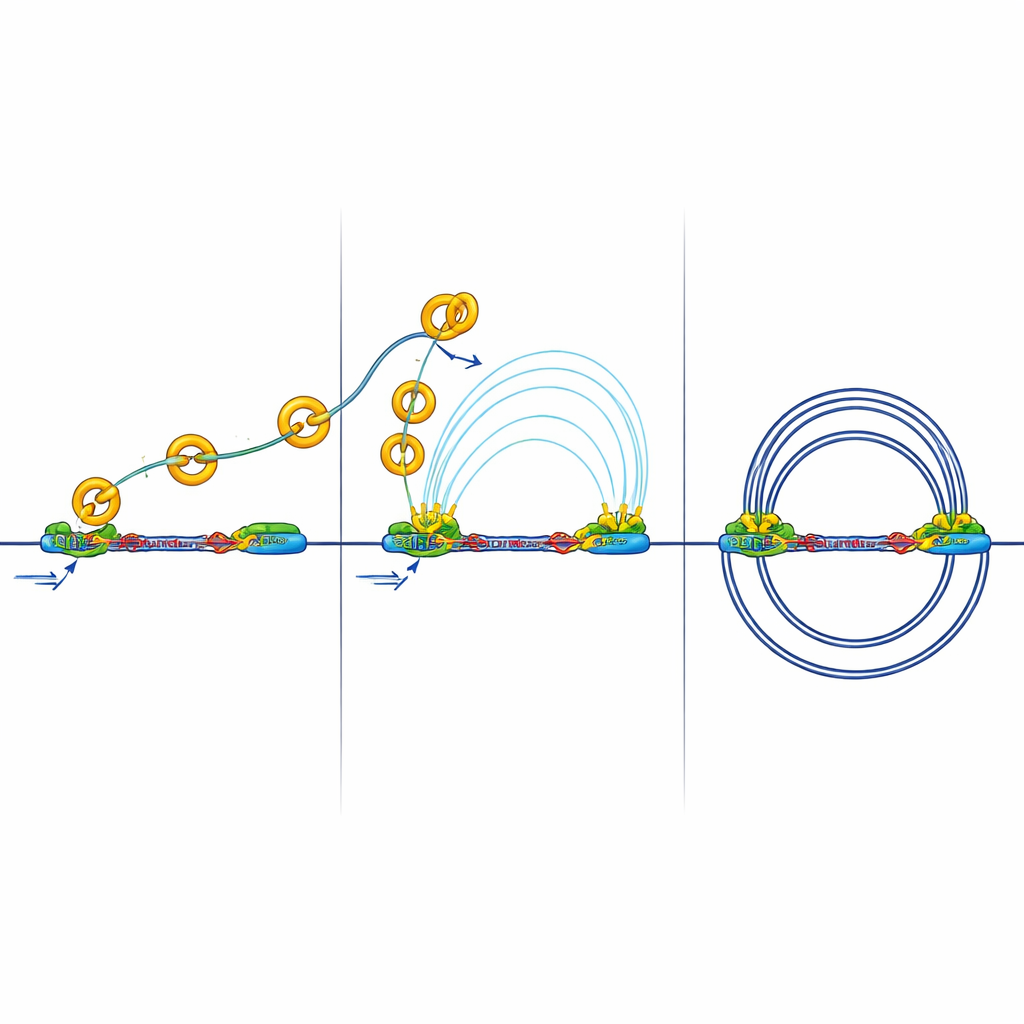
All’interno del nucleo, la fibra di DNA viene ripiegata in loop da una macchina proteica chiamata cohesina. Questi loop aiutano a raggruppare geni e i loro elementi di controllo in unità chiamate domini di associazione topologica, o TAD — essenzialmente quartieri entro i quali geni e interruttori interagiscono più liberamente. I confini tra questi quartieri sono spesso segnati da una proteina isolatrice chiamata CTCF, dove la cohesina tende a fermarsi. Gli autori hanno usato mappature ad alta risoluzione dei contatti cromosomici (Micro-C) e una serie di altri strumenti genomici per vedere come l’accensione o lo spegnimento di RB rimodella questo paesaggio di loop in cellule retiniche umane.
Hanno scoperto che quando RB manca, aumentano sia il numero sia la dimensione media dei loop di DNA, e i confini dei TAD diventano più forti. Allo stesso tempo, RB e la cohesina co-localizzano in molte regioni accessibili del genoma, specialmente agli isolatori. Una mappatura dettagliata della posizione della cohesina durante le diverse fasi del ciclo cellulare ha mostrato che RB è necessario per aiutare a rimuovere la cohesina da questi siti isolatori durante la mitosi, la fase in cui i cromosomi si condensano e poi si riaprono. Senza RB, la cohesina si accumula agli isolatori, rafforzando i confini e cambiando il modo in cui i quartieri del DNA sono isolati l’uno dall’altro.
Quando l’isolamento blocca le conversazioni geniche
I confini più forti hanno conseguenze. Gli isolatori possono bloccare le “chiamate a lunga distanza” tra enhancer e promotori necessarie per attivare i geni. Il gruppo ha misurato i contatti fisici tra regioni attive del DNA contrassegnate da un marcatore chimico chiamato H3K27ac. Nelle cellule prive di RB hanno osservato contatti tra enhancer e promotori meno numerosi e più deboli, nonostante molti segni di attivazione fossero ancora presenti. In altre parole, gli interruttori erano attivati, ma i loro segnali faticavano a oltrepassare i confini rinforzati. Esperimenti aggiuntivi hanno mostrato un ridotto reclutamento di un complesso mediatore chiave che normalmente aiuta gli enhancer a dialogare con i promotori, a supporto dell’idea che ciò che viene alterato è il cablaggio 3D piuttosto che i semplici marchi on/off.
Dal ripiegamento del DNA al comportamento cellulare
Per collegare questi cambiamenti architettonici a geni e tratti reali, gli autori si sono concentrati su geni i cui promotori non sono legati direttamente da RB o dai suoi partner abituali, ma che si trovano appena oltre un isolatore dove i livelli di cohesina cambiano quando RB viene perso. Per i geni vicini a isolatori che hanno accumulato cohesina (e quindi un’isolazione più forte), l’espressione tendeva a diminuire nelle cellule prive di RB, sebbene RB spesso aumenti globalmente molti geni legati alla crescita quando viene rimosso. Questi geni interessati risultavano arricchiti per ruoli nel mantenimento delle caratteristiche epiteliali e nell’organizzazione della matrice extracellulare — proprietà legate a quanto saldamente le cellule si attaccano tra loro e a quanto facilmente si muovono.
Coerentemente con questi cambiamenti genici, le cellule senza RB si staccavano più facilmente dalla superficie di coltura e chiudevano più in fretta “ferite” artificiali, entrambi segnali di maggiore mobilità. Quando gli autori raggrupparono i geni controllati da RB in base al comportamento nel corso del ciclo cellulare, identificarono un sottoinsieme che RB attiva effettivamente, piuttosto che reprimere, in modo dipendente dalla sua capacità di allentare l’isolamento ai confini vicini. Questo suggerisce che RB non agisce solo come un freno alla crescita; serve anche come regolatore positivo per insiemi specifici di geni che aiutano a preservare l’architettura tessutale normale.
Cosa significa questo per il cancro
Per i non specialisti, il messaggio chiave è che RB protegge le cellule non solo impedendo loro di dividersi al momento sbagliato, ma anche plasmando il modo in cui il loro DNA è ripiegato e cablato. Promuovendo la rimozione della cohesina dagli elementi di confine, RB indebolisce certe barriere e permette agli interruttori di controllo importanti di raggiungere i geni bersaglio. Quando RB viene perso, questi confini diventano troppo forti, alcuni geni che mantengono l’identità cellulare normale vengono silenziati e le cellule diventano più propense a staccarsi e migrare — tratti che possono alimentare la diffusione tumorale e la resistenza ai trattamenti. Questa visione ampliata di RB come architetto della struttura 3D del genoma può aiutare a spiegare perché la sua perdita segna spesso una svolta verso tumori più pericolosi e difficili da trattare.
Citazione: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Parole chiave: proteina del retinoblastoma, loop della cromatina, cohesina, organizzazione 3D del genoma, progressione del cancro