Clear Sky Science · es
Pérdida de RB modula la organización de la cromatina regulando bucles dependientes de cohesina e interacciones enhancers-promotores
Por qué importa el gestor del empaquetado celular
Cada célula de tu cuerpo debe compactar unos dos metros de ADN en un núcleo más pequeño que una mota de polvo. La forma en que ese ADN se pliega—no solo los genes que contiene—ayuda a decidir qué genes se activan o se silencian. Este artículo explora una proteína famosa por su papel en la defensa contra el cáncer llamada RB y revela que hace mucho más que frenar la división celular descontrolada. RB también contribuye a gestionar el plegamiento tridimensional del ADN, afinando qué genes pueden ser alcanzados por interruptores regulatorios cercanos. Comprender este papel oculto ofrece nuevas pistas sobre cómo los cánceres se vuelven agresivos cuando pierden RB.
Un guardián con un trabajo oculto
RB (abreviatura de proteína del retinoblastoma) es más conocida por actuar como freno del ciclo celular. Normalmente mantiene en silencio un conjunto de genes que impulsan el crecimiento hasta que la célula está lista para dividirse. Muchos tumores inactivan RB, lo que permite a las células multiplicarse sin control. Sin embargo, los cánceres deficientes en RB también muestran cambios desconcertantes—como mayor invasividad y la capacidad de cambiar de tipo celular—que no pueden explicarse únicamente por la pérdida de este freno del ciclo celular. Trabajos previos sugerían que RB se une no solo a los iniciadores de genes (promotores) sino también a regiones de control distantes (enhancers) y a sitios “aislantes” especiales que marcan los límites entre vecindarios de actividad del ADN. Esto planteó la posibilidad de que RB también actuara como organizador del plegamiento del genoma.
Bucles, límites y control del tráfico
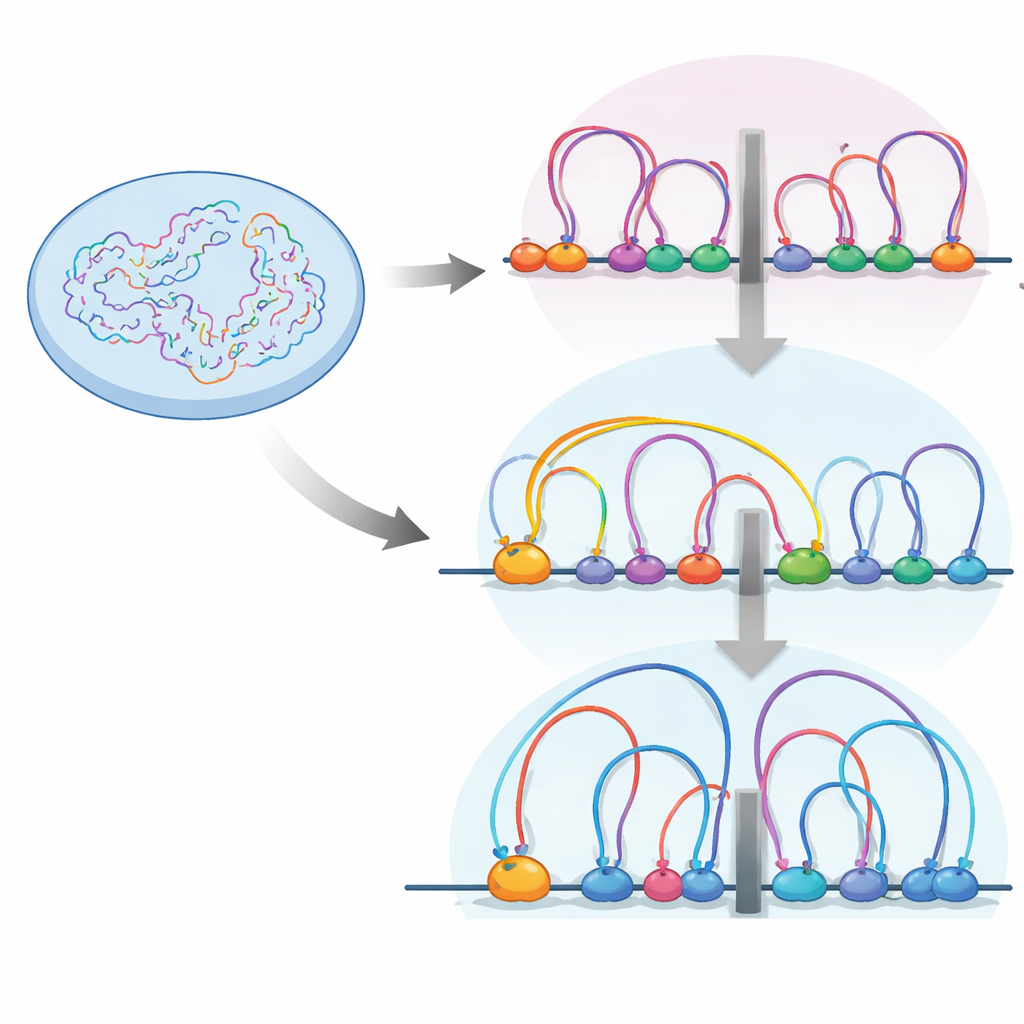
Dentro del núcleo, la fibra de ADN se pliega en bucles gracias a una máquina proteica llamada cohesina. Estos bucles ayudan a agrupar genes y sus elementos de control en unidades llamadas dominios de asociación topológica, o TADs—esencialmente vecindarios dentro de los cuales genes e interruptores interactúan con más facilidad. Los límites entre estos vecindarios suelen estar marcados por una proteína aislante llamada CTCF, donde la cohesina tiende a detenerse. Los autores usaron un mapeo de contactos cromosómicos de alta resolución (Micro-C) y una batería de otras herramientas genómicas para ver cómo encender o apagar RB remodela este paisaje de bucles en células retinianas humanas.
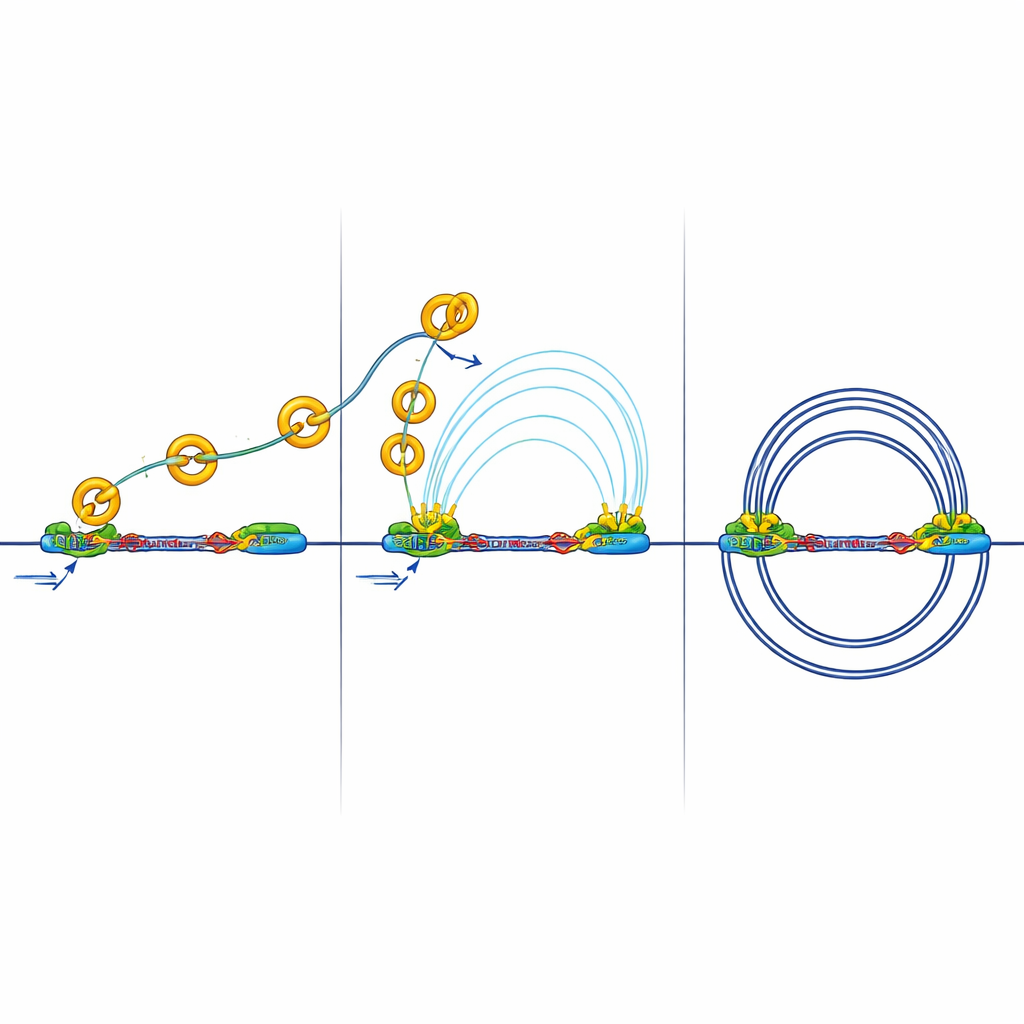
Encontraron que cuando RB falta, aumentan tanto el número como el tamaño medio de los bucles de ADN, y los límites de los TAD se vuelven más fuertes. Al mismo tiempo, RB y la cohesina se localizan juntos en muchas regiones accesibles del genoma, especialmente en aislantes. Un mapeo detallado de la ubicación de la cohesina durante distintas etapas del ciclo celular mostró que RB es necesario para ayudar a eliminar la cohesina de estos sitios aislantes durante la mitosis, la fase en la que los cromosomas se condensan y luego se reabren. Sin RB, la cohesina se acumula en los aislantes, reforzando los límites y cambiando cómo se aíslan entre sí los vecindarios de ADN.
Cuando el aislamiento bloquea las conversaciones génicas
Los límites más fuertes tienen consecuencias. Los aislantes pueden bloquear las “llamadas a larga distancia” entre enhancers y promotores que se necesitan para activar genes. El equipo midió contactos físicos entre regiones activas del ADN marcadas por una etiqueta química llamada H3K27ac. En células sin RB, observaron contactos entre enhancers y promotores menos frecuentes y más débiles, aunque muchas marcas de activación seguían presentes. En otras palabras, los interruptores estaban encendidos, pero sus señales tenían dificultades para cruzar los límites reforzados. Experimentos adicionales mostraron una reducción en el reclutamiento de un complejo mediador clave que normalmente ayuda a que los enhancers dialoguen con los promotores, lo que respalda la idea de que lo que se altera es el cableado 3D, más que las marcas básicas de encendido/apagado.
Del plegamiento del ADN al comportamiento celular
Para vincular estos cambios arquitectónicos con genes y rasgos reales, los autores se centraron en genes cuyos promotores no están directamente unidos por RB ni por sus factores asociados habituales, pero que se sitúan justo más allá de un aislante donde los niveles de cohesina cambian cuando se pierde RB. Para los genes próximos a aislantes que ganaron cohesina (y por tanto mayor aislamiento), la expresión tendió a disminuir en células deficientes en RB, aunque RB suele aumentar globalmente muchos genes relacionados con el crecimiento cuando se elimina. Estos genes afectados estaban enriquecidos en funciones relacionadas con el mantenimiento de rasgos epiteliales y la organización de la matriz que rodea a la célula—propiedades vinculadas a cuán fuertemente las células se adhieren entre sí y a qué facilidad se mueven.
En consonancia con estos cambios en la expresión génica, las células sin RB se desprendieron con más facilidad de la superficie de cultivo y cerraron “heridas” artificiales más rápido, ambas señales de mayor movilidad. Cuando los autores agruparon los genes controlados por RB según su comportamiento a lo largo del ciclo celular, identificaron un subconjunto que RB en realidad activa, en lugar de reprimir, de una manera que depende de su capacidad para aflojar el aislamiento en límites cercanos. Esto sugiere que RB no actúa solo como freno del crecimiento; también sirve como regulador positivo de conjuntos específicos de genes que ayudan a preservar la arquitectura normal de los tejidos.
Qué significa esto para el cáncer
Para quienes no son especialistas, el mensaje clave es que RB protege a las células no solo impidiendo que se dividan en momentos inadecuados, sino también moldeando cómo se pliega y cablea su ADN. Al promover la eliminación de la cohesina de elementos límite, RB debilita ciertas barreras y permite que interruptores de control importantes lleguen a sus genes diana. Cuando se pierde RB, estos límites se vuelven demasiado fuertes, algunos genes que mantienen la identidad celular normal se silencian y las células son más propensas a desprenderse y migrar—rasgos que pueden alimentar la diseminación tumoral y la resistencia al tratamiento. Esta visión ampliada de RB como arquitecto de la estructura 3D del genoma puede ayudar a explicar por qué su pérdida con frecuencia marca un punto de inflexión hacia cánceres más peligrosos y difíciles de tratar.
Cita: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Palabras clave: proteína del retinoblastoma, bucles de cromatina, cohesina, organización 3D del genoma, progresión del cáncer