Clear Sky Science · sv
Förlust av RB förändrar kromatinorganisation genom att reglera cohesinberoende slingor och enhancer-promotor-interaktioner
Varför cellens pakethanterare spelar roll
Varje cell i din kropp måste stoppa ungefär två meter DNA i en kärna som är mindre än ett dammkorn. Hur det DNA:t är vikt — inte bara vilka gener det bär — hjälper till att avgöra vilka gener som slås på eller av. Denna artikel undersöker ett välkänt cancerbekämpande protein kallat RB och visar att det gör mycket mer än att bara stoppa okontrollerad celldelning. RB hjälper också till att hantera DNA:s tredimensionella veckning och finjusterar vilka gener som kan nås av närliggande styrspakar. Att förstå denna dolda roll ger nya ledtrådar till hur cancer blir aggressiv när den förlorar RB.
En väktare med en dold uppgift
RB (kort för retinoblastomprotein) är mest känd som en broms i cellcykeln. Det håller normalt igen en uppsättning tillväxtdrivande gener tills cellen är redo att dela sig. Många tumörer inaktiverar RB, vilket låter celler föröka sig okontrollerat. Ändå visar RB-bristande cancerformer också förbryllande förändringar — såsom ökad invasivitet och förmåga att byta celltyp — som inte enbart kan förklaras av förlusten av denna cellcykelbroms. Tidigare arbete antydde att RB binder inte bara till genstartare (promotorer) utan också till avlägsna kontrollregioner (enhancers) och särskilda ”isolator”-platser som markerar gränser mellan DNA-aktivitetens kvarter. Det väckte möjligheten att RB också kan fungera som en organisatör av genomets veckning.
Slingor, gränser och trafikstyrning
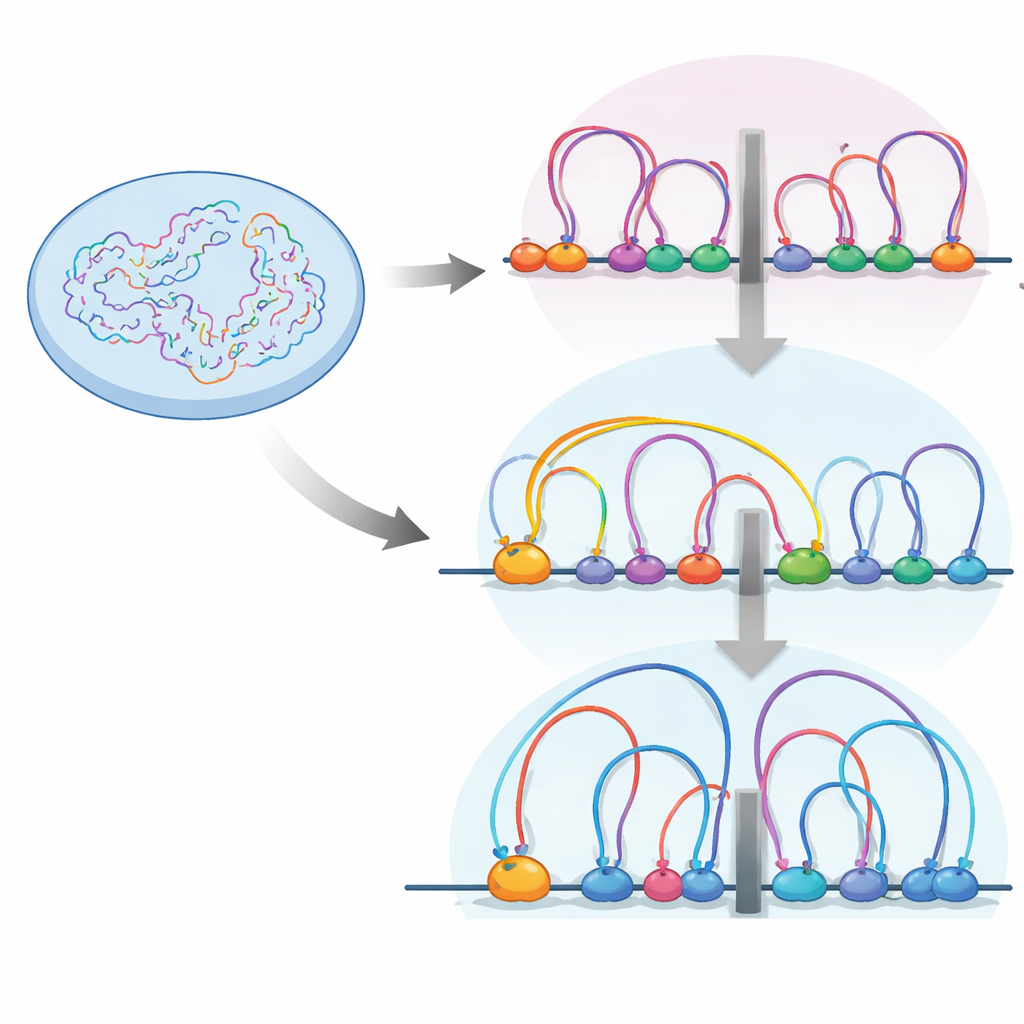
Inne i kärnan viks DNA-fibern i slingor av en proteinkomplex kallat cohesin. Dessa slingor hjälper till att gruppera gener och deras kontrollapparater till enheter kallade topologiskt associerande domäner, eller TADs — i praktiken kvarter inom vilka gener och strömbrytare interagerar mer fritt. Gränser mellan dessa kvarter markeras ofta av ett isolatorprotein kallat CTCF, där cohesin tenderar att pausa. Författarna använde högupplöst kromosomkontaktkartläggning (Micro-C) och en uppsättning andra genomiska verktyg för att se hur aktivering eller avstängning av RB omformar detta slinglandskap i mänskliga retinala celler.
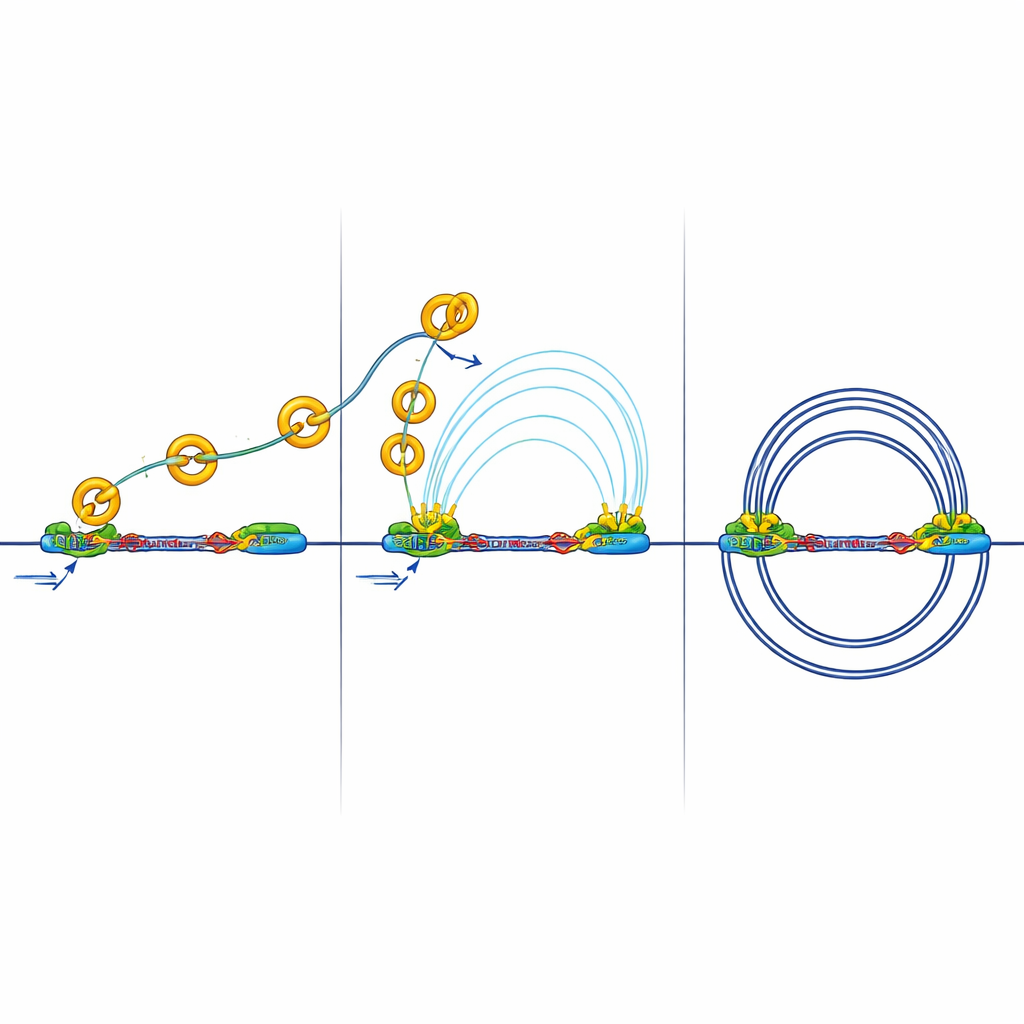
De fann att när RB saknas ökar antalet och medelstorleken på DNA-slingor, och TAD-gränser blir starkare. Samtidigt sitter RB och cohesin tillsammans vid många tillgängliga regioner över genomet, särskilt vid isolatorer. Detaljerad kartläggning av cohesins position under olika cellcykelstadier visade att RB behövs för att hjälpa till att avlägsna cohesin från dessa isolatorplatser under mitos, fasen då kromosomer kondenserar och sedan öppnar upp igen. Utan RB byggs cohesin upp vid isolatorer, vilket förstärker gränser och ändrar hur DNA-kvarteren isoleras från varandra.
När isolering blockerar genkonversationer
Starkare gränser får konsekvenser. Isolatorer kan blockera de ”långdistanssamtal” mellan enhancers och promotorer som krävs för att aktivera gener. Gruppen mätte fysiska kontakter mellan aktiva DNA-regioner märkta med en kemisk markör kallad H3K27ac. I celler utan RB såg de färre och svagare kontakter mellan enhancers och promotorer, även om många aktiveringsmarkörer fortfarande fanns kvar. Med andra ord var strömbrytarna på, men deras signaler hade svårt att ta sig över de förstärkta gränserna. Ytterligare experiment visade minskat rekryterande av ett viktigt mediator-complex som normalt hjälper enhancers att prata med promotorer, vilket stöder idén att den tredimensionella kopplingen, snarare än de grundläggande av-/på-markörerna, stördes.
Från DNA-veckning till cellbeteende
För att koppla dessa arkitektoniska förändringar till riktiga gener och egenskaper fokuserade författarna på gener vars promotorer inte är direkt bundna av RB eller dess vanliga partnerfaktorer, men som ligger precis bortom en isolator där cohesinnivåerna förändras när RB förloras. För gener intill isolatorer som fick mer cohesin (och därmed starkare isolering) tenderade uttrycket att minska i RB-deficienta celler, även om RB ofta globalt höjer många tillväxtrelaterade gener när det tas bort. De påverkade generna var berikade för roller i att bibehålla epiteliala egenskaper och organisera cellens omgivande matris — egenskaper kopplade till hur tätt celler sitter ihop och hur lätt de rör sig.
I linje med dessa genförändringar lossnade celler utan RB lättare från odlingsytan och stängde artificiella ”sår” snabbare, båda tecken på ökad rörlighet. När författarna grupperade RB-kontrollerade gener efter beteende under cellcykeln identifierade de en undergrupp som RB faktiskt aktiverar, snarare än repressionerar, på ett sätt som beror på dess förmåga att luckra upp isolering vid närliggande gränser. Detta tyder på att RB inte bara fungerar som en broms för tillväxt; det tjänar också som en positiv regulator för specifika genuppsättningar som hjälper till att bevara normal vävnadsarkitektur.
Vad detta betyder för cancer
För icke-specialister är huvudbudskapet att RB skyddar celler inte bara genom att stoppa dem från att dela sig vid fel tidpunkt utan också genom att forma hur deras DNA är vikt och kopplat. Genom att främja borttagning av cohesin från gränselement försvagar RB vissa barriärer och tillåter viktiga kontrollströmbrytare att nå sina mål. När RB förloras blir dessa gränser för starka, vissa gener som upprätthåller normal cellidentitet tystas, och celler blir mer benägna att lossna och migrera — egenskaper som kan driva tumörspridning och behandlingsmotstånd. Denna utvidgade syn på RB som en arkitekt för genomets 3D-struktur kan hjälpa till att förklara varför dess förlust så ofta markerar en vändpunkt mot mer farliga, svårbehandlade cancerformer.
Citering: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Nyckelord: retinoblastomprotein, kromatinloopar, cohesin, 3D-genomorganisation, cancerprogression