Clear Sky Science · pt
A perda de RB modula a organização da cromatina ao regular loops dependentes de cohesina e interações enhancer-promotor
Por que o organizador da célula importa
Cada célula do seu corpo precisa enfiar cerca de dois metros de DNA dentro de um núcleo menor que um grão de poeira. A maneira como esse DNA é dobrado — não apenas quais genes ele carrega — ajuda a determinar quais genes são ativados ou silenciados. Este artigo investiga uma conhecida proteína antitumoral chamada RB e revela que ela faz muito mais do que frear a divisão celular desenfreada. RB também ajuda a gerir o enrolamento tridimensional do DNA, ajustando finamente quais genes podem ser alcançados por interruptores regulatórios próximos. Entender esse papel oculto fornece novas pistas sobre como os cânceres se tornam agressivos quando perdem RB.
Um guardião com um trabalho oculto
RB (abreviação de proteína retinoblastoma) é mais conhecida como um freio do ciclo celular. Normalmente, mantém um conjunto de genes promotores do crescimento silenciosos até que a célula esteja pronta para se dividir. Muitos tumores inativam RB, o que permite que as células se multipliquem descontroladamente. No entanto, cânceres deficientes em RB também exibem mudanças enigmáticas — como maior invasividade e a capacidade de mudar de tipo celular — que não podem ser explicadas apenas pela perda desse freio do ciclo celular. Trabalhos anteriores sugeriram que RB se liga não apenas a inícios de genes (promotores), mas também a regiões regulatórias distantes (enhancers) e a locais especiais chamados “isoladores” que marcam as fronteiras entre bairros de atividade do DNA. Isso levantou a possibilidade de que RB também atue como um organizador do dobramento do genoma.
Loops, fronteiras e controle de tráfego
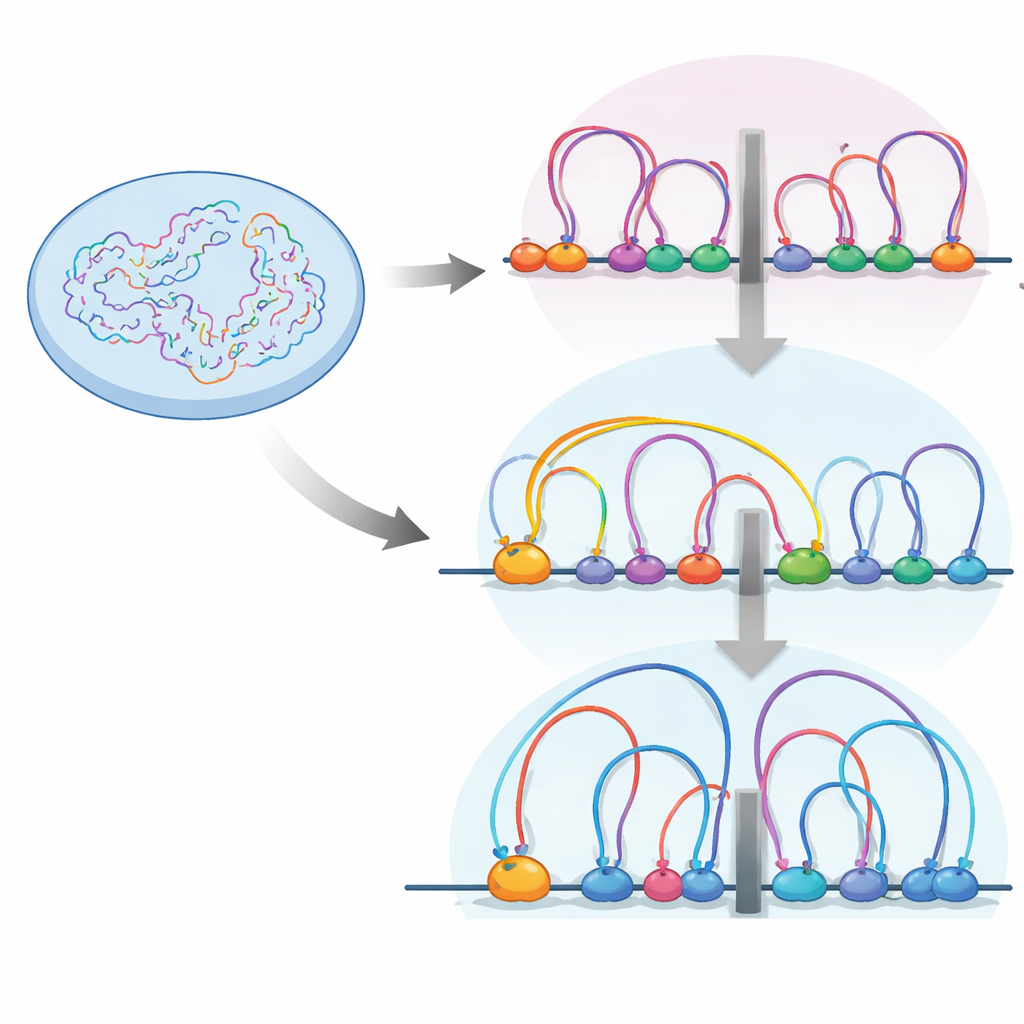
Dentro do núcleo, a fibra de DNA é dobrada em loops por uma máquina protéica chamada cohesina. Esses loops ajudam a agrupar genes e seus elementos regulatórios em unidades chamadas domínios de associação topológica, ou TADs — essencialmente bairros dentro dos quais genes e interruptores interagem com mais liberdade. As fronteiras entre esses bairros são frequentemente marcadas por uma proteína isoladora chamada CTCF, onde a cohesina tende a pausar. Os autores usaram mapeamento de contatos cromossômicos em alta resolução (Micro-C) e um conjunto de outras ferramentas genômicas para ver como ligar ou desligar RB remodela esse panorama de loops em células da retina humana.
Descobriram que, quando RB está ausente, o número e o tamanho médio dos loops de DNA aumentam, e as fronteiras dos TADs se tornam mais fortes. Ao mesmo tempo, RB e a cohesina se localizam juntos em muitas regiões acessíveis do genoma, especialmente em isoladores. Mapear detalhadamente a localização da cohesina durante diferentes estágios do ciclo celular mostrou que RB é necessário para ajudar a remover a cohesina desses sítios isoladores durante a mitose, a fase em que os cromossomos se condensam e depois se reabrem. Sem RB, a cohesina se acumula nos isoladores, reforçando as fronteiras e alterando como os bairros de DNA ficam isolados uns dos outros.
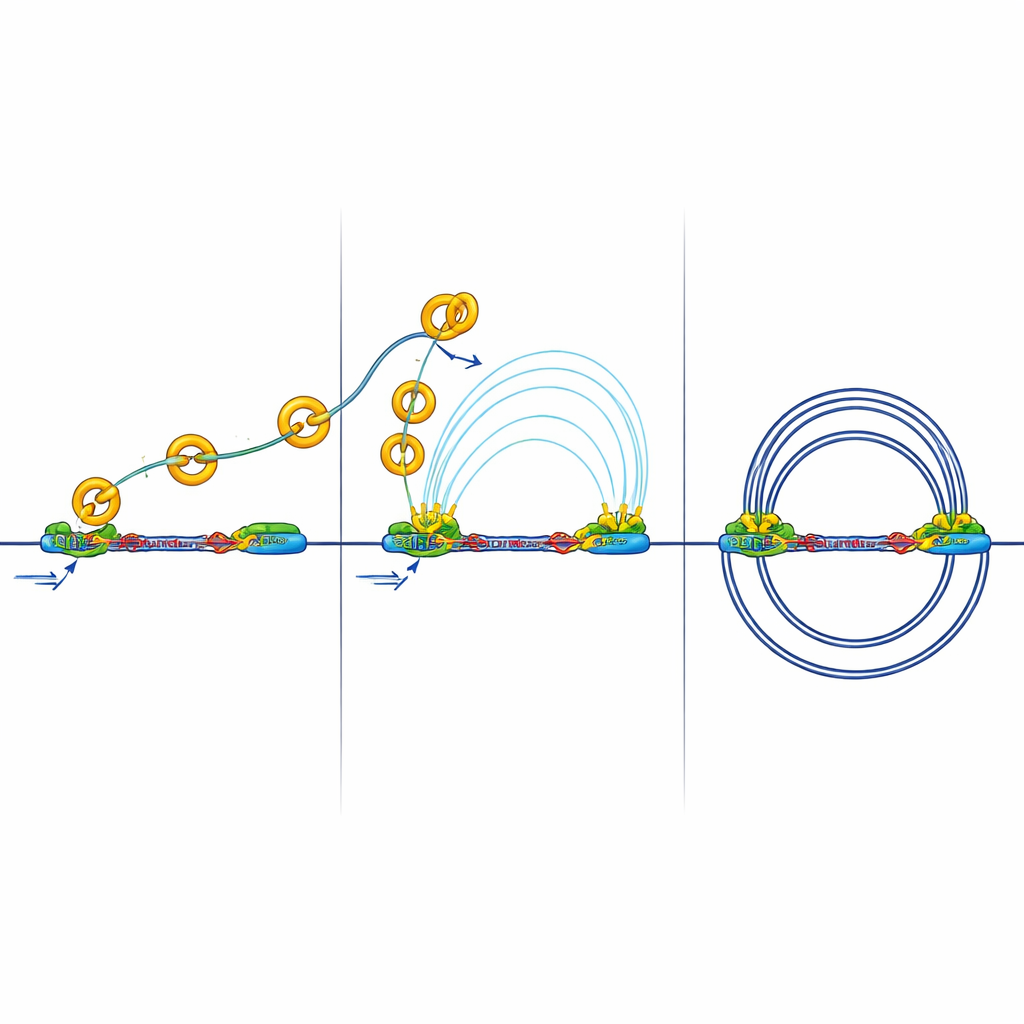
Quando a isolação bloqueia as conversas gênicas
Fronteiras mais fortes têm consequências. Isoladores podem bloquear as “chamadas de longa distância” entre enhancers e promotores necessárias para ativar genes. A equipe mediu contatos físicos entre regiões ativas do DNA marcadas por uma marca química chamada H3K27ac. Em células sem RB, observaram contatos entre enhancers e promotores menos numerosos e mais fracos, mesmo que muitas marcas de ativação ainda estivessem presentes. Em outras palavras, os interruptores estavam ligados, mas seus sinais tinham dificuldade para atravessar as fronteiras reforçadas. Experimentos adicionais mostraram recrutamento reduzido de um complexo mediador chave que normalmente ajuda enhancers a se comunicarem com promotores, corroborando a ideia de que a fiação 3D, e não apenas as marcas básicas de ligado/desligado, estava sendo perturbada.
Do dobramento do DNA ao comportamento celular
Para ligar essas mudanças arquiteturais a genes e características reais, os autores concentraram-se em genes cujos promotores não são diretamente ligados por RB ou seus parceiros habituais, mas que se situam logo além de um isolador onde os níveis de cohesina mudam quando RB é perdido. Para genes ao lado de isoladores que ganharam cohesina (e, portanto, maior isolamento), a expressão tendia a cair em células deficientes em RB, embora RB frequentemente aumente globalmente muitos genes relacionados ao crescimento quando é removido. Esses genes afetados eram enriquecidos em funções de manutenção de características epiteliais e organização da matriz extracelular — propriedades relacionadas a quão aderidas as células ficam entre si e à facilidade com que se movem.
Em consonância com essas alterações gênicas, células sem RB se desprendiam mais facilmente da superfície da cultura e fecharam “feridas” artificiais mais rapidamente, ambos sinais de maior mobilidade. Quando os autores agruparam genes controlados por RB segundo o comportamento ao longo do ciclo celular, identificaram um subconjunto que RB de fato ativa, em vez de reprimir, de uma maneira que depende de sua capacidade de afrouxar o isolamento em fronteiras próximas. Isso sugere que RB não age apenas como um freio ao crescimento; também funciona como um regulador positivo para conjuntos específicos de genes que ajudam a preservar a arquitetura normal do tecido.
O que isso significa para o câncer
Para não especialistas, a mensagem-chave é que RB protege as células não apenas impedindo-as de se dividir no momento errado, mas também moldando como seu DNA é dobrado e conectado. Ao promover a remoção da cohesina de elementos de fronteira, RB enfraquece certas barreiras e permite que interruptores importantes alcancem seus genes-alvo. Quando RB é perdido, essas fronteiras ficam fortes demais, alguns genes que mantêm a identidade celular normal são silenciados e as células ficam mais propensas a se desprender e migrar — características que podem impulsionar a disseminação tumoral e a resistência ao tratamento. Essa visão ampliada de RB como arquiteto da estrutura 3D do genoma pode ajudar a explicar por que sua perda muitas vezes marca um ponto de virada rumo a cânceres mais perigosos e difíceis de tratar.
Citação: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Palavras-chave: proteína retinoblastoma, loops de cromatina, cohesina, organização 3D do genoma, progressão do câncer