Clear Sky Science · ja
RBの喪失はコヒーシン依存のループとエンハンサー–プロモーター相互作用を制御してクロマチン構造を変調する
なぜ細胞の“パッケージ管理者”が重要なのか
体内のあらゆる細胞は、約二メートルのDNAをほこり粒より小さな核に詰め込まなければなりません。DNAがどのように折りたたまれているか――単にどの遺伝子を持っているかだけでなく――が、どの遺伝子がオンになるかオフになるかを左右します。本論文は有名ながん抑制タンパク質であるRBを調べ、単に細胞分裂を止める以上の役割を果たしていることを示します。RBはDNAの三次元的な折りたたみを管理し、近くの制御スイッチがどの遺伝子に届くかを微調整しているのです。この隠れた役割を理解することで、RBを失ったときにがんが攻撃的になる仕組みに新たな手がかりが得られます。
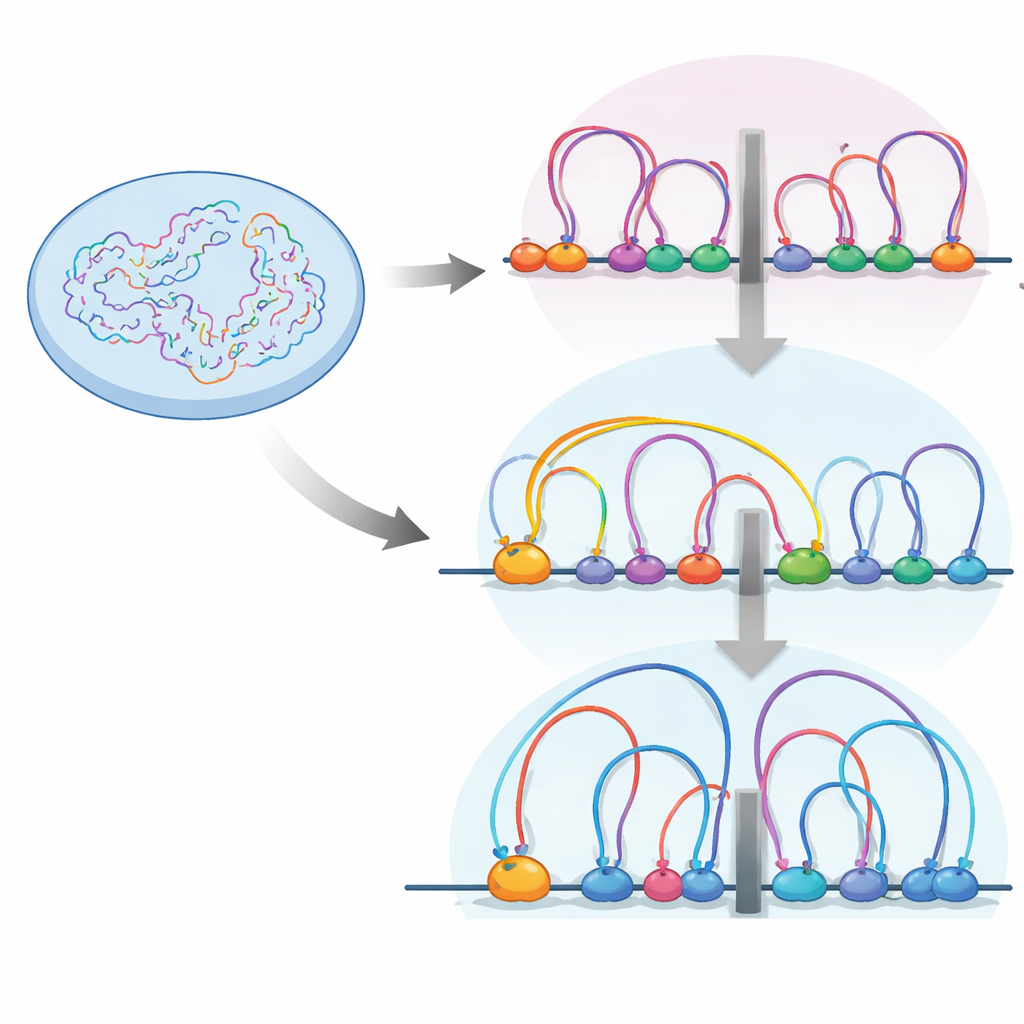
守護者の隠れた仕事
RB(網膜芽細胞腫タンパク質の略)は細胞周期のブレーキとして最もよく知られています。通常、細胞が分裂の準備が整うまで成長を促す一群の遺伝子を抑えます。多くの腫瘍はRBを無効化し、細胞が制御なく増殖するようにします。しかし、RB欠損のがんは浸潤性の増加や細胞型の転換など、単に細胞周期のブレーキを失っただけでは説明できない変化も示します。先行研究はRBがプロモーター(遺伝子の開始領域)だけでなく遠方の制御領域(エンハンサー)や、DNA活動の“近隣”境界を示す特別な「インシュレーター」部位にも結合することを示唆していました。これにより、RBがゲノム折りたたみのオーガナイザーとして働く可能性が浮上しました。
ループ、境界、そして交通整理
核内ではDNA繊維がコヒーシンと呼ばれるタンパク質機構によってループ状に折りたたまれます。これらのループは遺伝子とその制御要素をトポロジカルに相互作用するドメイン(TAD)という単位にまとめ、いわば遺伝子とスイッチがより自由にやり取りする“近隣”を形成します。これらの近隣の境界は多くの場合、CTCFというインシュレータータンパク質によってマークされ、コヒーシンが停止しやすい場所になっています。著者らは高解像度染色体接触マッピング(Micro-C)と一連のゲノミクス手法を用いて、ヒト網膜細胞でRBのオン・オフがこのループ景観をどのように再構築するかを調べました。
その結果、RBが欠損するとDNAループの数と平均サイズが増加し、TAD境界が強化されることが分かりました。同時に、RBとコヒーシンはゲノム全体の多くのアクセス可能領域、特にインシュレーターで共存していました。細胞周期の異なる段階でのコヒーシン位置を詳細にマッピングしたところ、RBは有糸分裂期(染色体が凝縮して再び開く段階)においてこれらインシュレーターからコヒーシンを除去するのを助ける必要があることが示されました。RBがないとコヒーシンがインシュレーターに蓄積し、境界が強化されてDNAの近隣間の隔離の仕方が変わります。
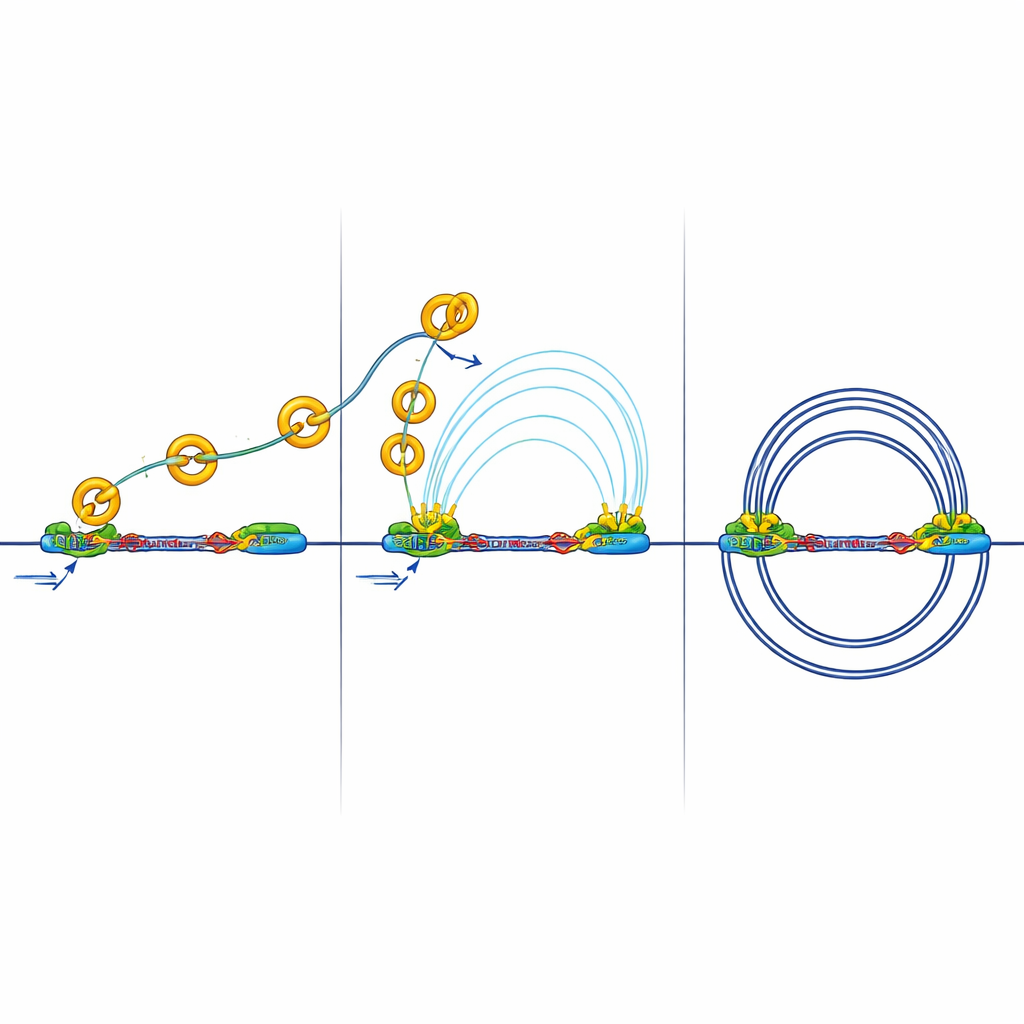
絶縁が遺伝子の“会話”を遮るとき
境界の強化は影響をもたらします。インシュレーターはエンハンサーとプロモーター間の“長距離通話”を遮断して、遺伝子活性化に必要なやり取りを阻害することがあります。研究チームはH3K27acという化学的マークで示される活性領域間の物理的接触を測定しました。RB欠損細胞では、エンハンサーとプロモーター間の接触が減少し弱まっているのが観察されましたが、多くの活性化マーク自体はまだ存在していました。言い換えれば、スイッチはオンになっていたものの、その信号は強化された境界を越えて伝わりにくくなっていたのです。追加実験では、エンハンサーがプロモーターと対話するのを助ける主要なメディエーター複合体の呼び寄せが減少していることが示され、基本的なオン/オフのマークではなく3次元の配線が乱されているという考えを支持しました。
DNAの折りたたみから細胞の振る舞いへ
これらの構造変化を実際の遺伝子と形質に結びつけるため、著者らはプロモーターに直接RBやその通常のパートナー因子が結合していないが、インシュレーターのすぐ先に位置し、RB喪失時にコヒーシン量が変化する遺伝子に注目しました。コヒーシンが増加し(したがって隔離が強化され)たインシュレーターの隣にある遺伝子では、RB欠損細胞で発現が低下する傾向がありました。これはRBが除去されると全般的に多くの成長関連遺伝子が上昇する場合があるにもかかわらず観察された現象です。影響を受けた遺伝子群は上皮の特徴の維持や細胞外マトリックスの組織化に関与する役割が濃縮しており、これは細胞どうしの接着の強さや移動のしやすさに結びつく性質です。
こうした遺伝子変動と一致して、RBのない細胞は培養表面から剥がれやすく、人工的な“創傷”をより速く閉じる傾向があり、いずれも運動性の増加を示す兆候です。著者らが細胞周期にわたる振る舞いでRBが制御する遺伝子群を分類したところ、RBが実際に抑制ではなく活性化しているサブセットがあり、その活性化は近隣の境界での隔離を緩める能力に依存していることが明らかになりました。これはRBが単に増殖のブレーキとして働くだけでなく、正常な組織構造を維持する特定の遺伝子セットに対する正の調節因子としても機能することを示唆します。
がんにとっての意味
専門外の読者にとっての要点は、RBが細胞を守るのは不適切な時期に分裂を止めるだけでなく、DNAの折りたたみと配線の形を整えることによっても行っている、ということです。RBは境界要素からコヒーシンを取り除くのを促進することで特定の障壁を弱め、重要な制御スイッチが標的遺伝子に届くことを可能にします。RBを失うとこれらの境界が強まり、正常な細胞同定を維持するいくつかの遺伝子が沈黙し、細胞は剥がれやすく移動しやすくなります――これらは腫瘍の拡散や治療抵抗性を助長し得る性質です。ゲノムの3次元構造の設計者としてのRBという拡張された見方は、その喪失がしばしばより危険で治療困難ながんへの転機を示す理由を説明する手がかりになるかもしれません。
引用: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
キーワード: 網膜芽細胞腫タンパク質, クロマチンループ, コヒーシン, 3次元ゲノム構造, がん進行