Clear Sky Science · fr
La perte de RB module l’organisation de la chromatine en régulant les boucles dépendantes de cohesine et les interactions enhancers-promoteurs
Pourquoi le gestionnaire de l’emballage cellulaire compte
Chaque cellule de votre corps doit compacter environ deux mètres d’ADN dans un noyau plus petit qu’un grain de poussière. La façon dont cet ADN est replié — pas seulement les gènes qu’il contient — contribue à déterminer quels gènes sont activés ou réprimés. Cet article explore une protéine célèbre pour son rôle anticancéreux, RB, et révèle qu’elle fait bien plus que freiner la division cellulaire incontrôlée. RB participe aussi à l’organisation tridimensionnelle de l’ADN, ajustant finement quels gènes peuvent être atteints par les interrupteurs de contrôle à proximité. Comprendre ce rôle caché donne de nouveaux éléments pour expliquer pourquoi les cancers deviennent agressifs lorsqu’ils perdent RB.
Un gardien avec un travail caché
RB (abréviation de protéine du rétinoblastome) est surtout connue comme un frein du cycle cellulaire. Elle maintient normalement silencieux un ensemble de gènes favorisant la croissance jusqu’à ce que la cellule soit prête à se diviser. De nombreuses tumeurs désactivent RB, ce qui permet aux cellules de se multiplier de façon incontrôlée. Pourtant, les cancers dépourvus de RB présentent aussi des changements déroutants — comme une invasivité accrue et la capacité à changer de type cellulaire — qui ne s’expliquent pas uniquement par la perte de ce frein du cycle. Des travaux antérieurs suggéraient que RB se lie non seulement aux promoteurs de gènes mais aussi à des régions de contrôle lointaines (enhancers) et à des sites « isolateurs » qui marquent les frontières entre quartiers d’activité de l’ADN. Cela a soulevé l’hypothèse que RB pourrait aussi agir comme un organisateur du repliement du génome.
Boucles, frontières et gestion du trafic
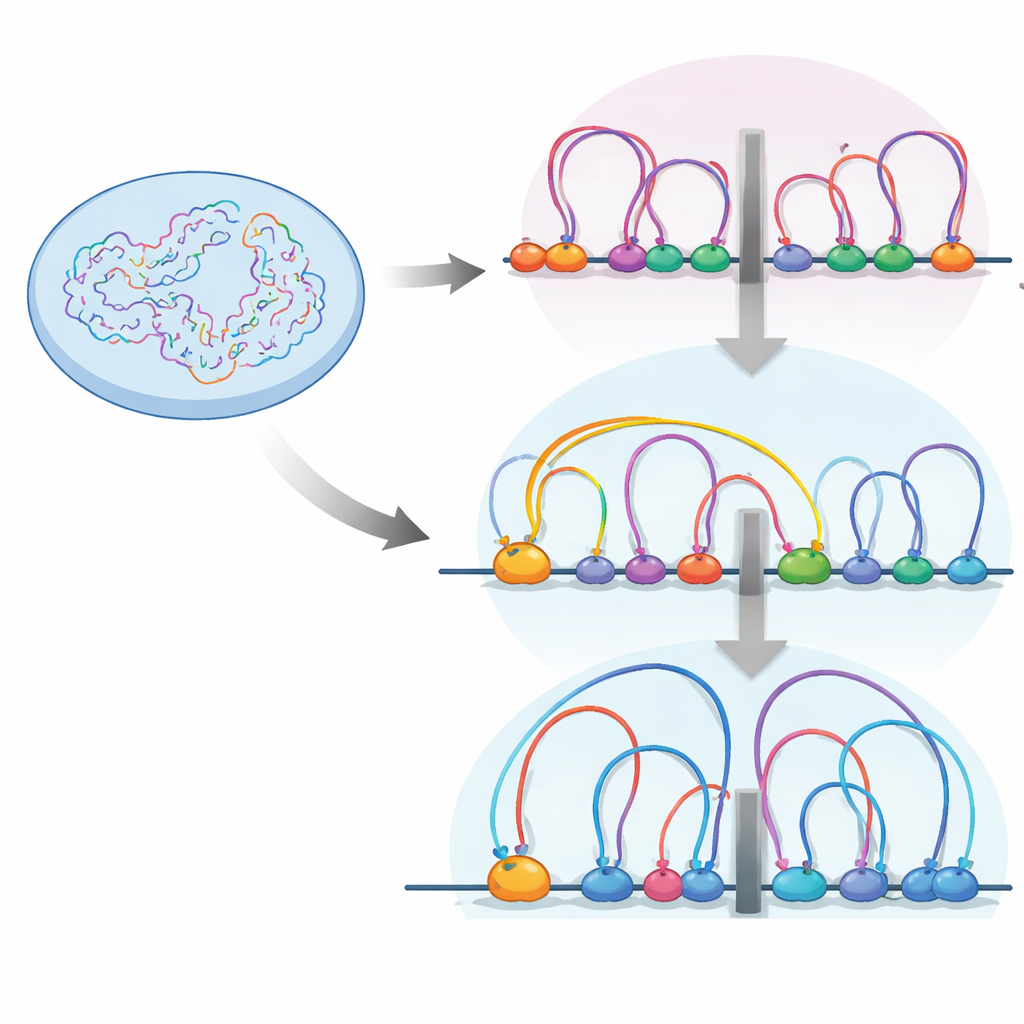
Dans le noyau, le fibre d’ADN est repliée en boucles par une machinerie protéique appelée cohesine. Ces boucles contribuent à regrouper gènes et éléments de contrôle en unités appelées domaines d’association topologique, ou TAD — essentiellement des quartiers au sein desquels gènes et interrupteurs interagissent plus librement. Les frontières entre ces quartiers sont souvent marquées par une protéine isolatrice appelée CTCF, où la cohesine a tendance à faire une pause. Les auteurs ont utilisé une cartographie des contacts chromosomiques à haute résolution (Micro-C) et un ensemble d’autres outils génomiques pour observer comment l’activation ou la perte de RB remodèle ce paysage de boucles dans des cellules rétiniennes humaines.
Ils ont constaté qu’en l’absence de RB, le nombre et la taille moyenne des boucles d’ADN augmentent, et que les frontières des TAD deviennent plus fortes. Parallèlement, RB et cohesine co-localisent à de nombreuses régions accessibles du génome, en particulier aux isolateurs. Un cartographie détaillée de la localisation de la cohesine selon les phases du cycle cellulaire a montré que RB est nécessaire pour aider à évacuer la cohesine de ces sites isolateurs pendant la mitose, la phase où les chromosomes se condensent puis se ré-ouvrent. Sans RB, la cohesine s’accumule aux isolateurs, renforçant les frontières et modifiant la façon dont les quartiers d’ADN sont isolés les uns des autres.
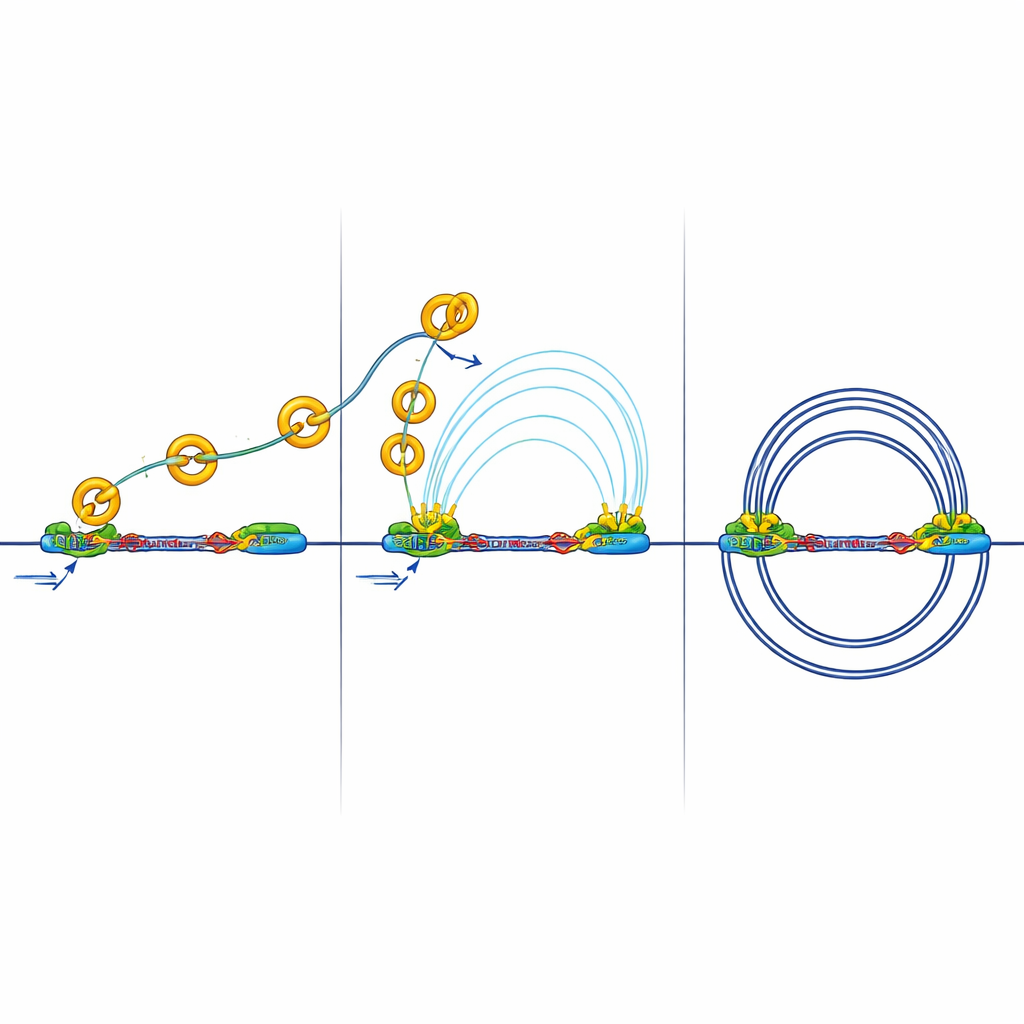
Quand l’isolation bloque les conversations géniques
Des frontières renforcées ont des conséquences. Les isolateurs peuvent bloquer les « appels longue distance » entre enhancers et promoteurs nécessaires à l’activation des gènes. L’équipe a mesuré les contacts physiques entre régions actives de l’ADN marquées par une modification chimique appelée H3K27ac. Dans les cellules dépourvues de RB, ils ont observé moins de contacts et des contacts plus faibles entre enhancers et promoteurs, même si de nombreuses marques d’activation étaient encore présentes. Autrement dit, les interrupteurs étaient activés, mais leurs signaux peinaient à franchir les frontières renforcées. Des expériences complémentaires ont montré une réduction du recrutement d’un complexe médiateur clé qui aide normalement les enhancers à dialoguer avec les promoteurs, soutenant l’idée que c’est le câblage 3D, plutôt que les marques d’activation de base, qui est perturbé.
Du repliement de l’ADN au comportement cellulaire
Pour relier ces changements architecturaux à des gènes et phénotypes concrets, les auteurs se sont concentrés sur des gènes dont les promoteurs ne sont pas directement liés par RB ou ses partenaires habituels, mais qui se trouvent juste au-delà d’un isolateur où les niveaux de cohesine changent lorsque RB est perdu. Pour les gènes voisins d’isolateurs ayant gagné en cohesine (et donc en isolation), l’expression a tendance à diminuer dans les cellules déficientes en RB, même si RB augmente souvent de façon globale de nombreux gènes liés à la croissance lorsqu’il est supprimé. Ces gènes affectés étaient enrichis pour des fonctions liées au maintien des caractéristiques épithéliales et à l’organisation de la matrice extracellulaire — propriétés associées à l’adhérence cellulaire et à la mobilité.
Conformément à ces changements d’expression, les cellules dépourvues de RB se détachaient plus facilement de la surface de culture et refermaient des « blessures » artificielles plus rapidement, deux signes d’une mobilité accrue. Lorsque les auteurs ont regroupé les gènes contrôlés par RB selon leur comportement au cours du cycle cellulaire, ils ont identifié un sous-ensemble que RB active en réalité, plutôt que de réprimer, d’une manière dépendante de sa capacité à assouplir l’isolation aux frontières voisines. Cela suggère que RB n’agit pas seulement comme un frein de la croissance ; elle sert aussi de régulateur positif pour des ensembles de gènes spécifiques qui contribuent à préserver l’architecture tissulaire normale.
Ce que cela signifie pour le cancer
Pour les non-spécialistes, le message clé est que RB protège les cellules non seulement en les empêchant de se diviser au mauvais moment, mais aussi en modelant la façon dont leur ADN est replié et câblé. En favorisant le retrait de la cohesine des éléments frontières, RB affaiblit certaines barrières et permet à des interrupteurs importants d’atteindre leurs gènes cibles. Lorsque RB est perdu, ces frontières deviennent trop fortes, certains gènes qui maintiennent l’identité cellulaire normale sont silencieux, et les cellules deviennent plus enclines à se détacher et à migrer — des caractéristiques qui peuvent alimenter la dissémination tumorale et la résistance au traitement. Cette vision élargie de RB comme architecte de la structure 3D du génome peut aider à expliquer pourquoi sa perte marque si souvent un tournant vers des cancers plus dangereux et difficiles à traiter.
Citation: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Mots-clés: protéine rétinoblastome, boucles de chromatine, cohesine, organisation 3D du génome, progression du cancer