Clear Sky Science · de
Der Verlust von RB verändert die Chromatinorganisation durch Regulierung cohesinabhängiger Schleifen und Enhancer-Promoter-Interaktionen
Warum der Verpackungsmanager der Zelle wichtig ist
Jede Zelle in Ihrem Körper muss etwa zwei Meter DNA in einen Zellkern quetschen, der kleiner ist als ein Staubkorn. Wie diese DNA gefaltet ist – nicht nur welche Gene sie trägt – beeinflusst, welche Gene ein- oder ausgeschaltet werden. Diese Arbeit untersucht ein bekanntes krebsbekämpfendes Protein namens RB und zeigt, dass es weit mehr tut als die unkontrollierte Zellteilung zu stoppen. RB hilft auch, die dreidimensionale Faltung der DNA zu steuern und feinabzustimmen, welche Gene von nahegelegenen Kontrollschaltern erreicht werden können. Das Verständnis dieser verborgenen Rolle liefert neue Hinweise darauf, wie Tumoren aggressiv werden können, wenn sie RB verlieren.
Ein Wächter mit versteckter Aufgabe
RB (kurz für Retinoblastom‑Protein) ist vor allem als Bremse des Zellzyklus bekannt. Normalerweise hält es eine Gruppe wachstumsfördernder Gene ruhig, bis die Zelle bereit ist, sich zu teilen. Viele Tumoren deaktivieren RB, wodurch sich Zellen unkontrolliert vermehren können. RB‑defiziente Krebserkrankungen zeigen jedoch auch rätselhafte Veränderungen – etwa erhöhte Invasivität und die Fähigkeit, den Zelltyp zu wechseln –, die sich nicht allein durch den Verlust dieser Zellzyklus‑Bremse erklären lassen. Frühere Arbeiten deuteten darauf hin, dass RB nicht nur an Genstarter (Promotoren) bindet, sondern auch an entfernte Kontrollregionen (Enhancer) und spezielle "Isolator"‑Stellen, die die Grenzen zwischen Aktivitätsnachbarschaften der DNA markieren. Das legte die Vermutung nahe, dass RB auch als Organisator der Genomfaltung wirken könnte.
Schleifen, Grenzen und Verkehrsregelung
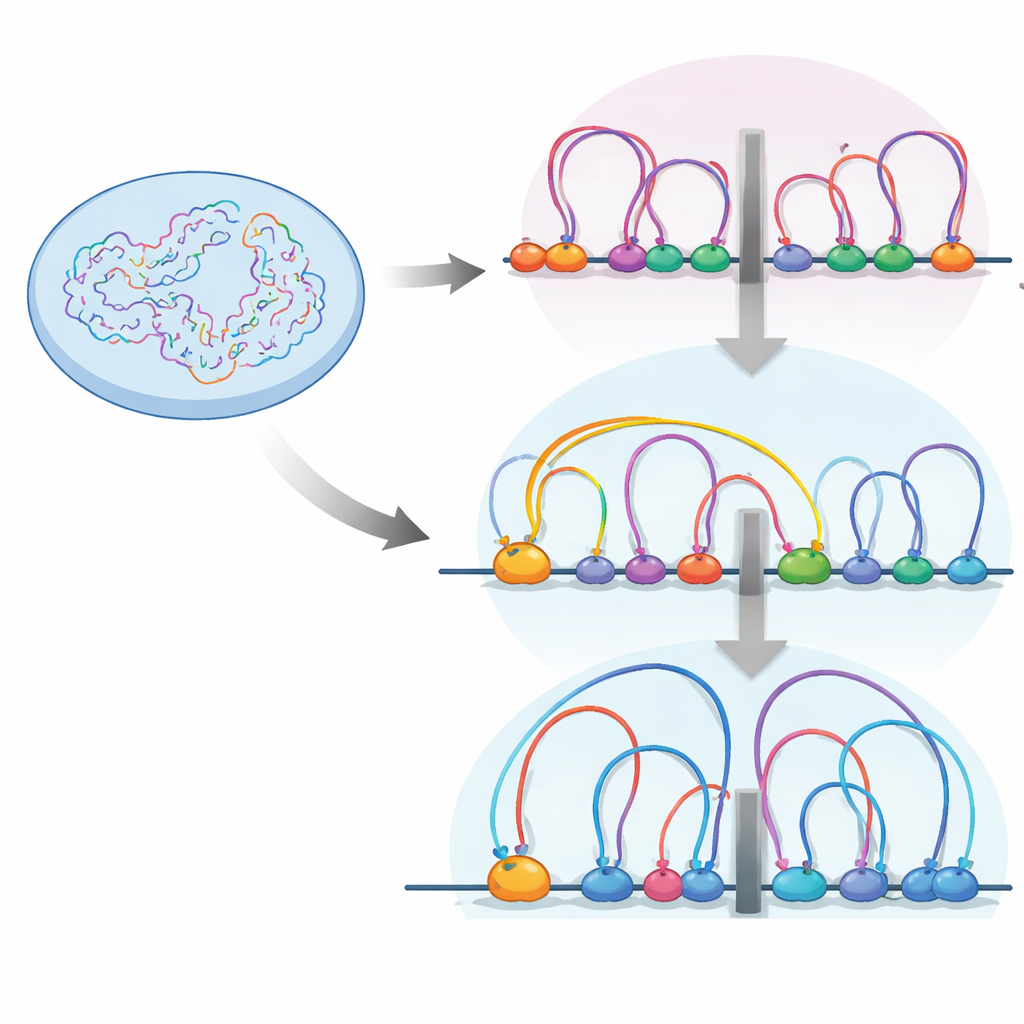
Im Zellkern wird der DNA‑Faden durch eine Proteinfunktion namens Cohesin in Schleifen gefaltet. Diese Schleifen helfen, Gene und ihre Kontrollelemente in Einheiten zusammenzufassen, die als topologisch assoziierte Domänen oder TADs bezeichnet werden – im Wesentlichen Nachbarschaften, innerhalb derer Gene und Schalter freier interagieren. Grenzen zwischen diesen Nachbarschaften sind oft durch ein Isolatorprotein namens CTCF markiert, an dem Cohesin häufig pausiert. Die Autoren verwendeten hochauflösendes Chromosomenkontaktmapping (Micro‑C) und eine Reihe weiterer genomischer Werkzeuge, um zu untersuchen, wie das Ein‑ oder Ausschalten von RB diese Loop‑Landschaft in menschlichen Netzhautzellen umgestaltet.
Sie fanden heraus, dass in Abwesenheit von RB sowohl die Anzahl als auch die durchschnittliche Größe der DNA‑Schleifen zunimmt und TAD‑Grenzen stärker werden. Gleichzeitig liegen RB und Cohesin gemeinsam an vielen zugänglichen Regionen im gesamten Genom, insbesondere an Isolatoren. Detaillierte Kartierungen von Cohesin‑Positionen während verschiedener Zellzyklusphasen zeigten, dass RB notwendig ist, um Cohesin während der Mitose – der Phase, in der sich Chromosomen verdichten und wieder öffnen – von diesen Isolatorstellen zu entfernen. Ohne RB häuft sich Cohesin an Isolatoren an, was die Grenzen verstärkt und die Art und Weise verändert, wie DNA‑Nachbarschaften voneinander abgeschirmt werden.
Wenn Isolierung Genkonversationen blockiert
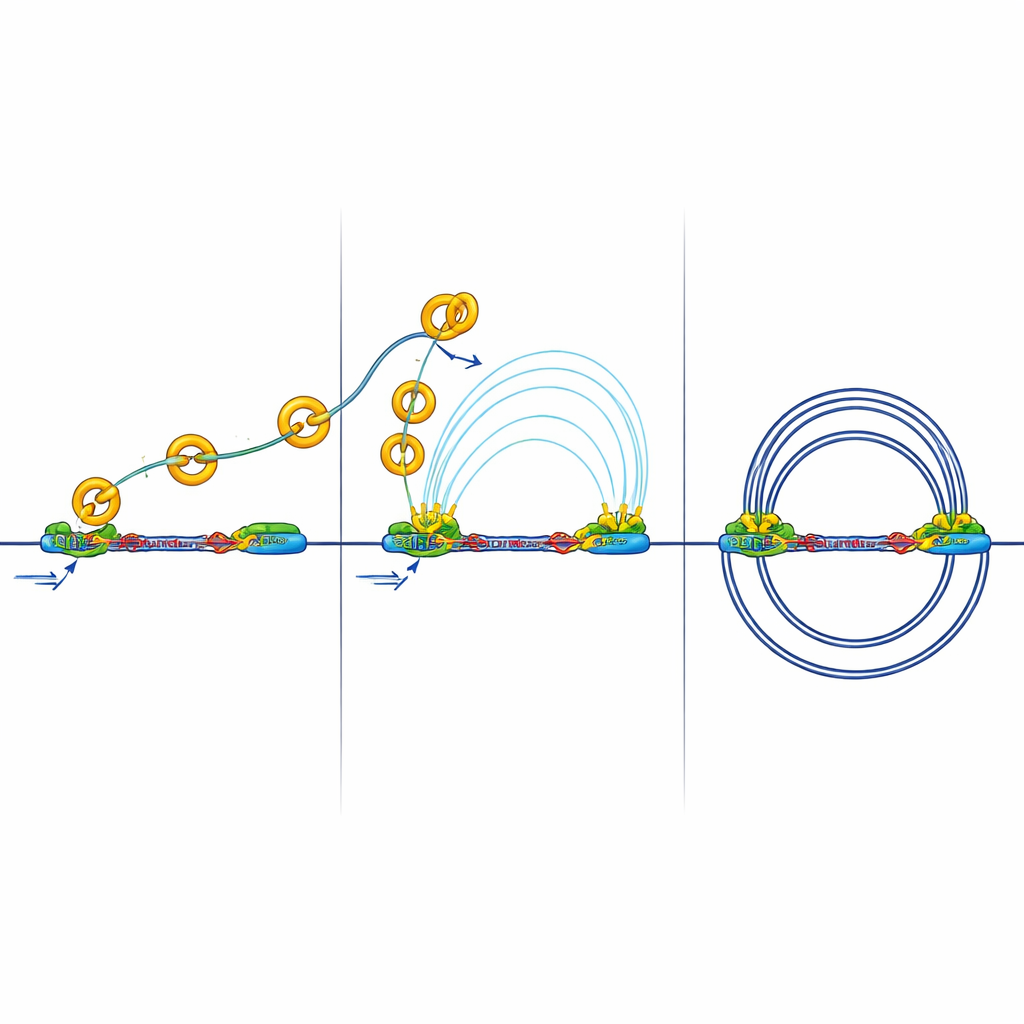
Stärkere Grenzen haben Konsequenzen. Isolatoren können die "Fernanrufe" zwischen Enhancern und Promotoren blockieren, die nötig sind, um Gene zu aktivieren. Das Team maß physische Kontakte zwischen aktiven DNA‑Regionen, die durch ein chemisches Markenzeichen namens H3K27ac gekennzeichnet sind. In Zellen ohne RB beobachteten sie weniger und schwächere Kontakte zwischen Enhancern und Promotoren, obwohl viele Aktivierungsmarken weiterhin vorhanden waren. Mit anderen Worten: Die Schalter waren an, aber ihre Signale gelangten nur schwer über die verstärkten Grenzen. Zusätzliche Experimente zeigten eine verringerte Rekrutierung eines wichtigen Mediator‑Komplexes, der normalerweise hilft, dass Enhancer mit Promotoren kommunizieren, und stützen die Idee, dass die 3D‑Verdrahtung – nicht die grundlegenden Ein/Aus‑Marken – gestört wird.
Von der DNA‑Faltung zum Zellverhalten
Um diese Architekturänderungen mit konkreten Genen und Merkmalen zu verbinden, konzentrierten sich die Autoren auf Gene, deren Promotoren nicht direkt von RB oder seinen üblichen Partnerfaktoren gebunden werden, die aber direkt hinter einem Isolator liegen, an dem sich die Cohesin‑Menge ändert, wenn RB verloren geht. Für Gene neben Isolatoren, die Cohesin gewonnen haben (und somit stärker isoliert wurden), sank die Expression in RB‑defizienten Zellen tendenziell, obwohl RB‑Entfernung oft global viele wachstumsbezogene Gene anhebt. Diese betroffenen Gene waren gehäuft für Funktionen in der Erhaltung epithelialer Merkmale und der Organisation der Umgebungsmatrix der Zelle zuständig – Eigenschaften, die damit zusammenhängen, wie fest Zellen zusammenhalten und wie leicht sie sich bewegen.
Im Einklang mit diesen Genveränderungen lösten sich RB‑freie Zellen leichter von der Kulturoberfläche und schlossen künstliche "Wunden" schneller, beides Hinweise auf erhöhte Beweglichkeit. Als die Autoren RB‑kontrollierte Gene nach ihrem Verhalten über den Zellzyklus gruppierten, identifizierten sie eine Untergruppe, die RB tatsächlich aktiviert – nicht repressed –, und zwar auf eine Weise, die von seiner Fähigkeit abhängt, die Isolierung an benachbarten Grenzen zu lockern. Das legt nahe, dass RB nicht nur als Wachstumsbremse wirkt, sondern auch als positiver Regulator spezifischer Genmengen dient, die helfen, die normale Gewebe‑Architektur zu erhalten.
Was das für Krebs bedeutet
Für Nichtfachleute lautet die Kernbotschaft: RB schützt Zellen nicht nur, indem es sie daran hindert, zur falschen Zeit zu teilen, sondern auch, indem es die Faltung und Vernetzung ihrer DNA mitgestaltet. Indem RB die Entfernung von Cohesin an Grenzelementen fördert, schwächt es bestimmte Barrieren und erlaubt wichtigen Kontrollschaltern, ihre Zielgene zu erreichen. Geht RB verloren, werden diese Grenzen zu stark, einige Gene, die die normale Zellidentität erhalten, werden stillgelegt, und Zellen neigen eher dazu, sich zu lösen und zu migrieren – Eigenschaften, die Tumorstreuung und Therapie‑Resistenz begünstigen können. Diese erweiterte Sicht auf RB als Architekt der 3D‑Genomstruktur kann helfen zu erklären, warum sein Verlust so oft einen Wendepunkt in Richtung gefährlicherer, schwer behandelbarer Krebserkrankungen markiert.
Zitation: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Schlüsselwörter: Retinoblastom-Protein, Chromatin-Schleifen, Cohesin, 3D-Genomorganisation, Krebsprogression