Clear Sky Science · nl
Verlies van RB moduleert chromatineorganisatie door cohesine-afhankelijke lussen en enhancer-promotorinteracties te reguleren
Waarom de verpakking van de cel ertoe doet
Elke cel in je lichaam moet ongeveer twee meter DNA in een kern proppen die kleiner is dan een stofdeeltje. Hoe dat DNA gevouwen is — niet alleen welke genen het bevat — helpt bepalen welke genen aan- of uitgezet worden. Dit artikel onderzoekt een bekend kankerinhiberend eiwit genaamd RB en laat zien dat het veel meer doet dan alleen het afremmen van uit de hand lopende celdeling. RB helpt ook bij het beheer van de driedimensionale vouwing van DNA, waardoor het bereik van nabijgelegen regelknoppen naar genen wordt fijngeregeld. Inzicht in deze verborgen rol biedt nieuwe aanwijzingen over hoe kankers agressiever worden wanneer ze RB verliezen.
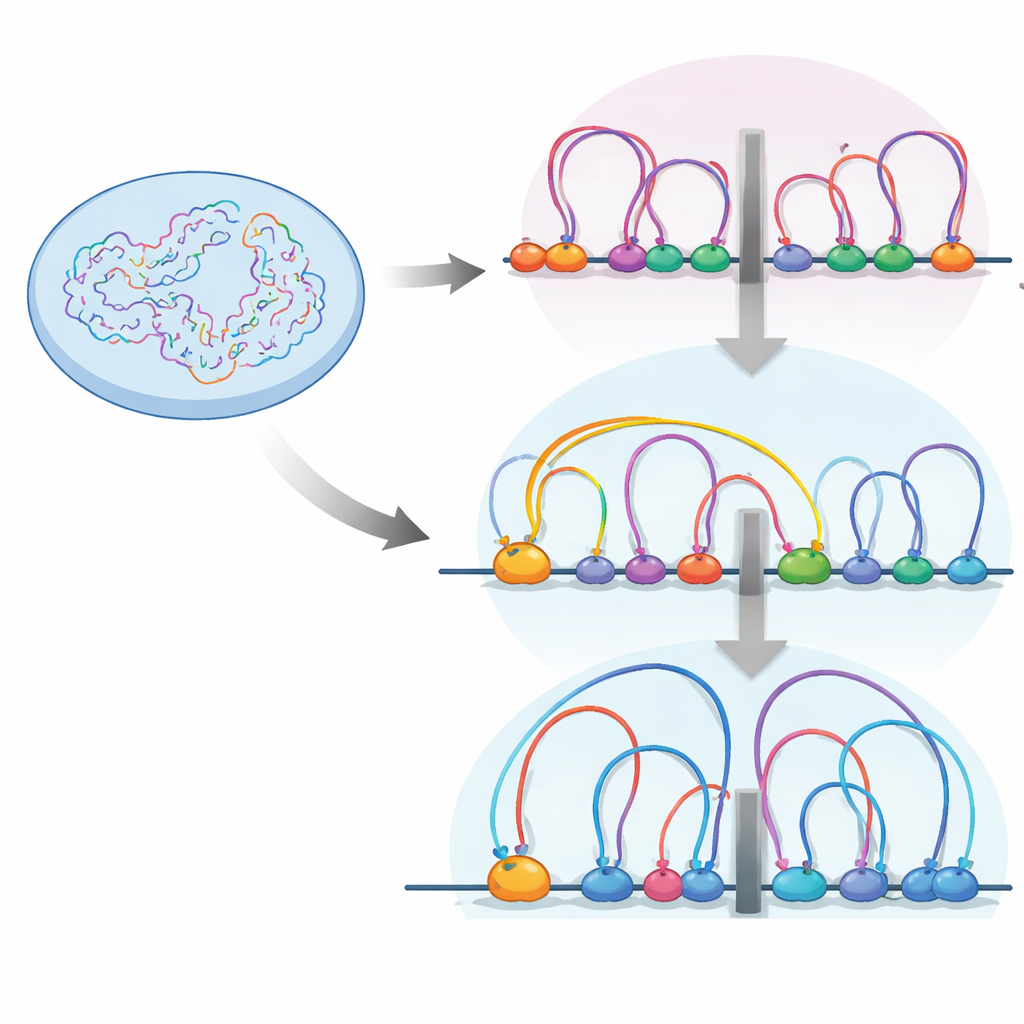
Een beschermer met een verborgen taak
RB (afkorting van retinoblastoom-eiwit) is vooral bekend als een rem op de celcyclus. Het houdt normaal gesproken een reeks groeigerelateerde genen stil totdat de cel klaar is om te delen. Veel tumoren schakelen RB uit, wat cellen toestaat zich ongecontroleerd te vermenigvuldigen. RB-deficiënte kankers vertonen echter ook raadselachtige veranderingen — zoals toegenomen invasiviteit en het vermogen van cellen om van type te wisselen — die niet alleen door het verlies van deze celcyclusrem verklaard kunnen worden. Eerder werk suggereerde dat RB niet alleen aan genstarters (promoters) bindt, maar ook aan verre regelregio’s (enhancers) en speciale “isolator”-plaatsen die de grenzen tussen DNA-buurten markeren. Dit riep de mogelijkheid op dat RB ook fungeert als organisator van de vouwing van het genoom.
Lussen, grenzen en verkeersregeling
Binnen de kern wordt de DNA-draad gevouwen in lussen door een eiwitmachine genaamd cohesine. Deze lussen helpen genen en hun regelende elementen te groeperen in eenheden die topologisch associërende domeinen of TADs worden genoemd — in wezen buurten waarin genen en schakelaars vrijer met elkaar kunnen omgaan. Grenzen tussen deze buurten worden vaak gemarkeerd door een isolator-eiwit genaamd CTCF, waar cohesine de neiging heeft te pauzeren. De auteurs gebruikten hoogresolutienetwerkanalyse van chromosoomcontacten (Micro-C) en een reeks andere genomische technieken om te zien hoe het aan- of uitzetten van RB dit luslandschap in menselijke retinale cellen hervormt.
Zij vonden dat wanneer RB ontbreekt, het aantal en de gemiddelde grootte van DNA-lussen toenemen en TAD-grenzen sterker worden. Tegelijkertijd zitten RB en cohesine samen op veel toegankelijke regio’s in het genoom, vooral bij isolatoren. Gedetailleerde kaarten van cohesine-locaties tijdens verschillende stadia van de celcyclus toonden aan dat RB nodig is om cohesine van deze isolatorplaatsen te helpen verwijderen tijdens mitose, de fase waarin chromosomen condenseren en daarna weer openen. Zonder RB hoopt cohesine zich op bij isolatoren, wat grenzen versterkt en verandert hoe DNA-buurten van elkaar geïsoleerd zijn.
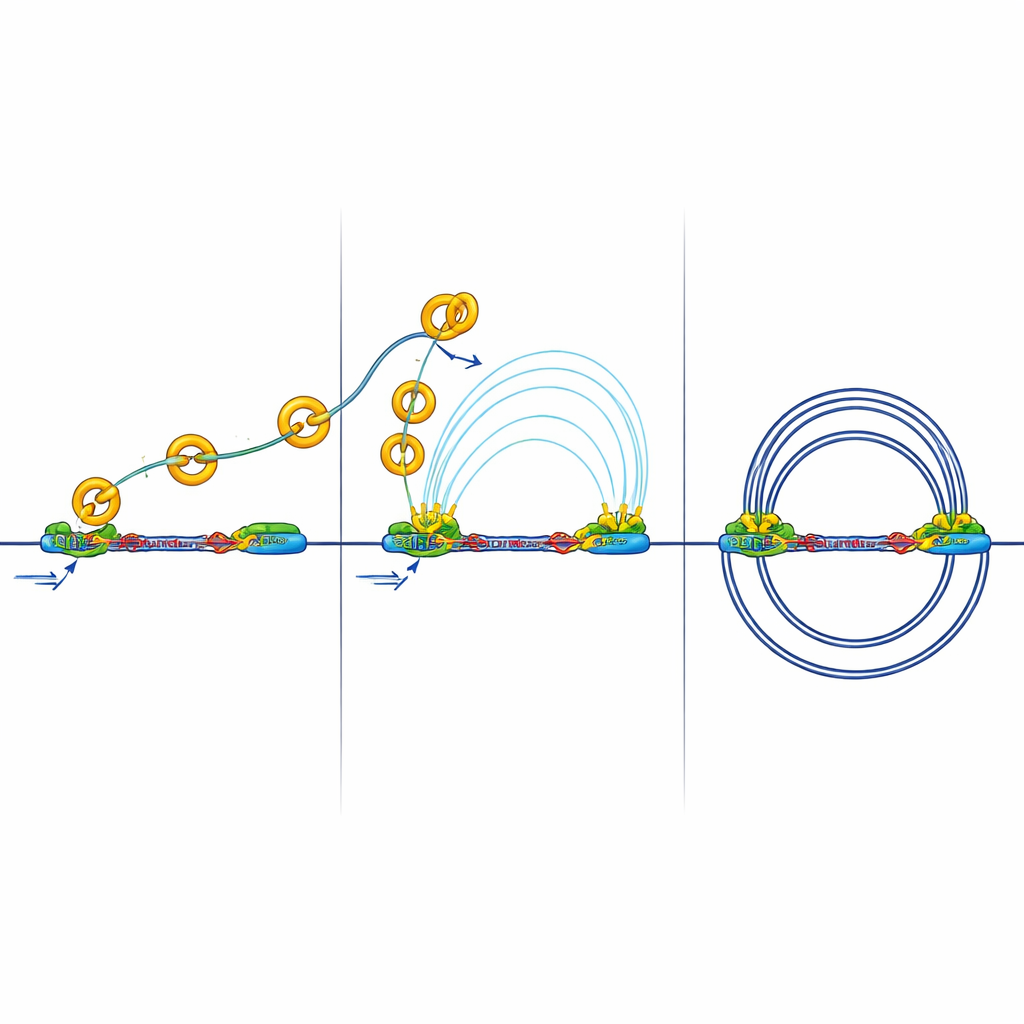
Wanneer isolatie genconversaties blokkeert
Sterkere grenzen hebben gevolgen. Isolatoren kunnen de “langeafstandsgesprekken” tussen enhancers en promoters blokkeren die nodig zijn om genen te activeren. Het team mat fysieke contacten tussen actieve delen van DNA die gemarkeerd zijn door een chemische markering genaamd H3K27ac. In cellen zonder RB zagen ze minder en zwakkere contacten tussen enhancers en promoters, ondanks dat veel activeringsmerken nog aanwezig waren. Met andere woorden: de schakelaars stonden aan, maar hun signalen hadden moeite de versterkte grenzen te oversteken. Aanvullende experimenten toonden verminderde rekrutering van een sleutelmolecuulcomplex dat normaal helpt bij de communicatie tussen enhancers en promoters, wat het idee ondersteunt dat de 3D-bekabeling, eerder dan de basale aan/uit-markeringen, verstoord is.
Van DNA-vouwing naar celgedrag
Om deze architecturale veranderingen te koppelen aan echte genen en eigenschappen, richtten de auteurs zich op genen waarvan de promoters niet direct door RB of zijn gebruikelijke partnerfactoren worden gebonden, maar die net voorbij een isolator zitten waar de cohesine-niveaus veranderen wanneer RB verloren gaat. Voor genen naast isolatoren die cohesine verwierven (en daardoor sterkere isolatie kregen), daalde de expressie in de RB-deficiënte cellen, ook al verhoogt het verlies van RB vaak wereldwijd veel groeigerelateerde genen. Deze aangedane genen waren verrijkt voor functies in het behouden van epitheliale kenmerken en in het organiseren van de extracellulaire matrix — eigenschappen die verband houden met hoe stevig cellen aan elkaar blijven plakken en hoe gemakkelijk ze zich verplaatsen.
Consistent met deze genveranderingen lieten RB-loze cellen zich makkelijker losmaken van het kweekoppervlak en sloten ze kunstmatige “wonden” sneller, beide tekenen van grotere beweeglijkheid. Toen de auteurs RB-gerelateerde genen groepeerden naar gedrag door de celcyclus, identificeerden ze een subset die RB feitelijk activeert in plaats van onderdrukt, op een manier die afhankelijk is van zijn vermogen om de isolatie bij nabijgelegen grenzen te versoepelen. Dit suggereert dat RB niet alleen als rem op groei fungeert; het dient ook als een positieve regulator voor specifieke genen die helpen normale weefselarchitectuur te behouden.
Wat dit betekent voor kanker
Voor niet-specialisten is de kernboodschap dat RB cellen niet alleen beschermt door te voorkomen dat ze op het verkeerde moment delen, maar ook door te bepalen hoe hun DNA gevouwen en bekabeld is. Door de verwijdering van cohesine van grens-elementen te bevorderen, verzwakt RB bepaalde barrières en laat het belangrijke regelknoppen hun doelgenen bereiken. Wanneer RB verloren gaat, worden deze grenzen te sterk, worden sommige genen die de normale celidentiteit behouden stilgelegd, en raken cellen vatbaarder om los te laten en te migreren — eigenschappen die tumoruitzaai en behandelingsresistentie kunnen bevorderen. Deze verbrede visie op RB als architect van de 3D-structuur van het genoom kan helpen verklaren waarom het verlies ervan zo vaak een keerpunt markeert richting gevaarlijkere, moeilijker te behandelen kankers.
Bronvermelding: Lee, H., Gkotinakou, IM., McGrath, C.G. et al. RB loss modulates chromatin organization by regulating cohesin-dependent loops and enhancer-promoter interactions. Nat Commun 17, 3696 (2026). https://doi.org/10.1038/s41467-026-71655-x
Trefwoorden: retinoblastoom-eiwit, chromatine-lussen, cohesine, 3D-genoomorganisatie, kankerprogressie