Clear Sky Science · zh
构建一种体积紧凑且高保真性的金黄色葡萄球菌 Cas9 变体,拓宽靶向范围并揭示其激活机制
用于修复缺陷基因的更小“剪刀”
像 CRISPR-Cas9 这样的基因编辑工具为遗传病的治疗带来了希望,但最常用的版本体积庞大,且可能误切错误的 DNA 片段。本研究介绍了一种基于金黄色葡萄球菌(Staphylococcus aureus)酶的紧凑且高度精确的 DNA“剪刀”,其经重新设计后能覆盖基因组中更多位点,同时保持切割的精确性。由于它足够小能装入常用的基因治疗病毒载体,并且在细胞和小鼠中均表现良好,可能使更安全的 DNA 修复更接近临床应用。
为什么体积和精确性很重要
基因组编辑的原始主力 SpCas9 来源于化脓性链球菌(Streptococcus pyogenes)。它功能强大但体积较大,这使得将其包装进广泛用于基因递送的腺相关病毒(AAV)载体变得困难。它还只识别形式为 NGG 的短 DNA 标签(PAM)。这些限制使许多致病突变无法触及。其较小的同源酶 SaCas9(来源于金黄色葡萄球菌)可以舒适地装入 AAV 并高效切割 DNA,但它要求更长更罕见的 PAM 序列,从而大幅减少可编辑位点。为放宽这些 PAM 限制而对多种 Cas9 版本进行的改造常常带来权衡:可靶向位点增多,但脱靶损伤也随之增加。
工程化出更广泛、更安全的基因编辑器
在掌握 SaCas9 的详细结构基础上,作者系统地替换了与 PAM 序列发生直接、碱基特异性接触的氨基酸残基。随后引入了新的带正电残基,以更普遍地抓握 DNA 骨架。这产生了名为 SaCas9-NNG 的变体,它识别简单的 NNG PAM,而不是更严格的 NNGRRT 模式,从而大幅增加了潜在编辑位点的数量。进一步的微调移除了在某些序列上削弱活性的微妙冲突。在体外反应和人类细胞中,SaCas9-NNG 在一系列 NNG 位点上高效切割或改写 DNA,尤其是以 C 或 T 结尾的位点——原始酶无法触及的那些。在许多靶点上,它的表现可与或优于其他“PAM 放宽”编辑器,如 SpRY、SpG 和 iGeoCas9。
提升编辑的可信度
扩大 Cas9 的切割范围提出了一个关键问题:它还能避免切错地方吗?为了解决这一点,研究团队通过削弱某些有助于蛋白容忍导向 RNA 与 DNA 间错配的接触,工程化出一种高保真版本。在稳定 RNA–DNA 双螺旋远端的区域引入的两个关键取代,使酶对错配的容忍性降低,尤其是那些远离 PAM、常导致脱靶切割的错配。该变体被称为 eSaCas9-NNG,在正确靶点上保持强活性,却显著减少了对不完全匹配位点的切割。在人类细胞中的比较显示,它匹配甚至优于已建立的高保真 SaCas9,并且比其低保真同类产生更少的误切。
从体外实验到治疗出血性疾病
为了测试这个紧凑编辑器在生物体内是否可行,研究者将 SaCas9-NNG 及其导向 RNA 打包进单一的 AAV8 载体,并注射入小鼠。针对与 B 型血友病相关的人类凝血因子 9(F9)基因,他们在肝脏中观察到了对 NNG 位点的高效小片段插入/缺失(indel),包括标准 SaCas9 无法触及的位点。他们还构建了无需断裂双链而替换单个碱基的碱基编辑版本。在携带人源 B 型血友病突变的小鼠模型中,由 SaCas9-NNG 构建的腺嘌呤碱基编辑器成功修正了既有经典 PAM 下的致病突变和先前无法到达的位点。接受治疗的动物其血液中的凝血因子活性显著提高,表明功能得到恢复。
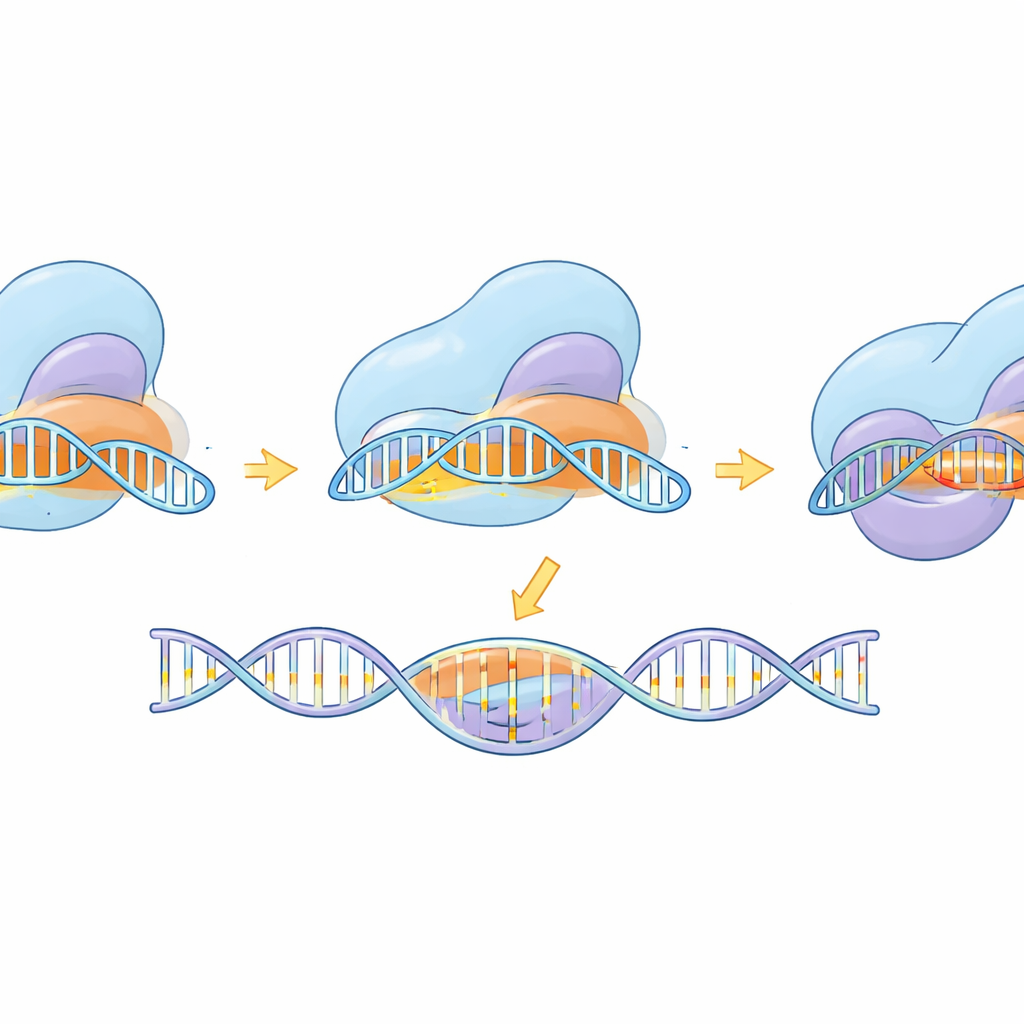
实时观察分子机器的工作过程
除了工具构建之外,研究通过冷冻电子显微镜对 eSaCas9-NNG 在其工作周期中的多个快照进行了捕捉——包括结合 DNA 之前、检测潜在位点时、与靶序列部分配对期间以及处于完全激活、准备切割的状态。这些结构揭示了酶如何首先锁定兼容的 NNG 标签,然后逐步形成 RNA–DNA 束状杂交螺旋。只有当该螺旋足够长且碱基配对正确时,内部结构域才会摆动到位并将两条 DNA 链上的切割中心对齐。那些改善特异性的工程化突变被观察到会破坏与在螺旋远端发生变形或错配的 DNA 的结合,使酶更倾向于释放而非错误切割。与形态更为灵活的 SpCas9 相关变体的比较表明,尽管构象不同,两者遵循相似的逻辑:要触发最终的切割动作,必须达到完整且准确的碱基配对。
这对未来基因治疗意味着什么
对非专业读者而言,核心信息是:作者们设计出了一种更小、更通用且更谨慎的基因编辑工具。eSaCas9-NNG 能靶向比原始 SaCas9 多得多的基因组区域,同时保持高精度,并且体积足够小可装入单一 AAV 包装——这是许多体内疗法的关键要求。它在 B 型血友病小鼠模型中修复凝血缺陷的成功,加上对其工作机制及避免错误的详细结构学见解,使该酶成为下一代治疗的有希望骨干,并为未来如更精确的碱基和首端(prime)编辑器的改进提供了基础。
引用: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
关键词: CRISPR, 基因治疗, Cas9, 碱基编辑, B 型血友病