Clear Sky Science · nl
Ontwikkeling van een compacte, hoog-fidelity Staphylococcus aureus Cas9-variant met een bredere richtingsbereik en mechanistische inzichten in de activering
Kleinere scharen om foutieve genen te repareren
Geredigeermiddelen zoals CRISPR-Cas9 beloven behandelingen voor erfelijke aandoeningen, maar de meest gebruikte varianten zijn log en kunnen per ongeluk het verkeerde DNA-fragment doorsnijden. Deze studie introduceert een compacte, zeer nauwkeurige DNA-“schaar” gebaseerd op een enzym van Staphylococcus aureus, herontworpen om veel meer locaties in het genoom te bereiken terwijl het toch precies knipt. Omdat het klein genoeg is om in een veelgebruikt virus voor gentherapie te passen en goed werkt zowel in cellen als in muizen, zou het veiliger DNA-herstel dichterbij klinische toepassing kunnen brengen.
Waarom grootte en nauwkeurigheid ertoe doen
Het oorspronkelijke werkpaard van genoombewerking, SpCas9, komt van Streptococcus pyogenes. Het is krachtig maar groot, wat het moeilijk maakt om in adeno-geassocieerde virus (AAV)-vectoren te verpakken die veel worden gebruikt voor levering van gentherapieën. Het herkent ook alleen korte DNA-tags, PAMs genoemd, van de vorm NGG. Deze beperkingen laten veel ziekteveroorzakende mutaties buiten bereik. Een kleinere verwant, SaCas9 van Staphylococcus aureus, past comfortabel in AAV en knipt DNA efficiënt, maar vereist een langere en zeldzamere PAM-sequentie, waardoor het aantal bewerkbare sites sterk wordt beperkt. Pogingen om deze PAM-regels in verschillende Cas9-versies te versoepelen leidden vaak tot een compromis: meer doelen maar ook meer off-target beschadiging.
Een bredere, veiligere genbewerker ontwerpen
Met gedetailleerde structurele kennis van SaCas9 vervingen de auteurs systematisch aminozuren die directe, letterspecifieke contacten met de PAM-sequentie maken. Ze introduceerden vervolgens nieuwe positief geladen residuen die de DNA-ruggengraat algemener vastgrijpen. Dit leverde een variant op met de naam SaCas9-NNG, die eenvoudige NNG-PAMs herkent in plaats van het striktere NNGRRT-patroon, waardoor het aantal potentiële bewerkingslocaties sterk toenam. Verdere verfijning verwijderde een subtiele botsing die de activiteit bij sommige sequenties zwakte. In reageerbuizen en menselijke cellen knipte of herschreef SaCas9-NNG efficiënt DNA op een breed paneel van NNG-sites, vooral die eindigend op C of T die het oorspronkelijke enzym niet kon bereiken. Over veel doelen heen evenaarde of overtrof de prestatie andere “PAM-verslapte” editors zoals SpRY, SpG en iGeoCas9.
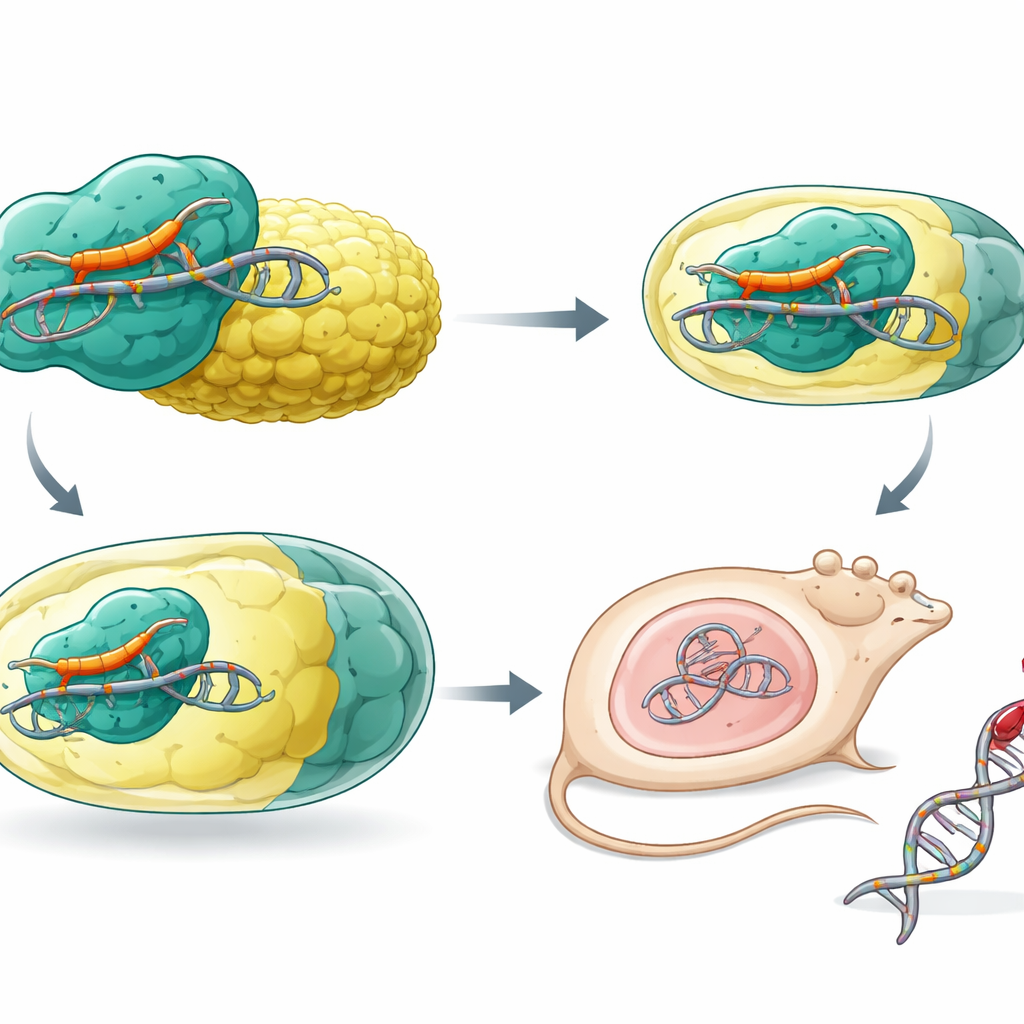
De bewerkingen betrouwbaarder maken
Het uitbreiden van de plekken waar Cas9 kan knippen roept een cruciale vraag op: kan het nog steeds de verkeerde plaatsen vermijden? Om dit aan te pakken ontwikkelde het team een high-fidelity versie door bepaalde contacten te verzwakken die het eiwit helpen mismatch-tolerantie tussen zijn gids-RNA en het DNA te permissiveren. Twee sleutelvervangingen in een regio die het verre uiteinde van de RNA–DNA-helix stabiliseert, maakten het enzym minder toegeeflijk voor mismatches, in het bijzonder die ver van de PAM, die vaak bron zijn van off-target knippen. Deze variant, eSaCas9-NNG genoemd, behield sterke activiteit op correcte doelen maar verminderde het knippen op onvolmaakte doelen sterk. Vergelijkingen in menselijke cellen toonden aan dat het kon matchen of beter presteerde dan een gevestigde high-fidelity SaCas9 en minder foutieve knipsels veroorzaakte dan zijn lagere-fidelity verwanten.
Van reageerbuis naar behandeling van bloedingsstoornissen
Om te testen of de compacte editor in een levend organisme kon werken, verpakte het team SaCas9-NNG en zijn gids-RNA in één enkele AAV8-vector en injecteerde die in muizen. Met als doel het menselijke stollingsfactor 9 (F9)-gen, belangrijk bij hemofilie B, zagen ze efficiënte invoer van kleine DNA-veranderingen (indels) op NNG-sites in de lever, inclusief sites die standaard SaCas9 niet kon bereiken. Ze maakten ook base-editingversies die één DNA-letter wisselen zonder de streng te knippen. In muismodellen met menselijke hemofilie B-mutaties corrigeerde de op SaCas9-NNG gebaseerde adenine-base-editor ziekteveroorzakende veranderingen zowel bij een klassieke PAM als bij een eerder ontoegankelijke PAM. Behandelde dieren toonden aanzienlijke toename van stollingsfactor-activiteit in hun bloed, wat wijst op functioneel herstel.
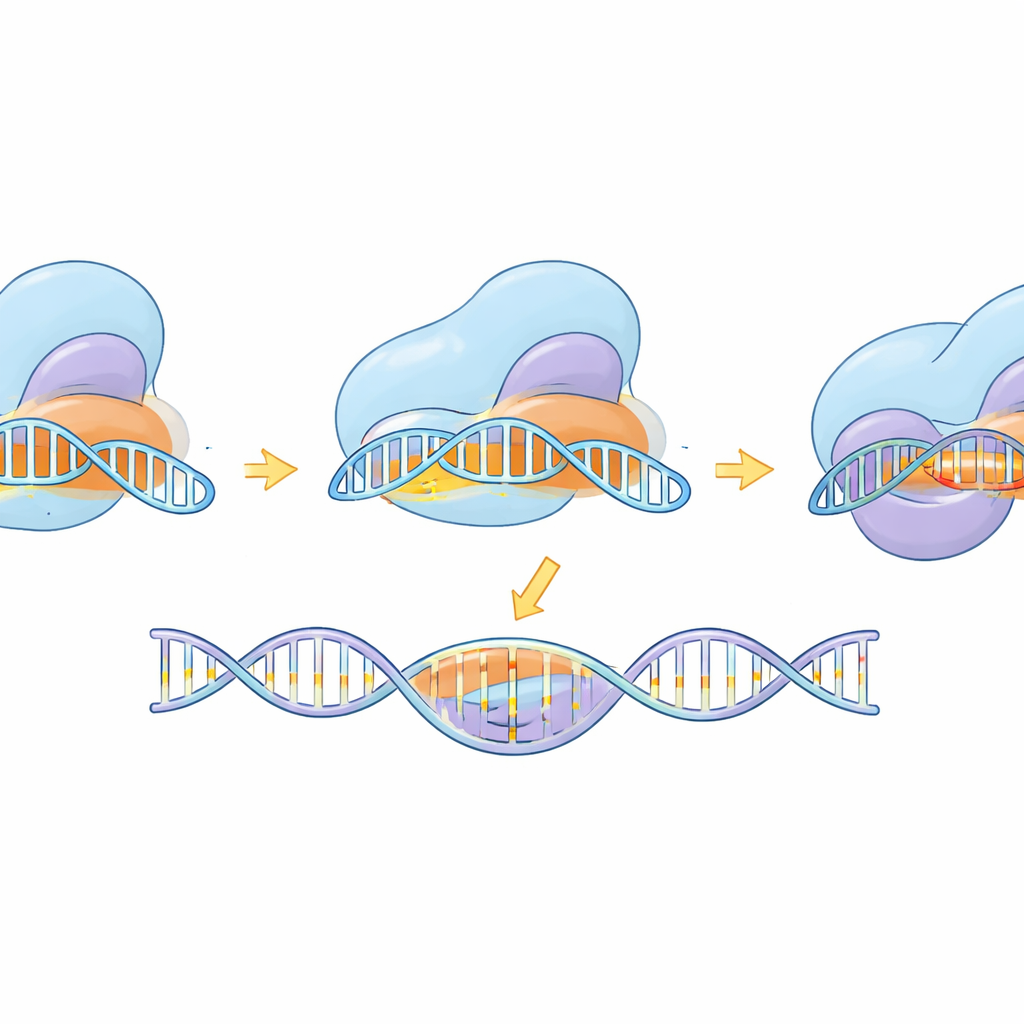
Het moleculaire machine in actie bekijken
Buiten het bouwen van het werktuig gebruikte de studie cryo-elektronenmicroscopie om eSaCas9-NNG vast te leggen in meerdere snapshots langs zijn werkcyclus—voordat het DNA bindt, terwijl het potentiële sites test, tijdens gedeeltelijke pairing met het doel, en in volledig geactiveerde vorm klaar om te knippen. Deze structuren laten zien hoe het enzym eerst vastklikt op een compatibele NNG-tag en vervolgens geleidelijk een RNA–DNA hybride helix vormt. Alleen wanneer de helix lang en correct gematched is, zwaaien interne domeinen in positie en lijnen de knipcentra op beide DNA-strengen uit. De geïngineerde mutaties die de specificiteit verbeterden, bleken de binding aan gedesintegreerd, mismatched DNA aan het verre uiteinde van de helix te destabiliseren, waardoor loslaten boven foutief knippen werd bevoordeeld. Vergelijking met een verwante, meer flexibele SpCas9-variant toont dat, ondanks verschillende vormen, beide een gedeelde logica volgen: volledige, nauwkeurige basenparing is vereist om de finale knipbeweging vrij te geven.
Wat dit betekent voor toekomstige gentherapieën
Voor niet-specialisten is de kernboodschap dat de auteurs een kleiner, veelzijdiger en zorgvuldiger genbewerkingsinstrument hebben ontwikkeld. eSaCas9-NNG kan een veel groter deel van het genoom doelgericht bereiken dan de oorspronkelijke SaCas9, behoudt toch hoge precisie en is compact genoeg om in één AAV-pakket te worden afgeleverd—een belangrijke vereiste voor veel in vivo-therapieën. Het succes bij het corrigeren van stollingsdefecten in hemofilie B-muismodellen, samen met gedetailleerd structureel inzicht in hoe het werkt en fouten vermijdt, positioneert dit enzym als een veelbelovend fundament voor volgende-generatie behandelingen en voor toekomstige verfijningen zoals nog preciezere base- en prime-editors.
Bronvermelding: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Trefwoorden: CRISPR, gentherapie, Cas9, base-editing, hemofilie B