Clear Sky Science · sv
Konstruering av en kompakt högfidelitetsvariant av Staphylococcus aureus Cas9 med bredare målområde och mekanistisk insikt i dess aktivering
Mindre saxar för att reparera defekta gener
Geredigeringsverktyg som CRISPR-Cas9 lovar behandlingar för ärftliga sjukdomar, men de mest använda varianterna är klumpiga och kan av misstag klippa fel bit av DNA. Denna studie presenterar en kompakt, högprecisions DNA‑"sax" baserad på ett enzym från Staphylococcus aureus, omdesignad för att nå många fler platser i genomet samtidigt som den klipper med stor noggrannhet. Eftersom den är tillräckligt liten för att rymmas i ett vanligt genterapivirus och fungerar väl både i celler och i möss, kan den föra säkrare DNA‑reparation närmare verklig medicinsk användning.
Varför storlek och noggrannhet spelar roll
Det ursprungliga arbetsdjuret för genredigering, SpCas9, kommer från Streptococcus pyogenes. Det är kraftfullt men stort, vilket gör det svårt att paketera i adenoassocierade virusvektorer (AAV) som ofta används för att leverera genterapier. Det känner dessutom bara igen korta DNA‑taggar, så kallade PAMs, av formen NGG. Dessa begränsningar gör att många sjukdomsframkallande mutationer ligger utanför räckhåll. En mindre släkting, SaCas9 från Staphylococcus aureus, får plats i AAV och klipper DNA effektivt, men kräver en längre och ovanligare PAM‑sekvens, vilket kraftigt minskar antalet redigerbara platser. Försök att luckra upp dessa PAM‑regler i olika Cas9‑varianter har ofta inneburit en kompromiss: fler mål men också fler oönskade klippningar.
Att skapa en bredare, säkrare genredigerare
Med detaljerad strukturell kunskap om SaCas9 bytte författarna systematiskt ut aminosyror som gör direkta, bokstavsspecifika kontakter med PAM‑sekvensen. De introducerade sedan nya positivt laddade rester som tar ett mer allmänt grepp om DNA‑ryggraden. Detta gav en variant som de kallade SaCas9‑NNG, vilken känner igen enkla NNG‑PAMs istället för den striktare NNGRRT‑mallen, vilket avsevärt ökar antalet potentiella redigeringsplatser. Ytterligare finslipning tog bort en subtil krock som hade försvagat aktiviteten vid vissa sekvenser. I reaktioner i provrör och i human‑celler klippte eller omskrev SaCas9‑NNG effektivt DNA vid ett brett panel av NNG‑platser, särskilt de som slutar med C eller T som det ursprungliga enzymet inte nådde. Över många mål matchade eller överträffade dess prestanda andra ”PAM‑lättade” redigerare som SpRY, SpG och iGeoCas9.
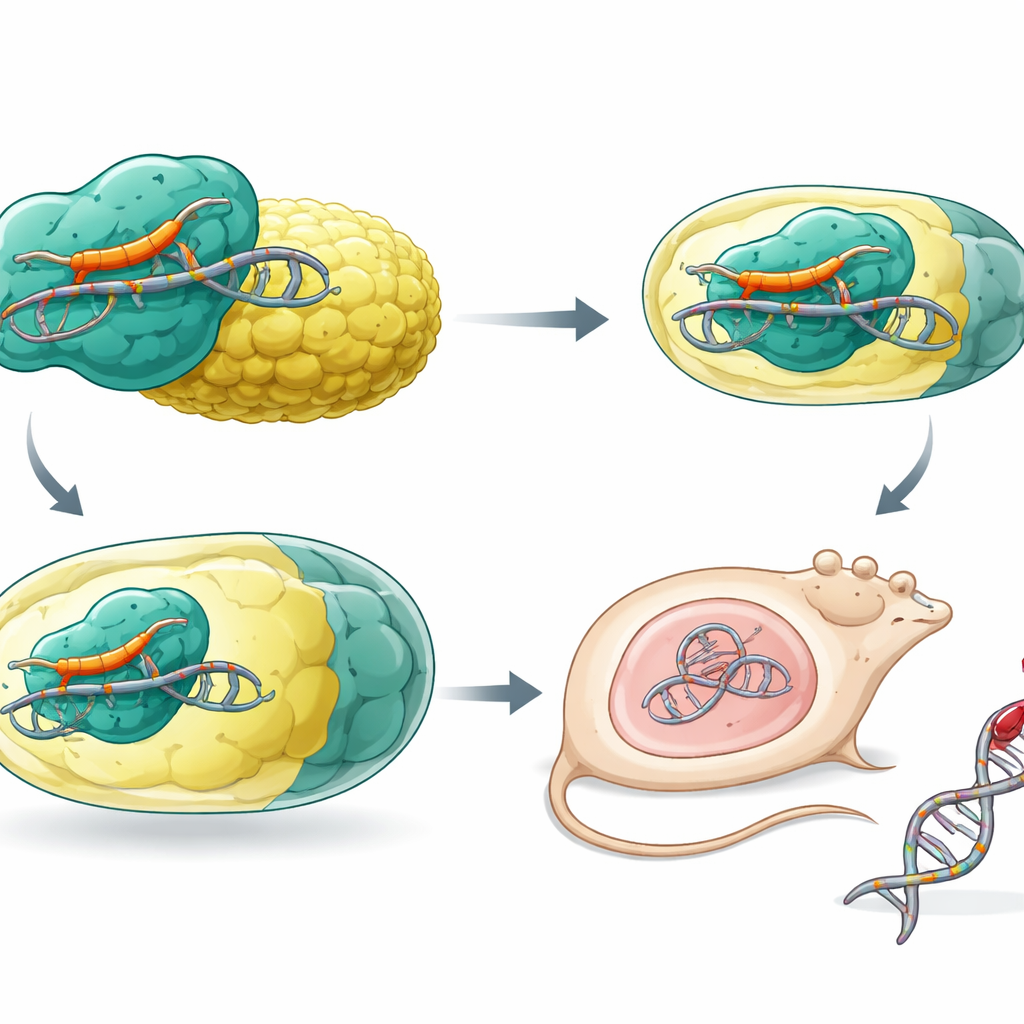
Göra redigeringarna mer tillförlitliga
Att utöka var Cas9 kan klippa väcker en avgörande fråga: kan det fortfarande undvika felaktiga platser? För att hantera detta konstruerade teamet en högfidelitetsversion genom att försvaga vissa kontakter som hjälper proteinet att tolerera mismatch mellan dess guide‑RNA och DNA. Två viktiga substitutioner i en region som stabiliserar den avlägsna änden av RNA–DNA‑helixen gjorde enzymet mindre förlåtande mot mismatch, särskilt de långt från PAM som ofta orsakar off‑target‑klipp. Denna variant, kallad eSaCas9‑NNG, behöll stark aktivitet på korrekta mål men minskade markant klippningen vid ofullständiga matchningar. Jämförelser i humana celler visade att den motsvarade eller överträffade en etablerad högfidelitets SaCas9 och hade färre oönskade klipp än sina lägre‑fidelitets‑släktingar.
Från provrör till behandling av blödningsrubbningar
För att testa om den kompakta redigeraren kunde fungera i en levande organism paketerade forskarna SaCas9‑NNG och dess guide‑RNA i en enda AAV8‑vektor och injicerade den i möss. Genom att rikta in sig på den humana koagulationsfaktorn 9 (F9), viktig vid hemofili B, såg de effektiv införing av små DNA‑ändringar (indels) vid NNG‑platser i levern, inklusive platser som standard SaCas9 inte kunde nå. De skapade också base‑redigeringsvarianter som byter en enskild DNA‑bokstav utan att klippa strängen. I musmodeller som bar humana hemofili B‑mutationer korrigerade den adenin‑base‑editor som byggts på SaCas9‑NNG sjukdomsframkallande förändringar både vid en klassisk PAM och vid en tidigare otillgänglig sådan. Behandlade djur visade betydande ökningar av koagulationsfaktoraktivitet i blodet, vilket indikerar funktionell återställning.
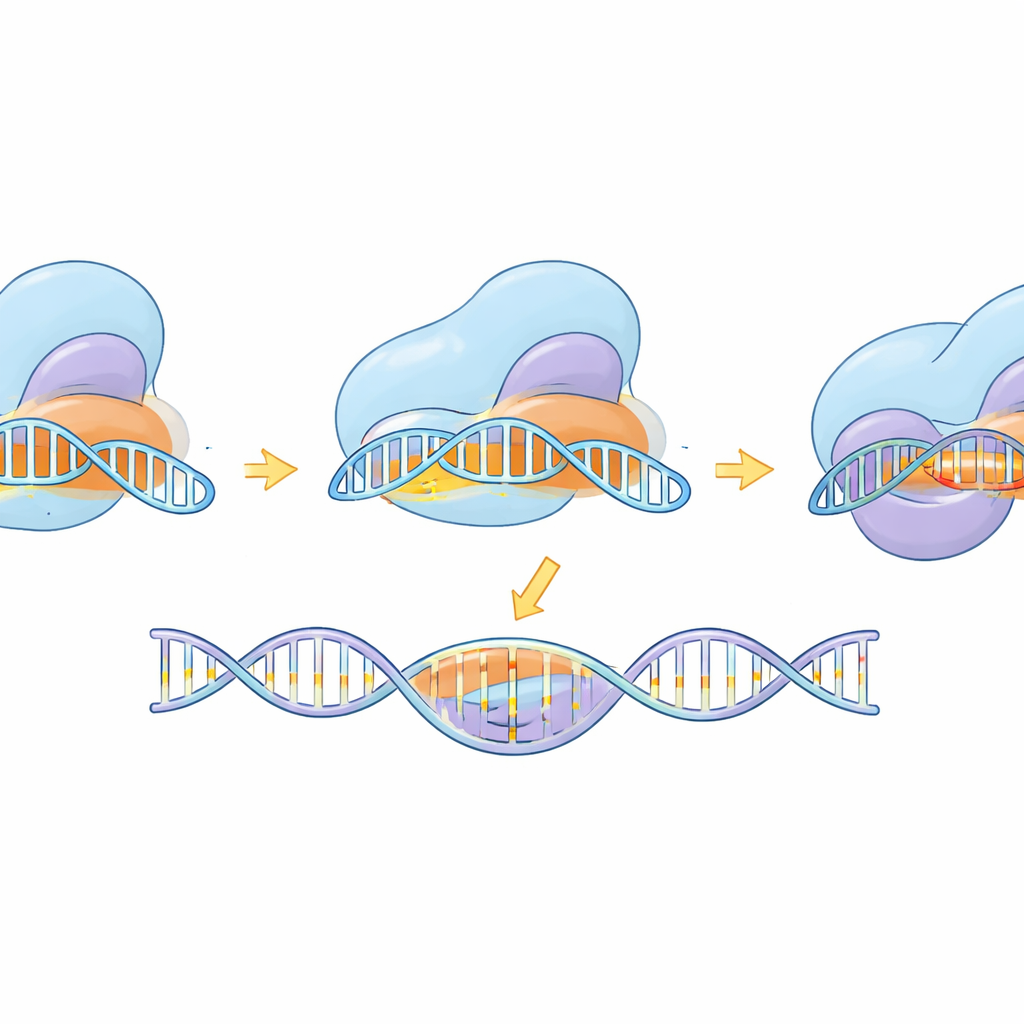
Att observera den molekylära maskinen i arbete
Bortom verktygsskapande använde studien kryoelektronmikroskopi för att fånga eSaCas9‑NNG i flera ögonblicksbilder längs dess arbetscykel—innan DNA‑bindning, när potentiella platser testas, under partiell parade med målet och i fullt aktiverad form redo att klippa. Dessa strukturer visar hur enzymet först hakar fast vid en kompatibel NNG‑tagg, och sedan gradvis bildar en RNA–DNA‑hybridhelix. Först när helixen är lång och korrekt matchad svänger inre domäner på plats och riktar in klippcentren på båda DNA‑strängarna. De konstruerade mutationerna som förbättrade specificiteten visade sig destabilisera bindningen till förvrängt, mismatchat DNA i den avlägsna änden av helixen, vilket gynnar frisläppning framför felaktigt klipp. Jämförelse med en närbesläktad, mer flexibel SpCas9‑variant visar att trots olika former följer båda en gemensam logik: fullständig, korrekt basparning krävs för att låsa upp den slutliga klippsrörelsen.
Vad det här betyder för framtida genterapier
För icke‑specialister är huvudbudskapet att författarna har skapat ett mindre, mer flexibelt och mer varsamt genredigeringsverktyg. eSaCas9‑NNG kan rikta in sig mot en mycket större del av genomet än ursprungliga SaCas9, samtidigt som det behåller hög precision, och är tillräckligt kompakt för att levereras i ett enda AAV‑paket—en nyckelkrav för många in vivo‑terapier. Dess framgång i att korrigera koagulationsdefekter i hemofili B‑musmodeller, tillsammans med detaljerad strukturell insikt i hur det fungerar och undviker misstag, placerar detta enzym som en lovande bas för nästa generations behandlingar och för framtida förbättringar såsom ännu mer precisa base‑ och prime‑redigerare.
Citering: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Nyckelord: CRISPR, genterapi, Cas9, base-redigering, hemofili B