Clear Sky Science · it
Progettazione di una variante compatta e ad alta fedeltà di Cas9 da Staphylococcus aureus con gamma di targeting più ampia e approfondimenti meccanicistici sulla sua attivazione
Forbici più piccole per riparare geni difettosi
Strumenti di editing genico come CRISPR-Cas9 promettono terapie per malattie ereditarie, ma le varianti più diffuse sono ingombranti e possono accidentalmente tagliare il pezzo sbagliato di DNA. Questo studio presenta delle “forbici” del DNA compatte e altamente accurate basate su un enzima di Staphylococcus aureus, riprogettate per raggiungere molti più siti nel genoma pur mantenendo un taglio preciso. Poiché sono abbastanza piccole da entrare in un comune virus usato per la terapia genica e funzionano bene sia in cellule che in topo, potrebbero avvicinare la riparazione del DNA più sicura all’impiego medico reale.
Perché dimensione e accuratezza contano
Il cavallo di battaglia originale dell’editing del genoma, SpCas9, proviene da Streptococcus pyogenes. È potente ma di grande dimensione, il che rende difficile il suo confezionamento nei vettori adeno-associati (AAV) ampiamente usati per somministrare terapie geniche. Riconosce inoltre solo brevi segnali di DNA, detti PAM, della forma NGG. Queste limitazioni lasciano molti mutazioni responsabili di malattie fuori portata. Un cugino più piccolo, SaCas9 di Staphylococcus aureus, si adatta comodamente all’interno di un AAV e taglia il DNA in modo efficiente, ma richiede una sequenza PAM più lunga e rara, riducendo nettamente il numero di siti modificabili. I tentativi di allentare queste regole del PAM in varie versioni di Cas9 hanno spesso creato un compromesso: più bersagli a scapito di maggiori danni fuori bersaglio.
Progettare un editor genico più ampio e più sicuro
Utilizzando una conoscenza strutturale dettagliata di SaCas9, gli autori hanno sostituito in modo sistematico gli amminoacidi che stabiliscono contatti diretti e specifici con la sequenza PAM. Hanno poi introdotto nuovi residui carichi positivamente che afferrano più in generale lo scheletro del DNA. Questo ha prodotto una variante chiamata SaCas9-NNG, che riconosce PAM semplici di tipo NNG invece del più stringente modello NNGRRT, ampliando notevolmente il numero di siti potenzialmente editabili. Un’ulteriore messa a punto ha rimosso un sottile conflitto che riduceva l’attività su alcune sequenze. In reazioni in provetta e in cellule umane, SaCas9-NNG ha tagliato o riscritto efficacemente il DNA su un ampio pannello di siti NNG, in particolare quelli terminanti in C o T che l’enzima originale non poteva toccare. Su molti bersagli, le sue prestazioni hanno eguagliato o superato altri editor “con PAM allentato” come SpRY, SpG e iGeoCas9.
Rendere le modifiche più affidabili
Espandere i luoghi in cui Cas9 può tagliare pone una questione cruciale: può ancora evitare i posti sbagliati? Per affrontare questo aspetto, il gruppo ha ingegnerizzato una versione ad alta fedeltà indebolendo alcuni contatti che consentono alla proteina di tollerare discrepanze tra il suo RNA guida e il DNA. Due sostituzioni chiave in una regione che stabilizza l’estremità lontana dell’elica RNA–DNA hanno reso l’enzima meno permissivo verso gli errori di appaiamento, in particolare quelli distanti dal PAM che sono una fonte comune di tagli fuori bersaglio. Questa variante, chiamata eSaCas9-NNG, ha mantenuto un’elevata attività sui bersagli corretti ma ha ridotto nettamente i tagli su bersagli imperfetti. Confronti in cellule umane hanno mostrato che eSaCas9-NNG si è allineata o ha superato una SaCas9 ad alta fedeltà già consolidata e ha prodotto meno tagli spurii rispetto alle sue controparti a fedeltà inferiore.
Dalla provetta al trattamento dei disturbi emorragici
Per verificare se l’editor compatto potesse funzionare in un organismo vivente, i ricercatori hanno confezionato SaCas9-NNG e il suo RNA guida in un singolo vettore AAV8 e lo hanno iniettato nei topi. Mirando al gene umano del fattore della coagulazione 9 (F9), importante nell’emofilia B, hanno osservato l’efficiente introduzione di piccole modifiche del DNA (indel) in siti NNG nel fegato, inclusi siti che la SaCas9 standard non poteva raggiungere. Hanno anche creato versioni per base editing che sostituiscono una singola lettera del DNA senza tagliare il filamento. In modelli murini portatori di mutazioni umane dell’emofilia B, l’editor di adenina costruito su SaCas9-NNG ha corretto variazioni causanti malattia sia in un PAM classico sia in uno precedentemente inaccessibile. Gli animali trattati hanno mostrato aumenti sostanziali dell’attività del fattore della coagulazione nel sangue, indicativi di un recupero funzionale.
Osservare la macchina molecolare in azione
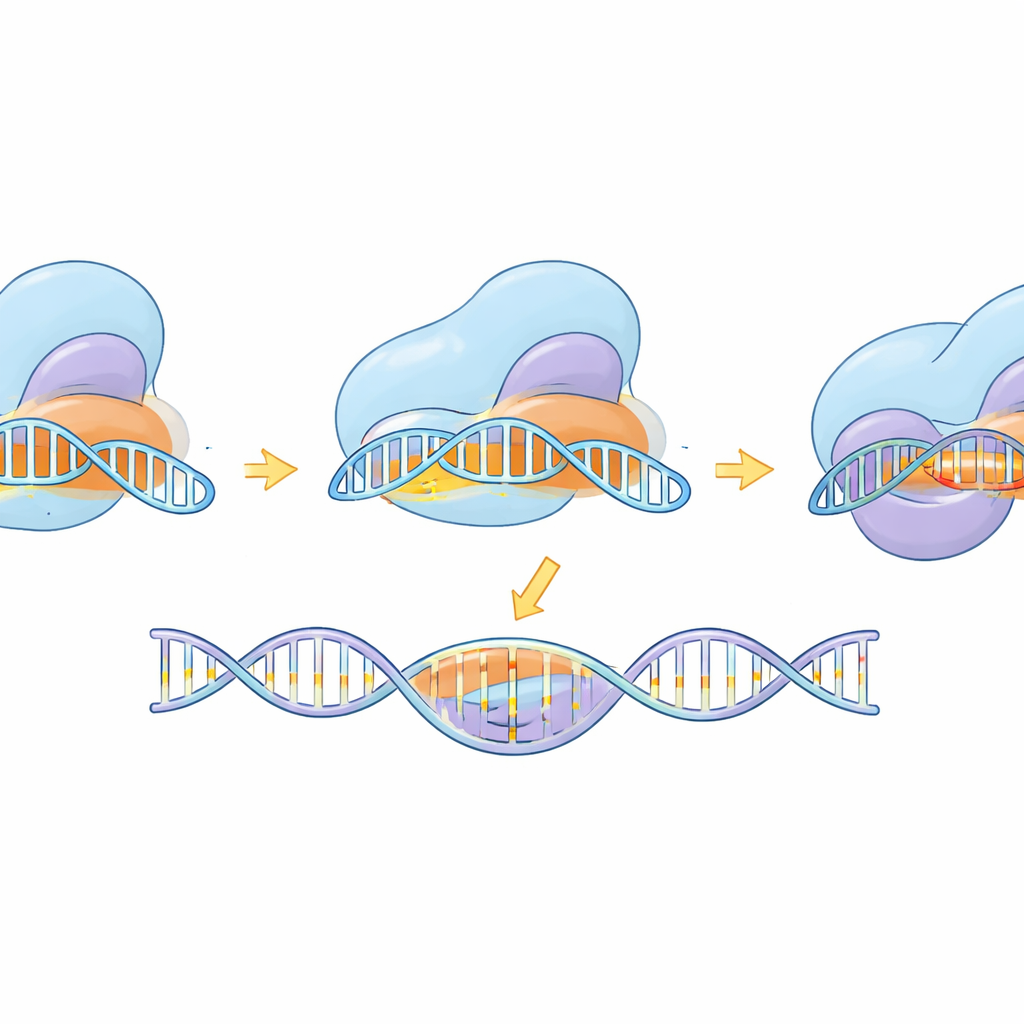
Oltre alla costruzione dello strumento, lo studio ha usato la criomicroscopia elettronica per catturare eSaCas9-NNG in molteplici istantanee lungo il suo ciclo operativo—prima del legame al DNA, mentre testa siti potenziali, durante l’appaiamento parziale con il bersaglio e nella forma completamente attivata pronta al taglio. Queste strutture rivelano come l’enzima si agganci inizialmente a un tag NNG compatibile, quindi formi gradualmente un’elica ibrida RNA–DNA. Solo quando l’elica è lunga e correttamente appaiata i domini interni ruotano in posizione e allineano i centri di taglio su entrambi i filamenti del DNA. Le mutazioni ingegnerizzate che hanno migliorato la specificità sono state osservate destabilizzare il legame a DNA distorti o con mismatch all’estremità lontana dell’elica, favorendo il rilascio piuttosto che un taglio erroneo. Il confronto con una variante correlata e più flessibile di SpCas9 mostra che, nonostante forme diverse, entrambe seguono una logica condivisa: un appaiamento completo e accurato delle basi è necessario per sbloccare il movimento finale di taglio.
Cosa significa per le future terapie geniche
Per i non specialisti, il messaggio centrale è che gli autori hanno realizzato uno strumento di editing genico più piccolo, più versatile e più prudente. eSaCas9-NNG può mirare a una frazione molto più ampia del genoma rispetto alla SaCas9 originale, pur mantenendo alta precisione, ed è abbastanza compatto da essere consegnato in un unico pacchetto AAV—un requisito chiave per molte terapie in vivo. Il suo successo nel correggere difetti della coagulazione in modelli murini di emofilia B, insieme a dettagliate intuizioni strutturali su come funziona ed evita errori, pone questo enzima come una promettente base per terapie di nuova generazione e per futuri perfezionamenti come editor di basi e prime ancora più precisi.
Citazione: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Parole chiave: CRISPR, terapia genica, Cas9, editing di basi, emofilia B