Clear Sky Science · ar
تصميم متغيّر صغير وعالي الدقّة لإنزيم Cas9 من Staphylococcus aureus مع مدى استهداف أوسع ورؤى ميكانيكية حول تفعيله
مقصات أصغر لإصلاح الجينات المعيبة
تعد أدوات تحرير الجينات مثل CRISPR‑Cas9 بعلاجات للأمراض الوراثية، لكن النسخ الأكثر استخدامًا كبيرة الحجم وقد تقصّ الخيط الخاطئ من الـDNA عن غير قصد. تقدّم هذه الدراسة «مقصًا» صغيرًا ودقيقًا مبنيًا على إنزيم من Staphylococcus aureus، أعيد تصميمه للوصول إلى مواضع أكثر في الجينوم مع الحفاظ على دقة القَص. وبما أنه صغير بما يكفي للارتباط بحامل فيروس شائع للعلاج الجيني ويعمل جيدًا في الخلايا والفئران، فقد يقرب إصلاح الـDNA الآمن من التطبيق الطبي الواقعي.
لماذا الحجم والدقّة مهمان
المحرّك الأصلي لتحرير الجينوم، SpCas9، يأتي من Streptococcus pyogenes. هو قوي لكن ضخم، ما يصعّب تعبئته في ناقلات فيروسية معروفة مثل الفيروس الحلقي المرتبط بالفيروس الغدي (AAV) المستخدمة على نطاق واسع لتوصيل العلاجات الجينية. كما أنه يتعرّف فقط على علامات قصيرة في الـDNA تُسمى PAM من الشكل NGG. هذه القيود تترك العديد من الطفرات المسببة للأمراض بعيدة عن المتناول. نظير أصغر، SaCas9 من Staphylococcus aureus، يتسع بسهولة داخل AAV ويقطع الـDNA بكفاءة، لكنه يتطلب تسلسل PAM أطول ونادرًا، مما يقلص بشدّة عدد المواقع القابلة للتحرير. محاولات تسييل قواعد PAM في نسخ مختلفة من Cas9 أدّت غالبًا إلى مقايضة: أهداف أكثر لكن أضرارًا غير مقصودة أكثر.
هندسة محرر جيني أوسع وأكثر أمانًا
باستخدام معرفة هيكلية مفصلة لـSaCas9، استبدل الباحثون منهجيًا الأحماض الأمينية التي تقيم اتصالات مباشرة ومحددة بالحروف مع تسلسل PAM. ثم أدخلوا شحنات موجبة جديدة تمسك بالعمود الفقري للـDNA بشكل عام. أنتج هذا متغيّرًا أسماه SaCas9‑NNG، الذي يتعرّف على PAMs بسيطة من نوع NNG بدلًا من نمط NNGRRT الأكثر تقييدًا، موسعًا بذلك عدد مواقع التحرير المحتملة بشكل كبير. تعديل دقيق آخر أزال تصادمًا طفيفًا كان يضعف النشاط عند بعض التسلسلات. في تفاعلات أنبوبية وخلايا بشرية، قطع SaCas9‑NNG أو أعاد كتابة الـDNA بكفاءة عند مجموعة واسعة من مواقع NNG، خاصة تلك التي تنتهي بـC أو T والتي لم يستطع الإنزيم الأصلي الوصول إليها. عبر العديد من الأهداف، كانت أداؤه يضاهي أو يتفوّق على محرّرين «مُرخّصي PAM» آخرين مثل SpRY وSpG وiGeoCas9.
جعل التعديلات أكثر موثوقية
توسيع الأماكن التي يمكن أن يقطعها Cas9 يطرح سؤالًا حاسمًا: هل ما زال يتجنب المواقع الخاطئة؟ لمعالجة هذا، هدفت المجموعة إلى هندسة نسخة عالية الدقّة عن طريق إضعاف اتصالات معيّنة تساعد البروتين على التسامح مع عدم التطابق بين الدليل الريبي (guide RNA) والـDNA. أدت تبديلتان رئيسيتان في منطقة تُثبّت الطرف البعيد لهيكل RNA–DNA إلى جعل الإنزيم أقل تساهلًا مع عدم التطابقات، خاصة تلك البعيدة عن PAM والتي تعد مصدرًا شائعًا للقصوص غير المرغوبة. حافظ هذا المتغيّر، المسمّى eSaCas9‑NNG، على نشاط قوي على الأهداف الصحيحة لكنه خفّض بشكل حاد القص على الأهداف غير المطابقة. أظهرت المقارنات في خلايا بشرية أنه ضاهى أو تفوّق على SaCas9 عالي الدقّة المعروف وسبّب قصوصًا عشوائية أقل من أقربائه الأقل دقّة.
من أنبوب الاختبار إلى علاج اضطرابات النزف
لاختبار ما إذا كان المحرّر الصغير يعمل داخل كائن حي، عبّأ الباحثون SaCas9‑NNG ودليل RNA الخاص به في ناقل AAV8 واحد وحقنوه في فئران. باستهداف جين العامل التاسع للتخثّر البشري (F9)، المهم في النزاف باء، لاحظوا إدخال تغيّرات صغيرة في الـDNA (indels) بكفاءة عند مواقع NNG في الكبد، بما في ذلك مواقع لم تستطع SaCas9 القياسية الوصول إليها. كما أنشأوا نسخ تحرير قاعدية تبدّل حرف DNA واحدًا دون قص الخيط. في نماذج فئران تحمل طفرات نزاف باء البشرية، صحّح محرّر قاعدة الأدينين المبني على SaCas9‑NNG التغيرات المسببة للمرض عند كل من PAM الكلاسيكي وآخر كان غير متاح سابقًا. أظهرت الحيوانات المعالجة زيادات كبيرة في نشاط عامل التخثّر في الدم، ما يدل على استعادة وظيفية.
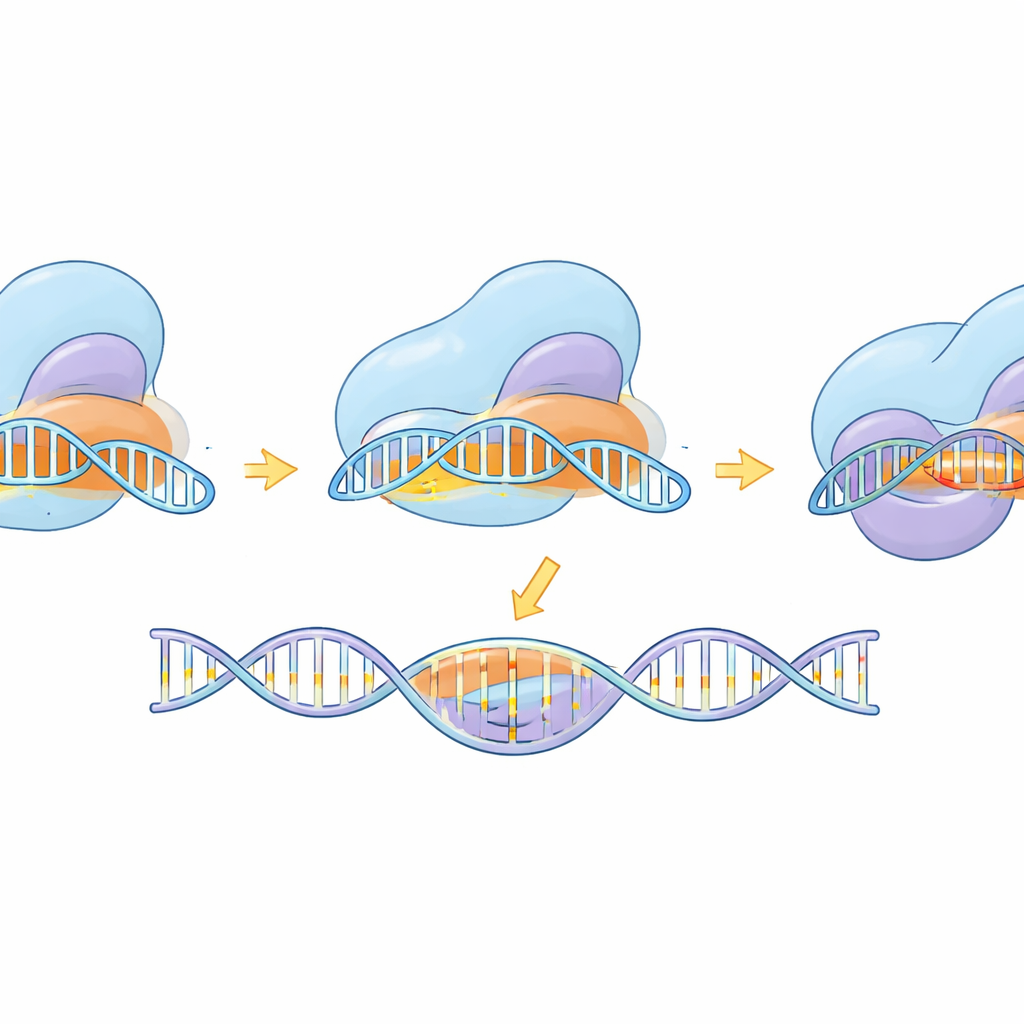
مشاهدة الجهاز الجزيئي أثناء العمل
بعيدًا عن بناء الأدوات، استخدمت الدراسة المجهر الإلكتروني بالتبريد (cryo‑EM) لالتقاط eSaCas9‑NNG في لقطات متعددة على طول دورة عمله—قبل ارتباطه بالـDNA، أثناء اختبار المواقع المحتملة، خلال التزاوج الجزئي مع الهدف، وفي الحالة المنشّطة بالكامل الجاهزة للقص. تكشف هذه البنى كيف يلتقط الإنزيم أولًا وسم NNG متوافقًا، ثم يشكّل تدريجيًا حلزونًا هجينًا من RNA–DNA. فقط عندما يكون الحلزون طويلًا ومطابقًا بدقة تتحرك المجالات الداخلية إلى مواضعها وتُحصِّل مراكز القص على كلا جدلي الـDNA. لوحظ أن الطفرات الهندسية التي حسّنت الدقّة تسبّب عدم استقرار ارتباط بالـDNA المشوَّه أو غير المطابق عند الطرف البعيد من الحلزون، مفضّلةً تحرير الرابطة بدلًا من القص الخاطئ. بالمقارنة مع متغيّر SpCas9 ذو مرونة أكبر، يتضح أنه بالرغم من الاختلافات الشكلية يتبع كلاهما منطقًا مشتركًا: توائم قواعد كاملة ودقيقة لازمة لفتح الحركة النهائية للقص.
ما الذي يعنيه هذا لعلاجات الجينات المستقبلية
للغير متخصصين، الرسالة الأساسية هي أن الباحثين صمّموا أداة تحرير جيني أصغر وأكثر تنوعًا وأكثر حيطة. eSaCas9‑NNG يمكنه استهداف جزء أكبر بكثير من الجينوم مقارنةً بـSaCas9 الأصلي، مع الحفاظ على دقّة عالية، وهو صغير بما يكفي للتوصيل داخل ناقل AAV واحد—متطلب أساسي للعديد من العلاجات داخل الجسم. نجاحه في تصحيح عيوب التخثّر في نماذج فئران نزاف باء، إلى جانب رؤى هيكلية مفصّلة حول كيفية عمله وتجنبه للأخطاء، يضع هذا الإنزيم كأساس واعد للأجيال القادمة من العلاجات وللتحسينات المستقبلية مثل محرّرات قواعد وبرايم أكثر دقّة.
الاستشهاد: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
الكلمات المفتاحية: CRISPR, العلاج الجيني, Cas9, التحرير القاعدي, النزاف باء