Clear Sky Science · fr
Conception d’une variante compacte et haute-fidélité de Cas9 de Staphylococcus aureus avec une plage de ciblage élargie et des éclairages mécanistiques sur son activation
Des ciseaux plus petits pour réparer des gènes défectueux
Les outils d’édition génétique comme CRISPR-Cas9 promettent des traitements pour des maladies héréditaires, mais les versions les plus répandues sont volumineuses et peuvent par erreur couper le mauvais fragment d’ADN. Cette étude présente des « ciseaux » d’ADN compacts et très précis basés sur une enzyme de Staphylococcus aureus, repensés pour atteindre beaucoup plus de sites dans le génome tout en conservant une grande précision de découpe. Parce qu’il est suffisamment petit pour tenir dans un vecteur viral couramment utilisé en thérapie génique et qu’il fonctionne bien à la fois dans des cellules et chez la souris, il pourrait rapprocher des réparations d’ADN plus sûres d’une utilisation clinique réelle.
Pourquoi la taille et la précision comptent
Le Cas9 historique, SpCas9, provient de Streptococcus pyogenes. Il est puissant mais volumineux, ce qui complique son conditionnement dans des vecteurs adéno-associés (AAV) largement employés pour délivrer des thérapies géniques. Il ne reconnaît en outre que des balises d’ADN courtes, appelées PAM, de la forme NGG. Ces limitations laissent de nombreuses mutations pathogènes hors de portée. Un cousin plus petit, SaCas9 provenant de Staphylococcus aureus, tient confortablement dans un AAV et coupe l’ADN efficacement, mais exige une séquence PAM plus longue et plus rare, réduisant fortement le nombre de sites éditables. Les tentatives pour assouplir ces contraintes de PAM dans diverses versions de Cas9 ont souvent entraîné un compromis : plus de cibles mais aussi plus de coupes hors cible.
Concevoir un éditeur génétique plus large et plus sûr
En s’appuyant sur une connaissance structurale détaillée de SaCas9, les auteurs ont remplacé de manière systématique des acides aminés qui établissent des contacts directs et spécifiques avec la séquence PAM. Ils ont ensuite introduit de nouveaux résidus chargés positivement qui saisissent plus généralement l’épine dorsale de l’ADN. Cela a produit une variante appelée SaCas9-NNG, qui reconnaît des PAM simples de type NNG au lieu du motif plus strict NNGRRT, augmentant considérablement le nombre de sites potentiellement éditables. Un affinage supplémentaire a supprimé un conflit subtil qui affaiblissait l’activité sur certaines séquences. Dans des réactions in vitro et dans des cellules humaines, SaCas9-NNG a coupé ou réécrit l’ADN de façon efficace sur un large panel de sites NNG, en particulier ceux se terminant par C ou T que l’enzyme d’origine ne pouvait pas toucher. Sur de nombreuses cibles, ses performances rivalisaient ou dépassaient celles d’autres éditeurs « relaxant le PAM » tels que SpRY, SpG et iGeoCas9.
Rendre les modifications plus fiables
Élargir les lieux de coupe de Cas9 soulève une question cruciale : peut-il encore éviter les mauvais emplacements ? Pour y répondre, l’équipe a conçu une version haute-fidélité en affaiblissant certains contacts qui aident la protéine à tolérer les mésappariements entre son ARN guide et l’ADN. Deux substitutions clés dans une région qui stabilise l’extrémité lointaine de l’hélice ARN–ADN ont rendu l’enzyme moins tolérante aux mésappariements, en particulier ceux éloignés du PAM, source fréquente de coupes hors cible. Cette variante, nommée eSaCas9-NNG, conserva une forte activité sur les cibles correctes tout en réduisant nettement la coupe sur les cibles imparfaites. Des comparaisons dans des cellules humaines montrèrent qu’elle égalait ou surpassait un SaCas9 haute-fidélité établi et produisait moins de coupes erratiques que ses homologues de fidélité moindre.
Du tube à l’organisme pour traiter les troubles hémorragiques
Pour tester si l’éditeur compact pouvait fonctionner dans un organisme vivant, les chercheurs ont conditionné SaCas9-NNG et son ARN guide dans un unique vecteur AAV8 et l’ont injecté chez la souris. Ciblant le gène humain du facteur de coagulation 9 (F9), important dans l’hémophilie B, ils ont observé l’introduction efficace de petites modifications d’ADN (indels) sur des sites NNG dans le foie, y compris des sites inaccessibles au SaCas9 standard. Ils ont également créé des versions d’édition de bases qui échangent une seule lettre d’ADN sans rompre la chaîne. Dans des modèles murins porteurs de mutations humaines responsables d’hémophilie B, l’éditeur de bases adénine dérivé de SaCas9-NNG a corrigé des changements pathogènes à la fois à un PAM classique et à un PAM auparavant inaccessible. Les animaux traités ont présenté des augmentations substantielles de l’activité du facteur de coagulation dans le sang, indiquant une restauration fonctionnelle.
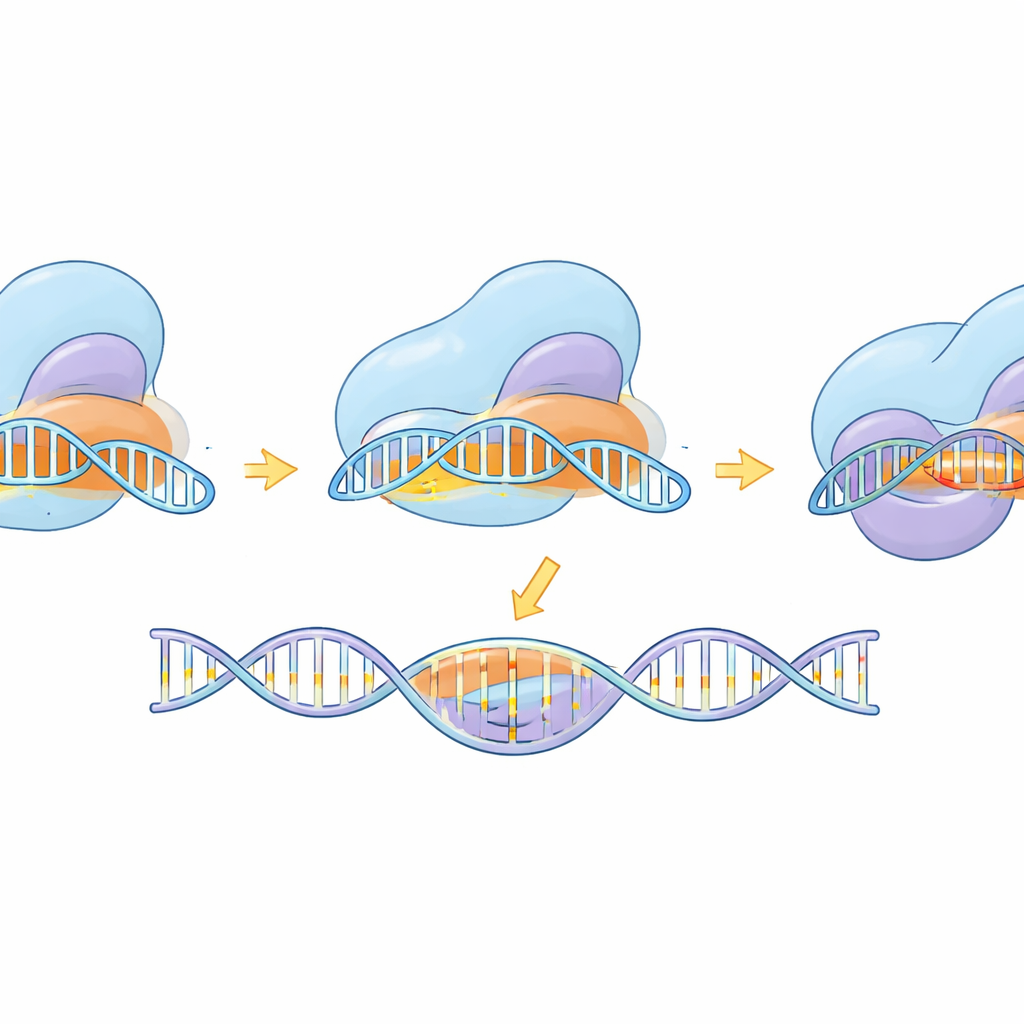
Observer la machine moléculaire en action
Au-delà de la simple conception d’outil, l’étude a utilisé la cryo-microscopie électronique pour capturer eSaCas9-NNG dans plusieurs instantanés le long de son cycle de travail — avant la liaison à l’ADN, lors du test de sites potentiels, pendant le pairage partiel avec la cible, et sous forme pleinement activée prête à couper. Ces structures révèlent comment l’enzyme s’accroche d’abord à une balise NNG compatible, puis forme progressivement une hélice hybride ARN–ADN. Ce n’est que lorsque l’hélice est longue et correctement appariée que des domaines internes basculent en place et alignent les centres de coupe sur les deux brins d’ADN. Les mutations conçues pour améliorer la spécificité apparaissent destabiliser la liaison à l’ADN déformé et mésapparié à l’extrémité lointaine de l’hélice, favorisant le relâchement plutôt que la coupe erronée. La comparaison avec une variante SpCas9 connexe et plus flexible montre que, malgré des conformations différentes, les deux suivent une logique commune : un appariement complet et exact des bases est nécessaire pour déclencher le mouvement final de coupe.
Ce que cela signifie pour les thérapies géniques à venir
Pour les non-spécialistes, le message central est que les auteurs ont élaboré un outil d’édition génétique plus petit, plus polyvalent et plus prudent. eSaCas9-NNG peut cibler une fraction bien plus large du génome que le SaCas9 d’origine, tout en conservant une grande précision, et il est suffisamment compact pour être délivré dans un seul paquet AAV — exigence clé pour de nombreuses thérapies in vivo. Son succès à corriger des défauts de coagulation dans des modèles murins d’hémophilie B, associé à des informations structurales détaillées sur son fonctionnement et sa capacité à éviter les erreurs, positionne cette enzyme comme une base prometteuse pour des traitements de nouvelle génération et pour des améliorations futures telles que des éditeurs de bases et de prime encore plus précis.
Citation: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Mots-clés: CRISPR, thérapie génique, Cas9, édition de bases, hémophilie B