Clear Sky Science · he
הנדסה של וריאנט קומפקטי ודייקן של Cas9 מ‑Staphylococcus aureus עם טווח מטרה רחב יותר ותובנות מכניסטיות על הפעלתו
מספריים קטנים יותר לתיקון גנים פגומים
כלי עריכת גנים כמו CRISPR‑Cas9 מבטיחים טיפולים למחלות תורשתיות, אך הגרסאות הנפוצות ביותר הן מגושמות ולעתים עלולות לחתוך מקטעי DNA לא נכונים. מחקר זה מציג "מספריים" DNA קומפקטיים ודייקנים המבוססים על אנזים מ‑Staphylococcus aureus, שעוצב מחדש כדי להגיע להרבה מקומות נוספים בגנום תוך שמירה על חיתוך מדויק. מאחר שהוא קטן מספיק כדי להיכנס לווירוס טיפולי גנים נפוץ ופועל היטב גם בתאים וגם בעכברים, הוא עשוי לקדם תיקון DNA בטוח יותר לשימוש רפואי מעשי.
מדוע גודל ודיוק חשובים
עבודת הסוס של עריכת הגנום, SpCas9, מגיעה מ‑Streptococcus pyogenes. היא חזקה אך גדולה, מה שמקשה על אריזתה לוקטורי אדנו‑אסוציאטיבי (AAV) שמשמשים רחב לטיפול גנטי. היא גם מזהה רק תגיות קצרות ב‑DNA, שנקראות PAM, בצורת NGG בלבד. מגבלות אלה משאירות הרבה מוטציות גורמות מחלה מחוץ להישג היד. קרובתה הקטנה יותר, SaCas9 מ‑Staphylococcus aureus, נכנסת בנוחות ל‑AAV וחותכת DNA ביעילות, אך דרושה לה רצף PAM ארוך ונדיר יותר, מה שמצמצם במידה ניכרת את מספר האתרים הניתנים לעריכה. ניסיונות להרחיב את כללי ה‑PAM בגרסאות שונות של Cas9 לעתים קרובות יצרו פשרה: יותר מטרות אבל גם יותר חיתוכים לא רצויים.
הנדסה של עורך גנים רחב ובטוח יותר
בהסתמך על ידע מבני מפורט של SaCas9, החוקרים החליפו שיטתית חומצות אמינו שמקיימות קשרים ישירים ותלויי אותיות עם רצף ה‑PAM. לאחר מכן הוסיפו שיירים טעוני מטען חיובי שנוגעים בגב היתד של ה‑DNA באופן כללי יותר. זה הניב וריאנט שנקרא SaCas9‑NNG, שמזהה PAMs פשוטים בצורת NNG במקום התבנית המחמירה NNGRRT, וכך מגדיל מאוד את מספר אתרי העריכה הפוטנציאליים. כוונון נוסף הסיר התנגשות עדינה שהחלישה פעילות במספר רצפים. בתגובות מבחנה ובתאים אנושיים, SaCas9‑NNG חיתך או שכתב DNA ביעילות בפאנל רחב של אתרי NNG, במיוחד אלה שמסתיימים ב‑C או T שהאנזים המקורי לא יכול היה להגיע אליהם. על פני מגוון מטרות, ביצועיו התקרבו או עלו על עורכים "הרפוים PAM" אחרים כגון SpRY, SpG ו‑iGeoCas9.
להפוך את העריכות לאמינות יותר
הרחבת המקומות שבהם Cas9 יכול לחתוך מעלה שאלה קריטית: האם הוא עדיין יכול להימנע מהמקומות הנכונים? כדי לענות על כך, הצוות מהנדס גרסה בעלת אמינות גבוהה על‑ידי השעית קשרים מסוימים שעוזרים לחלבון לסבול אי‑התאמות בין ה‑gRNA ל‑DNA. שתי החלפות מפתח באזור שמייצב את קצה ההליקס של ה‑RNA–DNA הפכו את האנזים לפחות סלחני לאי‑התאמות, במיוחד אלה הרחוקות מה‑PAM שמקורן בחיתוכי יעד לא נכונים. וריאנט זה, שנקרא eSaCas9‑NNG, שמר על פעילות חזקה על מטרות נכונות אך צמצם חדות חיתוך במטרות לא מדויקות. השוואות בתאים אנושיים הדגימו שהוא שווה או עדיף על SaCas9 בעל אמינות גבוהה ידועה, והיו לו פחות חיתוכים שגויים מאשר קרוביו בעלי האמינות הנמוכה יותר.
מבחנה לטיפול בהפרעות דימום
כדי לבדוק האם העורך הקומפקטי יכול לפעול בתוך אורגניזם חי, החוקרים ארזו את SaCas9‑NNG ואת ה‑gRNA שלו בתוך וקטור AAV8 יחיד והזריקו אותו לעכברים. כשהכוונו לגֵן האנושי של גורם הקרישה 9 (F9), החשוב בהמופיליה B, נצפו הכנסת שינויים קטנים ב‑DNA (indels) ביעילות באתרי NNG בכבד, כולל אתרים ש‑SaCas9 הסטנדרטי לא הצליח להגיע אליהם. הם גם פיתחו גרסאות לעריכת בסיס שמחליפות אות בודדת ב‑DNA ללא קריעה של השרשרת. במודלים עכבריים הנושאים מוטציות המופיליה B אנושיות, עורך בסיס האדנין המבוסס על SaCas9‑NNG תיקן שינויים גורמי מחלה הן ב‑PAM קלאסי והן באחד שהיה קודם לכן בלתי נגיש. בעכברים מטופלים נצפתה עלייה משמעותית בפעילות גורם הקרישה בדם, שמעידה על הצלה פונקציונלית.
צפייה במכונה המולקולרית בפעולה
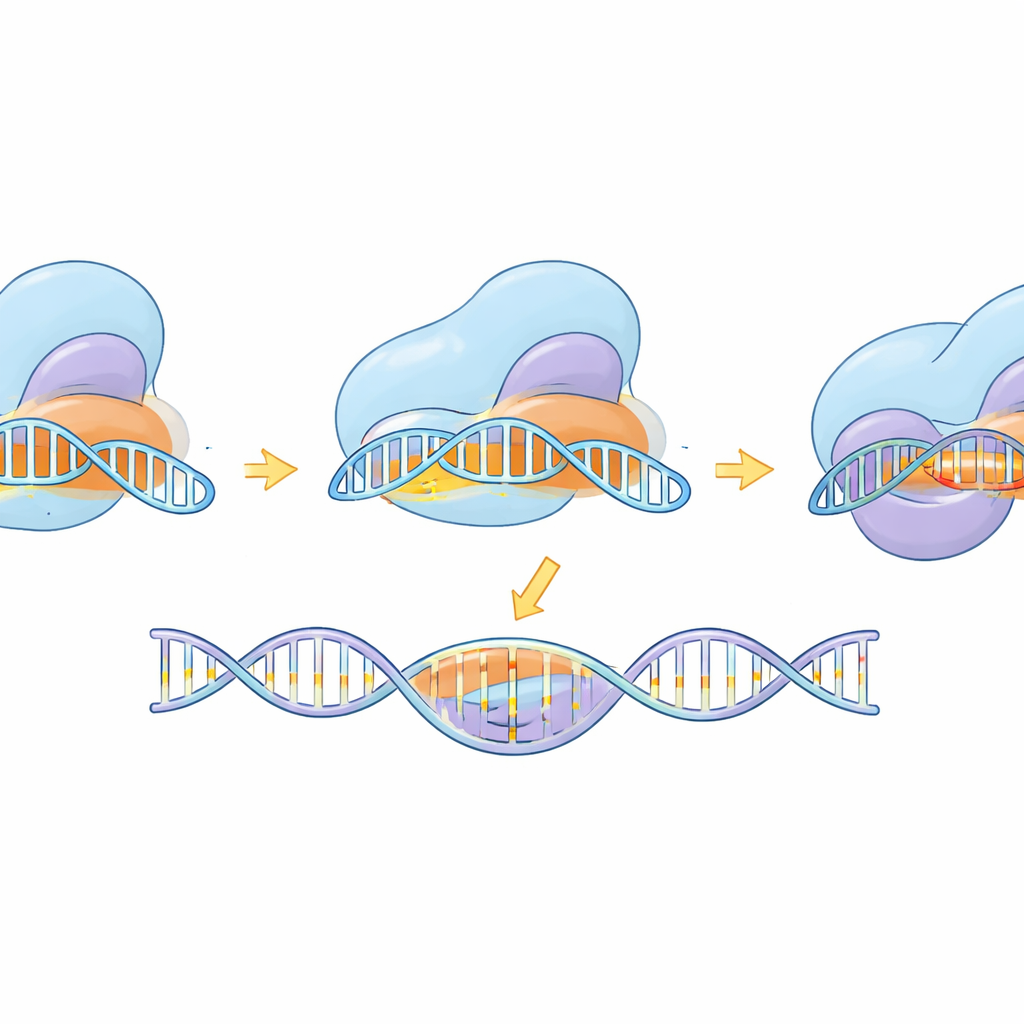
מעבר לבניית כלים, המחקר השתמש במיקרוסקופיה קריואלקטרונית כדי לתפוס את eSaCas9‑NNG במספר תמונות לאורך מחזור העבודה שלו — לפני קשירת ה‑DNA, בזמן בדיקת אתרים פוטנציאליים, במהלך התאמה חלקית מול היעד, ובצורה פעילה לחלוטין המוכנה לחתוך. המבנים הללו מראים כיצד האנזים לוכד תחילה תגית NNG תואמת, ואז יוצר בהדרגה הליקס RNA–DNA היברידי. רק כאשר ההליקס ארוך ומתאים נכונה נעים תחומים פנימיים למקומם ומיישרים את מרכזי החיתוך בשתי גדילי ה‑DNA. המוטציות ההנדסיות ששיפרו את הספציפיות נראו כמפריעות ליציבות הקשירה ל‑DNA מעוות ולא תואם בקצה הרחוק של ההליקס, מה שמעדיף שחרור על פני חיתוך שגוי. השוואה לגרסה קרובה וגמישה יותר של SpCas9 מראה שלמרות הצורות השונות, שתיהן פועלות לפי לוגיקה משותפת: התאמה בסיסית מלאה ומדויקת נחוצה כדי לפתוח את תנועת החיתוך הסופית.
מה זה אומר עבור טיפולים גנטיים עתידיים
לאלה שאינם מומחים, המסר המרכזי הוא שהחוקרים פיתחו כלי עריכת גנים קטן יותר, ורסטילי וזהיר יותר. eSaCas9‑NNG יכול לטרגט חלק גדול הרבה יותר מהגנום מאשר SaCas9 המקורי, ועדיין לשמור על דיוק גבוה, והוא קומפקטי דיו כדי להימסר באריזת AAV יחידה — דרישה מרכזית עבור טיפולים רבים שבוצעו בתוך הגוף. הצלחתו בתיקון פגמים בקרישה במודלים של המופיליה B בעכברים, יחד עם תובנות מבניות מפורטות על אופן פעולתו ואיך הוא נמנע מטעויות, מציבות אנזים זה כביסוס מבטיח לדור הבא של טיפולים ולכיוונים עתידיים של שיפורים כגון עורכי בסיס ו‑prime מדויקים אף יותר.
ציטוט: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
מילות מפתח: CRISPR, טיפול גנטי, Cas9, עריכת בסיסים, המופיליה B