Clear Sky Science · pt
Engenharia de uma variante compacta e de alta fidelidade da Cas9 de Staphylococcus aureus com alcance de alvo ampliado e insights mecanicistas sobre sua ativação
Tesouras menores para corrigir genes defeituosos
Ferramentas de edição gênica como CRISPR-Cas9 prometem tratamentos para doenças hereditárias, mas as versões mais populares são volumosas e podem cortar acidentalmente a região errada do DNA. Este estudo apresenta umas “tesouras” de DNA compactas e altamente precisas, baseadas em uma enzima de Staphylococcus aureus, redesenhadas para alcançar muito mais locais no genoma mantendo a precisão do corte. Como é pequena o suficiente para caber em um vírus comum de terapia gênica e funciona bem tanto em células quanto em camundongos, ela pode aproximar reparos de DNA mais seguros de aplicações médicas reais.
Por que tamanho e precisão importam
O cavalo de batalha original da edição do genoma, SpCas9, vem de Streptococcus pyogenes. É potente, mas grande, o que torna difícil empacotá-lo em vetores de vírus adeno-associados (AAV) amplamente usados para entregar terapias gênicas. Além disso, ele reconhece apenas pequenas etiquetas de DNA, chamadas PAMs, na forma NGG. Essas limitações deixam muitas mutações causadoras de doenças fora de alcance. Um primo menor, SaCas9 de Staphylococcus aureus, cabe confortavelmente dentro de AAV e corta DNA de forma eficiente, mas exige uma sequência PAM mais longa e rara, reduzindo fortemente o número de locais editáveis. Tentativas de afrouxar essas regras de PAM em várias versões de Cas9 frequentemente criaram um trade-off: mais alvos, mas mais danos fora de alvo.
Engenharia de um editor gênico mais amplo e mais seguro
Usando conhecimento estrutural detalhado da SaCas9, os autores substituíram sistematicamente aminoácidos que fazem contatos diretos e específicos com letras da sequência PAM. Em seguida, introduziram novos resíduos carregados positivamente que seguram a coluna vertebral do DNA de forma mais geral. Isso produziu uma variante chamada SaCas9-NNG, que reconhece PAMs simples NNG em vez do padrão mais restrito NNGRRT, ampliando muito o número de possíveis locais de edição. Ajustes adicionais removeram um confronto sutil que havia enfraquecido a atividade em algumas sequências. Em reações em tubo de ensaio e em células humanas, SaCas9-NNG cortou ou reescreveu DNA de forma eficiente em um amplo painel de sítios NNG, especialmente aqueles terminando em C ou T que a enzima original não alcançava. Em muitos alvos, seu desempenho igualou ou superou outros editores “com PAM relaxado” como SpRY, SpG e iGeoCas9.
Tornando as edições mais confiáveis
Expandir onde a Cas9 pode cortar levanta uma questão crítica: ela ainda consegue evitar os lugares errados? Para responder, a equipe projetou uma versão de alta fidelidade enfraquecendo certos contatos que ajudam a proteína a tolerar incompatibilidades entre seu RNA guia e o DNA. Duas substituições-chave em uma região que estabiliza a extremidade distante do híbrido RNA–DNA tornaram a enzima menos permissiva a incompatibilidades, particularmente aquelas afastadas do PAM, fonte comum de cortes fora de alvo. Essa variante, chamada eSaCas9-NNG, manteve forte atividade em alvos corretos, mas reduziu drasticamente cortes em alvos imperfeitos. Comparações em células humanas mostraram que ela igualou ou superou uma SaCas9 de alta fidelidade estabelecida e apresentou menos cortes espúrios que suas versões de menor fidelidade.
Do tubo de ensaio ao tratamento de distúrbios hemorrágicos
Para testar se o editor compacto funcionaria em um organismo vivo, os pesquisadores empacotaram SaCas9-NNG e seu RNA guia em um único vetor AAV8 e o injetaram em camundongos. Mirando o gene humano do fator de coagulação 9 (F9), importante na hemofilia B, observaram a introdução eficiente de pequenas alterações no DNA (indels) em sítios NNG no fígado, incluindo locais que a SaCas9 padrão não conseguia acessar. Eles também criaram versões de edição de base que trocam uma única letra do DNA sem cortar a fita. Em modelos de camundongo portadores de mutações humanas de hemofilia B, o editor de base de adenina construído a partir de SaCas9-NNG corrigiu mudanças causadoras de doença tanto em um PAM clássico quanto em um anteriormente inacessível. Animais tratados mostraram aumentos substanciais na atividade do fator de coagulação no sangue, indicando resgate funcional.
Observando a máquina molecular em ação
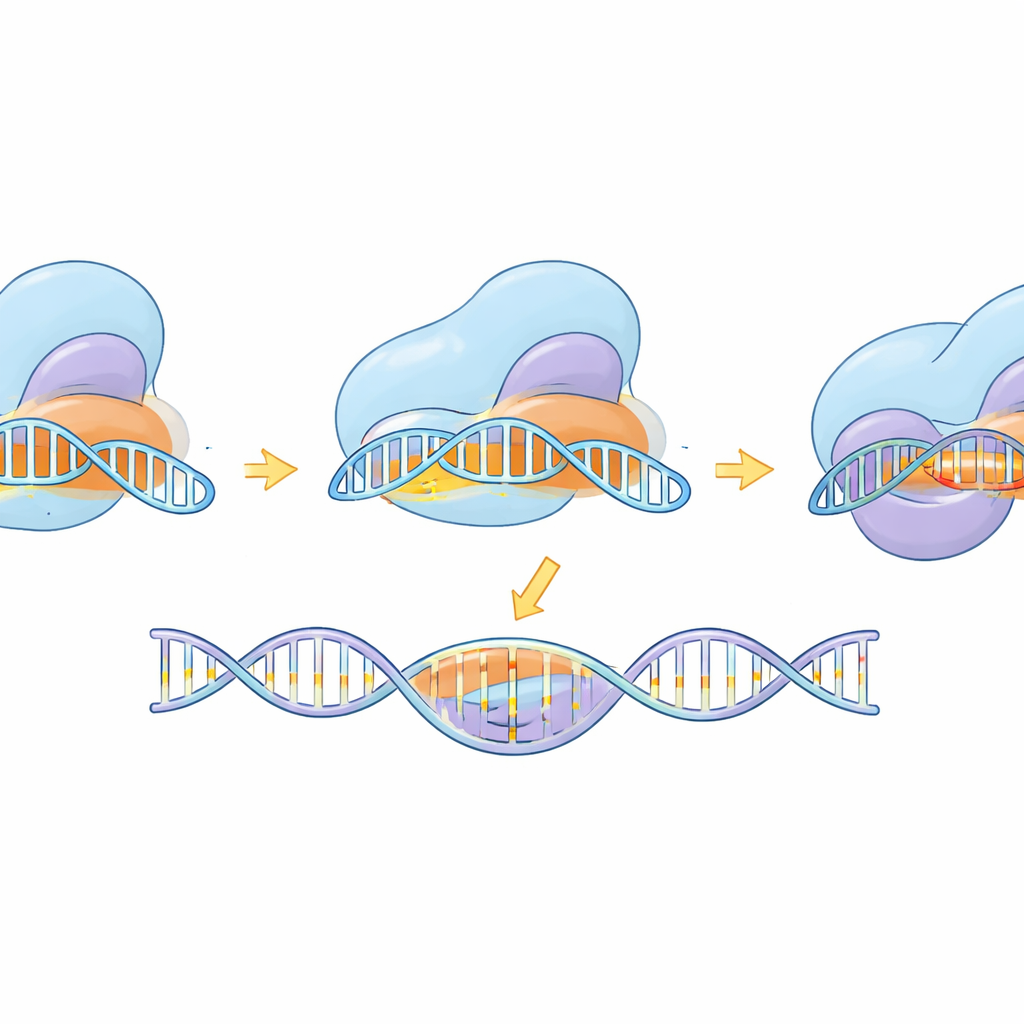
Além da construção da ferramenta, o estudo usou crio-microscopia eletrônica para capturar eSaCas9-NNG em múltiplos instantâneos ao longo de seu ciclo de trabalho—antes de ligar ao DNA, enquanto testa sítios potenciais, durante emparelhamento parcial com o alvo, e na forma totalmente ativada pronta para cortar. Essas estruturas revelam como a enzima primeiro se fixa em uma etiqueta NNG compatível e então gradualmente forma um híbrido helicoidal RNA–DNA. Só quando a hélice é longa e corretamente pareada é que domínios internos se movem para a posição e alinham os centros de corte em ambas as fitas de DNA. As mutações projetadas que melhoraram a especificidade mostraram desestabilizar a ligação a DNA distorcido e incompatível na extremidade distante da hélice, favorecendo a liberação em vez de um corte errado. A comparação com uma variante relacionada e mais flexível, SpCas9, mostra que, apesar de formas diferentes, ambas seguem uma lógica compartilhada: pareamento completo e preciso de bases é requerido para destravar o movimento final de corte.
O que isso significa para futuras terapias gênicas
Para não especialistas, a mensagem central é que os autores criaram uma ferramenta de edição gênica menor, mais versátil e mais cuidadosa. eSaCas9-NNG pode mirar uma fração muito maior do genoma do que a SaCas9 original, mantendo alta precisão, e é compacta o suficiente para ser entregue em um único pacote AAV—um requisito chave para muitas terapias in vivo. Seu sucesso em corrigir defeitos de coagulação em modelos murinos de hemofilia B, juntamente com insights estruturais detalhados sobre como funciona e evita erros, posiciona essa enzima como uma base promissora para tratamentos de próxima geração e para refinamentos futuros, como editores de base e prime ainda mais precisos.
Citação: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Palavras-chave: CRISPR, terapia gênica, Cas9, edição de base, hemofilia B