Clear Sky Science · ru
Разработка компактного высокоточного варианта Cas9 из Staphylococcus aureus с расширенным диапазоном мишеней и механистическими сведениями об его активации
Меньше «ножниц» для исправления дефектных генов
Инструменты редактирования генома, такие как CRISPR-Cas9, обещают лечение наследственных заболеваний, но самые популярные варианты громоздки и могут случайно разрезать не тот участок ДНК. В этом исследовании представлен компактный, высокоточный «нож» для ДНК на основе фермента из Staphylococcus aureus, перестроенный так, чтобы достигать значительно большего числа позиций в геноме при сохранении точности разреза. Поскольку он достаточно мал, чтобы поместиться в распространённый вирусный носитель для генной терапии, и эффективно работает как в клетках, так и в мышах, он может приблизить более безопасную рекомпозицию ДНК к клиническому применению.
Почему важны размер и точность
Классический рабочий инструмент редактирования генома, SpCas9 из Streptococcus pyogenes, мощный, но большой, что затрудняет его упаковку в векторы адено-ассоциированного вируса (AAV), широко используемые для доставки генных терапий. Он также распознаёт только короткие ДНК-метки PAM формата NGG. Эти ограничения оставляют многие болезнетворные мутации недоступными. Его более маленький родственник, SaCas9 из Staphylococcus aureus, помещается в AAV и эффективно разрезает ДНК, но требует более длинной и редкой последовательности PAM, что резко сокращает число редактируемых сайтов. Попытки ослабить требования к PAM в различных версиях Cas9 часто создавали компромисс: больше мишеней — но больше побочных разрезов.
Создание более широкого и более безопасного редактора генов
Используя детальные структурные данные о SaCas9, авторы систематически заменяли аминокислоты, которые обеспечивают непосредственные, букво-специфичные контакты с PAM-последовательностью. Затем они ввели новые положительно заряженные остатки, которые более обобщённо захватывают фосфодиэфирный остов ДНК. В результате получился вариант, названный SaCas9-NNG, который распознаёт простые PAM формата NNG вместо более строгого NNGRRT, что значительно увеличивает число потенциальных сайтов редактирования. Дальнейшая тонкая настройка устранила небольшой конфликт, ослаблявший активность в некоторых последовательностях. В пробирочных реакциях и в человеческих клетках SaCas9-NNG эффективно разрезал или переписывал ДНК на широком наборе NNG-сайтов, особенно на тех, которые оканчивались на C или T и были недоступны для исходного фермента. По многим целям его эффективность сопоставима или превосходит другие «PAM-ослабленные» редакторы, такие как SpRY, SpG и iGeoCas9.
Повышение доверия к внесённым изменениям
Расширение диапазона разрезов Cas9 ставит критический вопрос: может ли он по-прежнему избегать неверных мест? Чтобы ответить на это, команда создала высокоточный вариант, ослабив некоторые контакты, которые помогают белку терпимо относиться к несоответствиям между направляющей РНК и ДНК. Две ключевые замены в участке, стабилизирующем дальний конец RNA–DNA-спирали, сделали фермент менее снисходительным к несоответствиям, особенно к тем, которые удалены от PAM и часто становятся источником побочных разрезов. Этот вариант, названный eSaCas9-NNG, сохранил высокую активность по правильным мишеням, но резко снизил разрезы по неточным. Сравнения в человеческих клетках показали, что он сопоставим или превосходит уже известный высокоточный SaCas9 и имеет меньше спонтанных разрезов, чем его менее точные собратья.
От пробирки до лечения кровоточащих расстройств
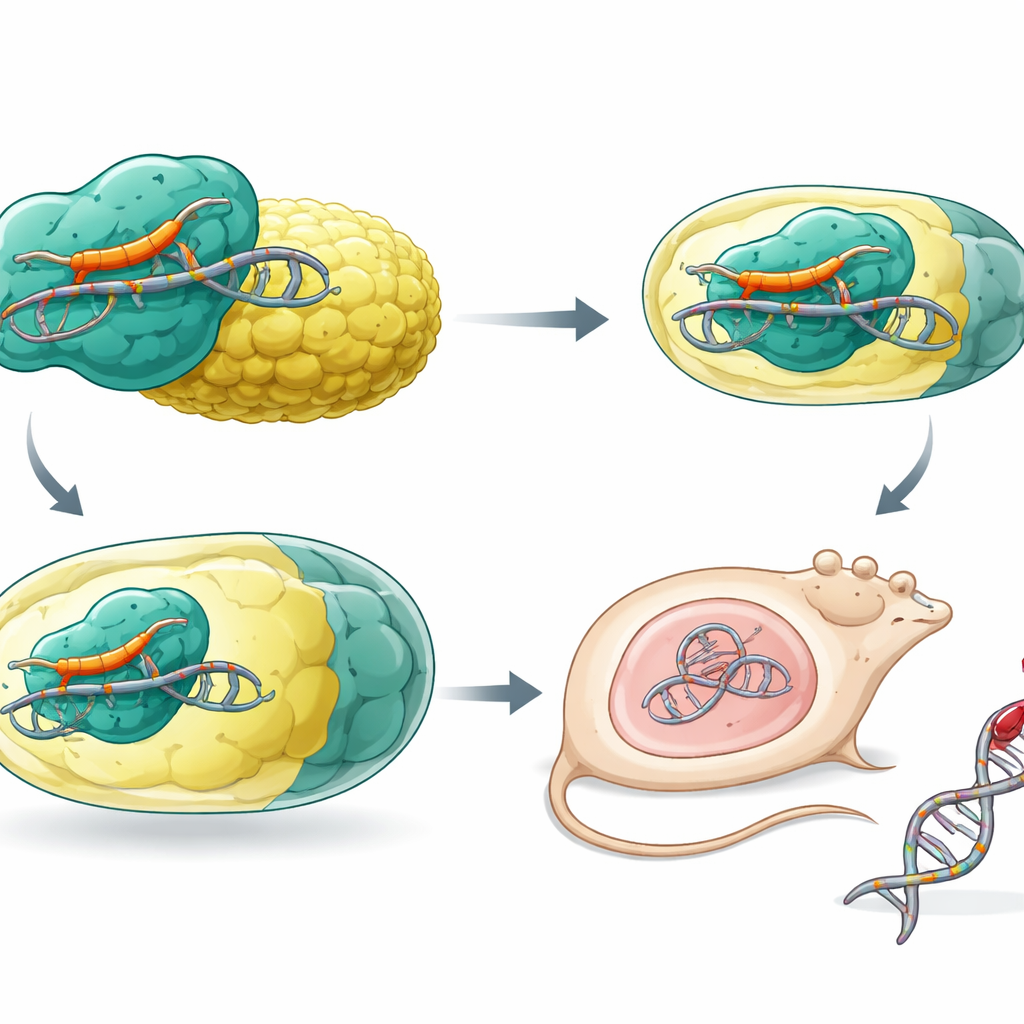
Чтобы проверить, может ли компактный редактор работать в живом организме, исследователи упаковали SaCas9-NNG и его направляющую РНК в единый вектор AAV8 и ввели его мышам. Нацеливаясь на ген человеческого фактора свертывания IX (F9), важный при гемофилии B, они наблюдали эффективное внесение небольших изменений ДНК (инделов) в NNG-сайтах в печени, включая сайты, недоступные для стандартного SaCas9. Также были созданы версии для базового редактирования, которые заменяют одну букву ДНК без разрезания цепи. В модельных мышах с человеческими мутациями гемофилии B адениновые базовые редакторы на основе SaCas9-NNG исправляли болезнетворные изменения как в классическом PAM, так и в ранее недоступном. Лечёные животные демонстрировали существенное увеличение активности фактора свертывания в крови, что свидетельствует о функциональном восстановлении.
Наблюдение за молекулярной машиной в действии
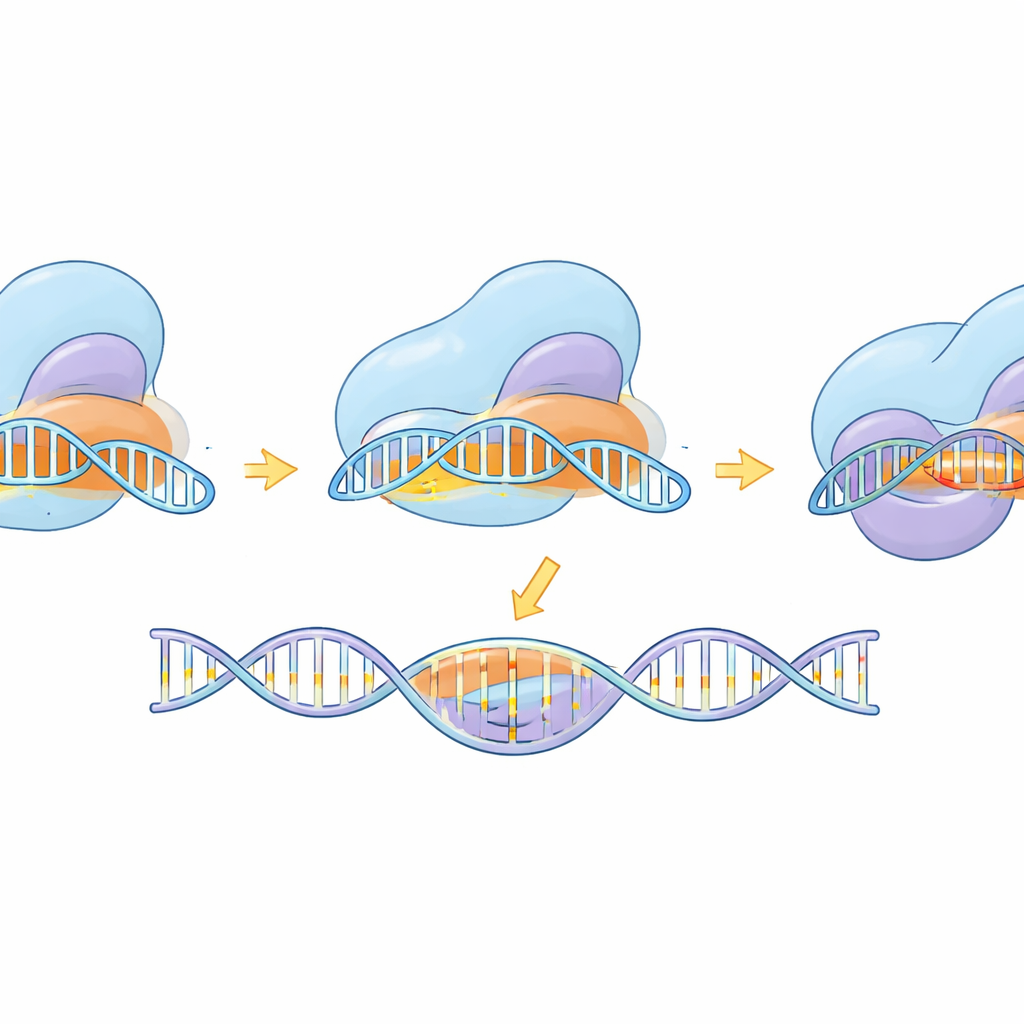
Помимо создания инструмента, исследование использовало крио-электронную микроскопию, чтобы зафиксировать eSaCas9-NNG в нескольких состояниях его рабочего цикла — до связывания с ДНК, при распознавании потенциальных сайтов, во время частичного спаривания с мишенью и в полностью активированной форме, готовой к разрезанию. Эти структуры показывают, как фермент сначала цепляется за совместимый NNG-тег, затем постепенно формирует RNA–DNA-гибридную спираль. Только когда спираль становится длинной и правильно спаренной, внутренние домены совершают поворот и выравнивают центры разреза по обеим цепям ДНК. Инженерные замены, повышающие специфичность, выявлены как ослабляющие связывание с искажённой, несопадающей ДНК на дальнем конце спирали, что стимулирует отпускание вместо ошибочного разреза. Сравнение с родственным, более гибким вариантом SpCas9 показывает, что, несмотря на разные формы, оба следуют общей логике: полное и точное спаривание оснований требуется, чтобы «разблокировать» финальное режущее движение.
Что это означает для будущих генных терапий
Для неспециалистов главный вывод таков: авторы создали меньший, более универсальный и более осторожный инструмент для редактирования генома. eSaCas9-NNG может нацеливаться на значительно большую долю генома, чем исходный SaCas9, при этом сохраняет высокую точность и достаточно компактен, чтобы доставляться в одном пакете AAV — ключевом требовании для многих терапий in vivo. Его успех в исправлении дефектов свертывания крови в моделях мышей с гемофилией B, вместе с детальными структурными сведениями о том, как он работает и избегает ошибок, делает этот фермент многообещающей основой для следующего поколения лечебных подходов и для дальнейших улучшений, таких как ещё более точные базовые и prime‑редакторы.
Цитирование: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Ключевые слова: CRISPR, генная терапия, Cas9, базовое редактирование, гемофилия B