Clear Sky Science · de
Entwicklung einer kompakten, hochpräzisen Staphylococcus aureus Cas9-Variante mit erweitertem Zielbereich und mechanistischen Einblicken in ihre Aktivierung
Kleinere Scheren zum Reparieren fehlerhafter Gene
Gene-Editing-Werkzeuge wie CRISPR-Cas9 versprechen Behandlungen für vererbte Krankheiten, doch die gebräuchlichsten Varianten sind sperrig und können versehentlich die falschen DNA-Stellen zerschneiden. Diese Studie stellt eine kompakte, hochpräzise DNA-„Schere“ vor, basierend auf einem Enzym von Staphylococcus aureus, das neu gestaltet wurde, um viel mehr Stellen im Genom zu erreichen und gleichzeitig präzise zu schneiden. Da sie klein genug ist, um in ein gängiges Gentherapie-Virus zu passen, und sowohl in Zellen als auch in Mäusen gut wirkt, könnte sie sicherere DNA-Reparaturen näher an die klinische Anwendung bringen.
Warum Größe und Genauigkeit wichtig sind
Der ursprüngliche Arbeitspferd des Genom-Editings, SpCas9, stammt von Streptococcus pyogenes. Er ist leistungsfähig, aber groß, was es schwierig macht, ihn in Adeno-assoziierte Virus(Vektor)en (AAV) zu verpacken, die häufig zur Verabreichung von Gentherapien genutzt werden. Zudem erkennt er nur kurze DNA-Markierungen, sogenannte PAMs, der Form NGG. Diese Einschränkungen lassen viele krankheitsverursachende Mutationen unerreichbar. Ein kleinerer Verwandter, SaCas9 von Staphylococcus aureus, passt bequem in AAV und schneidet effizient, verlangt jedoch eine längere und seltenere PAM-Sequenz, was die Anzahl editierbarer Stellen stark einschränkt. Versuche, diese PAM-Regeln in verschiedenen Cas9-Versionen zu lockern, führten oft zu einem Kompromiss: mehr Zielstellen, aber auch mehr Off-Target-Schäden.
Entwicklung eines breiteren, sichereren Gen-Editors
Unter Verwendung detaillierter struktureller Kenntnisse von SaCas9 ersetzten die Autoren systematisch Aminosäuren, die direkte, buchstabenspezifische Kontakte mit der PAM-Sequenz herstellen. Anschließend führten sie neue positiv geladene Reste ein, die den DNA-Rückgrat allgemein stärker greifen. Das ergab eine Variante namens SaCas9-NNG, die einfache NNG-PAMs erkennt statt des restriktiveren NNGRRT-Musters und damit die Anzahl potenzieller Editierstellen erheblich vergrößert. Weitere Feinabstimmungen beseitigten eine subtile sterische Störung, die die Aktivität an einigen Sequenzen geschwächt hatte. In Reaktionen im Reagenzglas und in menschlichen Zellen schnitt bzw. schrieb SaCas9-NNG DNA effizient an einer breiten Palette von NNG-Stellen um, insbesondere an solchen, die auf C oder T enden und die ursprüngliche Enzymvariante nicht erreichen konnte. Über viele Ziele hinweg entsprach seine Leistung oder übertraf andere „PAM-gelockerte“ Editoren wie SpRY, SpG und iGeoCas9.
Die Editierungen vertrauenswürdiger machen
Die Ausweitung der Schnittstellen von Cas9 wirft eine zentrale Frage auf: Kann es weiterhin falsche Stellen vermeiden? Um dies zu klären, entwickelten die Forscher eine hochpräzise Variante, indem sie bestimmte Kontakte abschwächten, die dem Protein erlauben, Ungenauigkeiten zwischen seiner Guide-RNA und der DNA zu tolerieren. Zwei Schlüsselsubstitutionen in einer Region, die das entfernte Ende der RNA–DNA-Helix stabilisiert, machten das Enzym weniger nachsichtig gegenüber Fehlpaarungen, insbesondere solchen, die weit vom PAM entfernt sind und eine häufige Quelle von Off-Target-Schnitten darstellen. Diese Variante, eSaCas9-NNG genannt, behielt starke Aktivität an korrekten Zielen bei, reduzierte aber deutlich das Schneiden an unvollkommenen Stellen. Vergleiche in menschlichen Zellen zeigten, dass sie einer etablierten hochpräzisen SaCas9-Variante ebenbürtig war oder diese übertraf und weniger unerwünschte Schnitte als ihre weniger präzisen Verwandten aufwies.
Vom Reagenzglas zur Behandlung von Blutungsstörungen
Um zu prüfen, ob der kompakte Editor in einem lebenden Organismus funktionieren kann, verpackten die Forschenden SaCas9-NNG und seine Guide-RNA in einen einzelnen AAV8-Vektor und injizierten ihn in Mäuse. Mit Ziel auf das menschliche Gen für den Gerinnungsfaktor 9 (F9), das bei Hämophilie B wichtig ist, beobachteten sie effiziente Einführung kleiner DNA-Veränderungen (Indels) an NNG-Stellen in der Leber, einschließlich Stellen, die mit standardmäßigem SaCas9 nicht erreichbar waren. Sie erzeugten außerdem Base-Editing-Versionen, die einen einzelnen DNA-Buchstaben austauschen, ohne den Strang zu zerschneiden. In Mausmodellen mit menschlichen Hämophilie-B-Mutationen korrigierte der auf SaCas9-NNG aufgebaute Adenin-Base-Editor krankheitsverursachende Veränderungen sowohl an einem klassischen PAM als auch an einer zuvor unzugänglichen Stelle. Die behandelten Tiere zeigten deutliche Steigerungen der Gerinnungsfaktor-Aktivität im Blut, was auf eine funktionelle Wiederherstellung hindeutet.
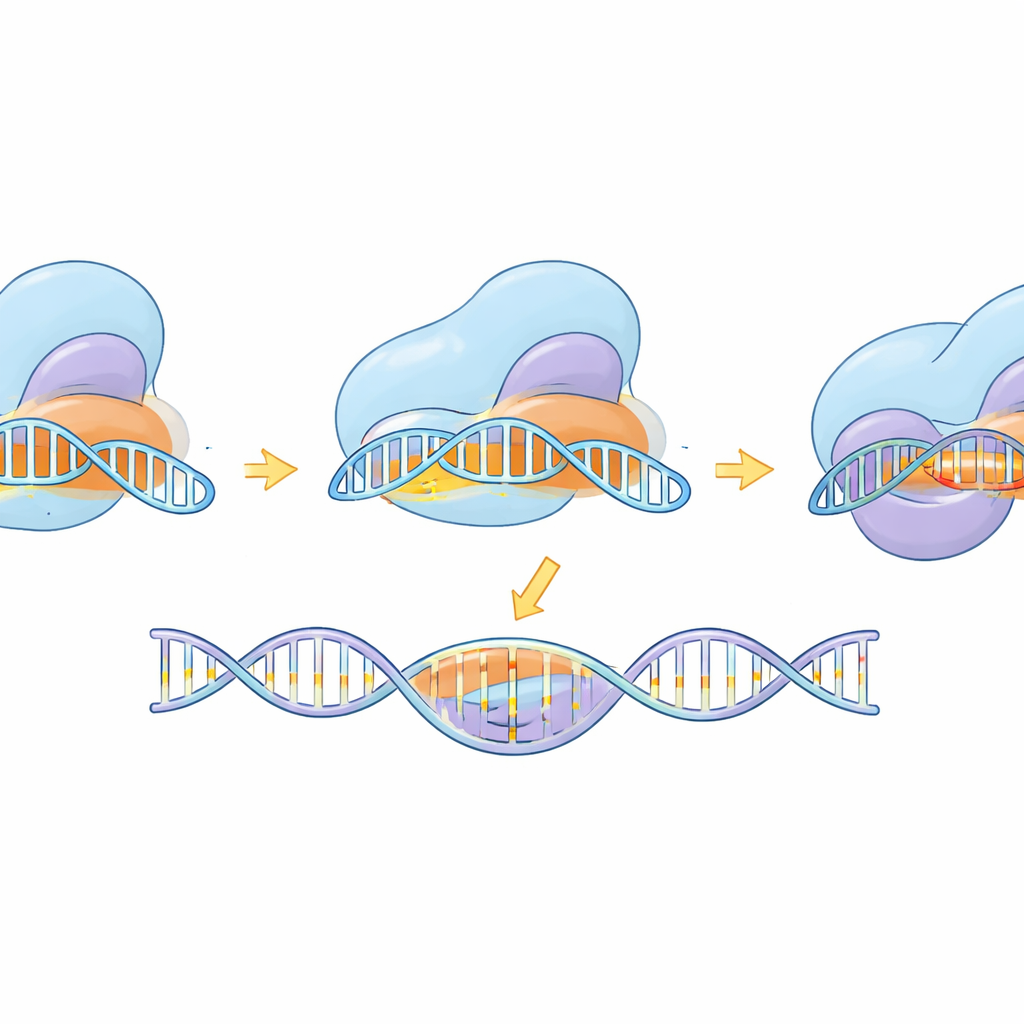
Die molekulare Maschine in Aktion beobachten
Über den Werkzeugbau hinaus nutzte die Studie Kryo-Elektronenmikroskopie, um eSaCas9-NNG in mehreren Schnappschüssen entlang seines Arbeitszyklus einzufangen—vor dem DNA-Binden, beim Testen potenzieller Stellen, während teilweiser Paarung mit dem Ziel und in der voll aktivierten Form, bereit zum Schneiden. Diese Strukturen zeigen, wie das Enzym zunächst an ein kompatibles NNG-Tag andockt und dann schrittweise eine RNA–DNA-Hybridhelix ausbildet. Erst wenn die Helix lang und korrekt gepaart ist, schwenken interne Domänen in Position und richten die Schneidezentren auf beiden DNA-Strängen aus. Die ingenieurmäßigen Mutationen, die die Spezifität verbesserten, destabilisierten die Bindung an verzerrte, fehlgepaarte DNA am entfernten Ende der Helix, was die Freisetzung anstelle eines fehlerhaften Schnitts begünstigt. Der Vergleich mit einer verwandten, flexibleren SpCas9-Variante zeigt, dass trotz unterschiedlicher Gestalten beide einer gemeinsamen Logik folgen: Volle, genaue Basenpaarung ist erforderlich, um die finale Schneidebewegung zu entsperren.
Was das für zukünftige Gentherapien bedeutet
Für Nicht-Spezialisten lautet die zentrale Botschaft: Die Autoren haben ein kleineres, vielseitigeres und vorsichtigeres Gen-Editing-Werkzeug entwickelt. eSaCas9-NNG kann einen deutlich größeren Bruchteil des Genoms anvisieren als das ursprüngliche SaCas9, behält dabei hohe Präzision und ist kompakt genug, um in einem einzigen AAV-Paket ausgeliefert zu werden—eine Schlüsselanforderung für viele in vivo-Therapien. Sein Erfolg bei der Korrektur von Gerinnungsdefekten in Hämophilie-B-Mausmodellen, zusammen mit detaillierten strukturellen Einblicken in Funktionsweise und Fehlervermeidung, positioniert dieses Enzym als vielversprechende Grundlage für Therapien der nächsten Generation und für künftige Verfeinerungen wie noch präzisere Base- und Prime-Editoren.
Zitation: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Schlüsselwörter: CRISPR, Gentherapie, Cas9, Base-Editing, Hämophilie B