Clear Sky Science · es
Ingeniería de una variante compacta y de alta fidelidad de Cas9 de Staphylococcus aureus con un rango de orientación más amplio e ideas mecanísticas sobre su activación
Tijeras más pequeñas para reparar genes defectuosos
Las herramientas de edición génica como CRISPR-Cas9 prometen tratamientos para enfermedades hereditarias, pero las versiones más populares son voluminosas y pueden cortar accidentalmente fragmentos equivocados de ADN. Este estudio presenta unas “tijeras” de ADN compactas y muy precisas basadas en una enzima de Staphylococcus aureus, rediseñadas para alcanzar muchos más lugares del genoma manteniendo la precisión. Al ser lo bastante pequeña como para caber en un virus común de terapia génica y funcionar bien tanto en células como en ratones, podría acercar la reparación segura del ADN a aplicaciones médicas reales.
Por qué importan el tamaño y la precisión
El caballo de batalla original de la edición del genoma, SpCas9, procede de Streptococcus pyogenes. Es potente pero grande, lo que dificulta su empaquetado en vectores de virus adenoasociados (AAV) que se usan ampliamente para administrar terapias génicas. Además, solo reconoce etiquetas cortas de ADN, llamadas PAM, de la forma NGG. Estas limitaciones dejan muchas mutaciones causantes de enfermedades fuera de alcance. Un pariente más pequeño, SaCas9 de Staphylococcus aureus, cabe cómodamente dentro de AAV y corta el ADN de manera eficiente, pero exige una secuencia PAM más larga y rara, lo que reduce drásticamente el número de sitios editables. Los intentos por relajar estas reglas de PAM en diversas versiones de Cas9 a menudo crearon un compromiso: más dianas pero más daños fuera de objetivo.
Diseñando un editor génico más amplio y más seguro
Usando un conocimiento estructural detallado de SaCas9, los autores reemplazaron sistemáticamente aminoácidos que hacen contactos directos y específicos con letras de la secuencia PAM. Luego introdujeron nuevos residuos cargados positivamente que sujetan la columna vertebral del ADN de forma más general. Esto produjo una variante llamada SaCas9-NNG, que reconoce PAMs sencillos NNG en lugar del patrón más estricto NNGRRT, ampliando enormemente el número de sitios potenciales de edición. Ajustes adicionales eliminaron un choque sutil que había debilitado la actividad en algunas secuencias. En reacciones de tubo de ensayo y en células humanas, SaCas9-NNG cortó o reescribió el ADN de manera eficiente en una amplia batería de sitios NNG, especialmente aquellos que terminan en C o T que la enzima original no podía tocar. En muchos objetivos, su rendimiento igualó o superó al de otros editores “con PAM relajado” como SpRY, SpG e iGeoCas9.
Haciendo las ediciones más confiables
Ampliar dónde puede cortar Cas9 plantea una pregunta crítica: ¿sigue pudiendo evitar los sitios equivocados? Para abordarlo, el equipo diseñó una versión de alta fidelidad debilitando ciertos contactos que ayudan a la proteína a tolerar desajustes entre su ARN guía y el ADN. Dos sustituciones clave en una región que estabiliza el extremo lejano del híbrido ARN–ADN hicieron la enzima menos permisiva con los desajustes, especialmente aquellos distantes del PAM que son fuente común de cortes fuera de objetivo. Esta variante, llamada eSaCas9-NNG, mantuvo fuerte actividad en dianas correctas pero redujo drásticamente el corte en dianas imperfectas. Comparaciones en células humanas mostraron que igualó o superó a una SaCas9 de alta fidelidad establecida y tuvo menos cortes espurios que sus parientes de menor fidelidad.
Del tubo de ensayo al tratamiento de trastornos hemorrágicos
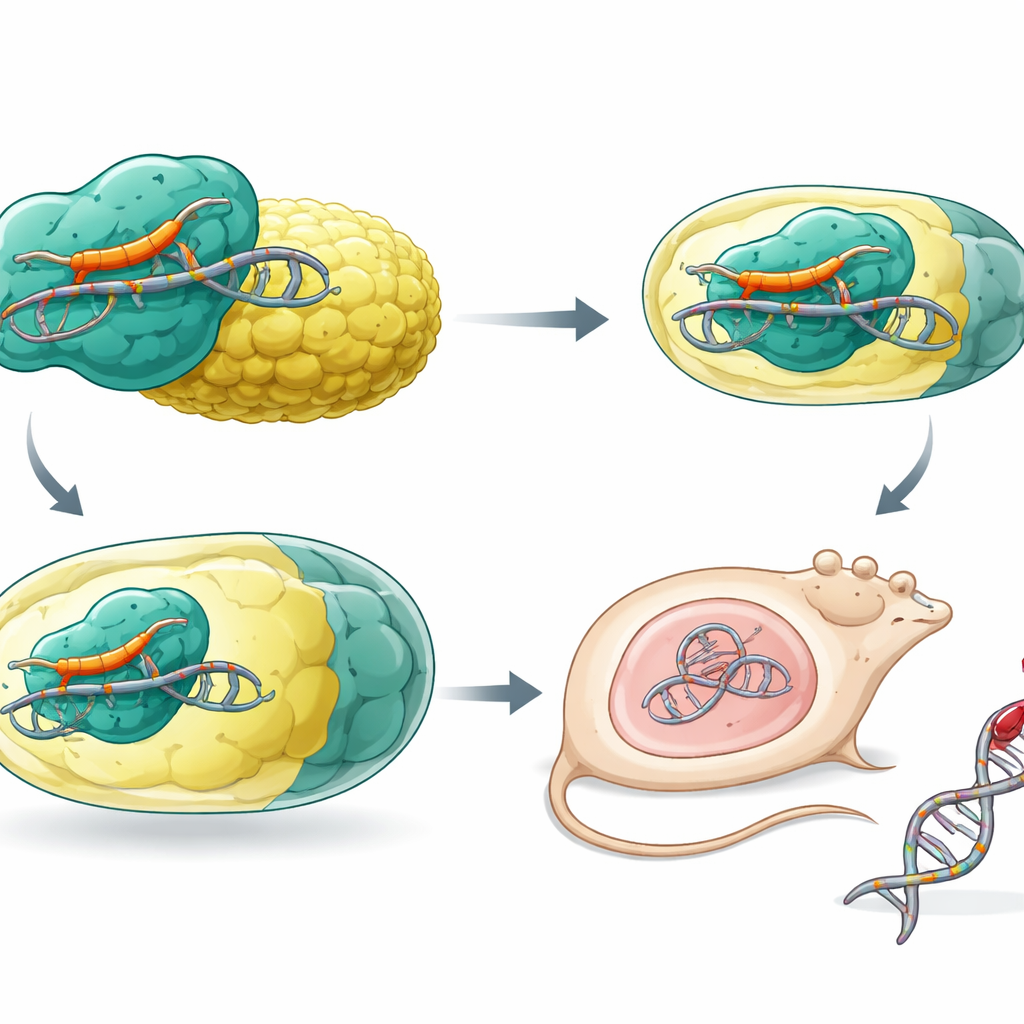
Para probar si el editor compacto podía funcionar dentro de un organismo vivo, los investigadores empaquetaron SaCas9-NNG y su ARN guía en un único vector AAV8 e inyectaron a ratones. Dirigiéndose al gen humano del factor de coagulación 9 (F9), importante en la hemofilia B, observaron la introducción eficiente de pequeños cambios en el ADN (indels) en sitios NNG en el hígado, incluidos sitios que la SaCas9 estándar no podía alcanzar. También crearon versiones de edición de bases que cambian una sola letra del ADN sin cortar la hebra. En modelos de ratón portadores de mutaciones humanas de hemofilia B, el editor de adenina construido a partir de SaCas9-NNG corrigió cambios causantes de la enfermedad tanto en un PAM clásico como en uno previamente inaccesible. Los animales tratados mostraron aumentos sustanciales en la actividad del factor de coagulación en sangre, lo que indica rescate funcional.
Observando la máquina molecular en acción
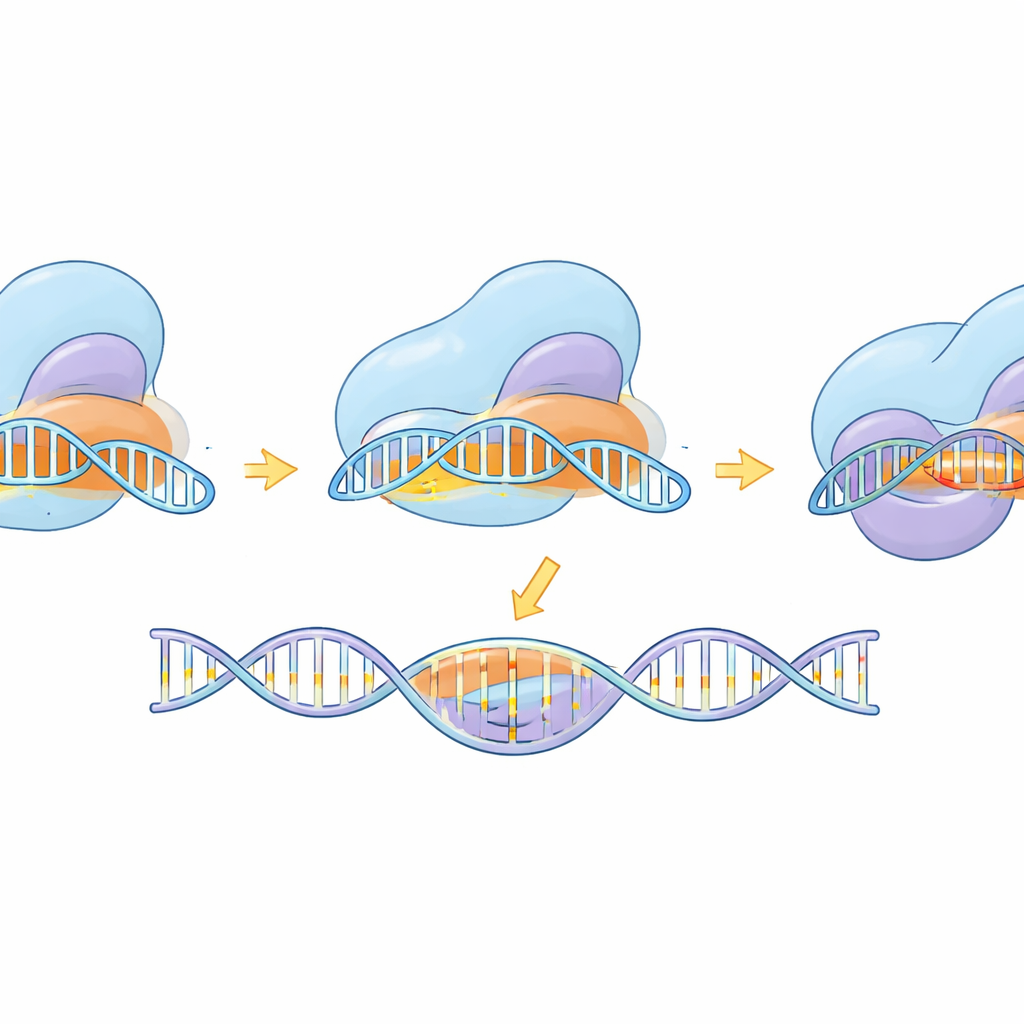
Más allá de la construcción de la herramienta, el estudio utilizó crio-microscopía electrónica para capturar a eSaCas9-NNG en múltiples instantáneas a lo largo de su ciclo de trabajo: antes de unirse al ADN, mientras prueba sitios potenciales, durante el emparejamiento parcial con la diana y en la forma totalmente activada lista para cortar. Estas estructuras revelan cómo la enzima primero se fija a una etiqueta NNG compatible y luego forma gradualmente un híbrido helicoidal ARN–ADN. Solo cuando la hélice es larga y está correctamente emparejada, los dominios internos se desplazan y alinean los centros de corte en ambas hebras del ADN. Las mutaciones diseñadas que mejoraron la especificidad se observaron desestabilizando la unión a ADN distorsionado o con desajustes en el extremo lejano de la hélice, favoreciendo la liberación frente al corte erróneo. La comparación con una variante relacionada y más flexible, SpCas9, muestra que, pese a las diferencias estructurales, ambos siguen una lógica común: un emparejamiento completo y preciso de bases es necesario para desbloquear el movimiento final de corte.
Qué significa esto para futuras terapias génicas
Para no especialistas, el mensaje central es que los autores han diseñado una herramienta de edición génica más pequeña, más versátil y más cuidadosa. eSaCas9-NNG puede dirigirse a una fracción mucho mayor del genoma que la SaCas9 original, a la vez que mantiene alta precisión, y es lo bastante compacta como para entregarse en un único paquete AAV, un requisito clave para muchas terapias in vivo. Su éxito corrigiendo defectos de coagulación en modelos de ratón de hemofilia B, junto con conocimientos estructurales detallados sobre su funcionamiento y cómo evita errores, posiciona a esta enzima como una base prometedora para tratamientos de nueva generación y para refinamientos futuros como editores de bases y prime aún más precisos.
Cita: Omura, S.N., Nakagawa, R., Kajimoto, S. et al. Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation. Nat Commun 17, 3584 (2026). https://doi.org/10.1038/s41467-026-71626-2
Palabras clave: CRISPR, terapia génica, Cas9, edición de bases, hemofilia B