Clear Sky Science · zh
克雷伯菌(Klebsiella pneumoniae)生物膜在体外的快速进化描绘了感染过程中被选择的适应性变化
为何医院里“粘性”细菌重要
许多医院感染并非始于我们的组织,而是在导管、呼吸管和其他医疗器械的塑料或硅胶表面上发生。在这些人工表面上,像克雷伯菌这样的细菌可以形成黏稠的、具有保护作用的群落,称为生物膜,难以清除且对抗生素难以治疗。本研究提出了一个简单却至关重要的问题:这些常见的医院病原体在多大速度和以何种方式进化,以更擅长在类似导管的表面形成生物膜——这对它们致病能力意味着什么?
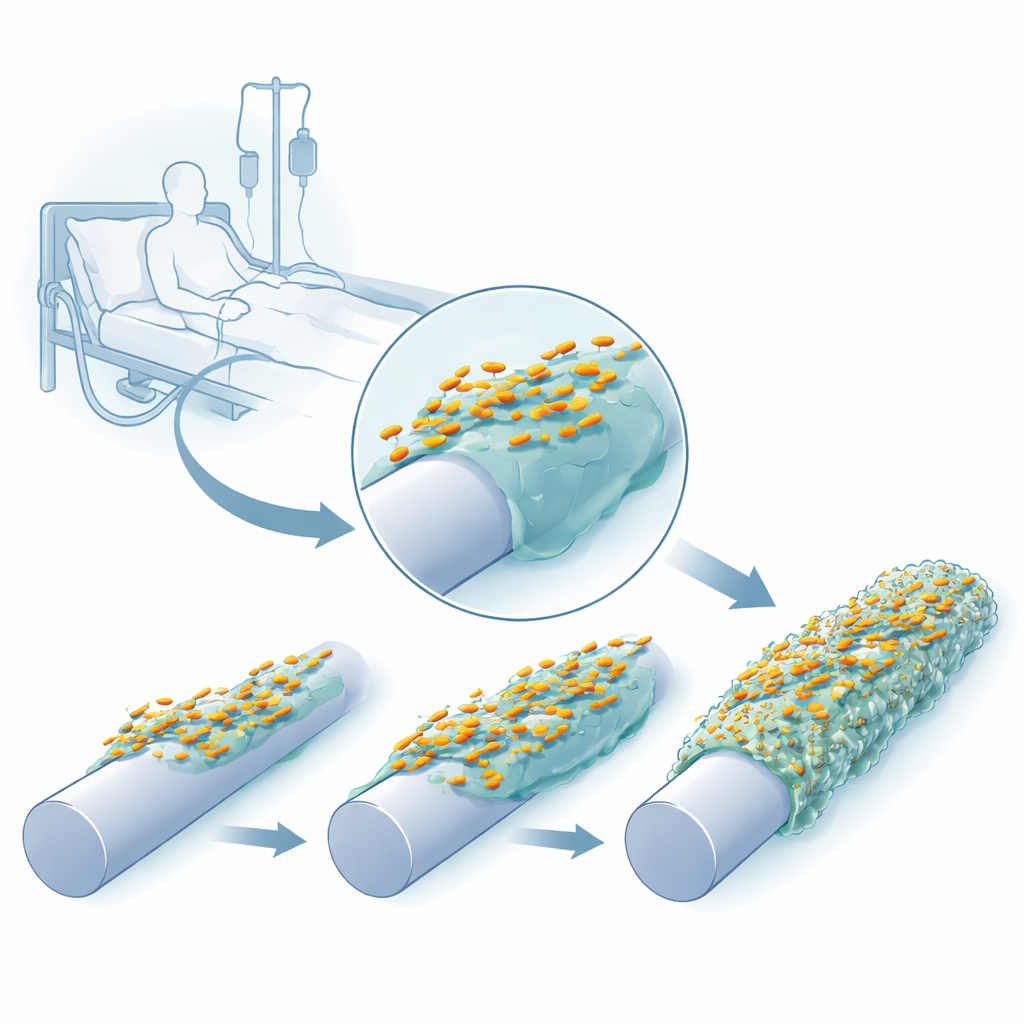
追踪细菌适应塑料表面的过程
研究者在实验室中用一种带销状装置的系统重建了类似导管的环境,其表面可保持裸露状态、涂覆硅胶,或覆盖人体血液蛋白纤维蛋白原(fibrinogen),后者会自然沉积在插入的导管上。他们在这些销上反复培养三株临床分离的K. pneumoniae,将附着的细胞收获后用于下一轮接种。仅经过几轮生长周期,细菌就形成了更厚、更稳固的生物膜,且其在培养基平板上的菌落外观开始发生变化——有的变得异常黏稠和拉丝状,有的变得更透明,或形成皱褶状表面。
变得更“粘”有遗传捷径
通过对一百多个进化克隆的基因组测序,团队表明这些新表型反映了在独立谱系中反复出现的特定遗传改变。许多突变影响了荚膜系统——一种通常帮助细菌躲避免疫攻击的多糖外衣。关键荚膜蛋白Wzc的细微改变产生了超黏稠、高粘性的细胞,使其在硅胶和纤维蛋白原涂层表面上扩展;而其他突变则完全关闭了荚膜生成,产生非黏稠但高度粘附的细胞。第二个主要靶点是毛状表面结构(3型菌毛)末端的尖端蛋白MrkD,它像抓钩一样发挥作用。该蛋白的小结构调整,或调控这些菌毛的信号网络变化,增强了早期附着并改变了生物膜在不同表面上的扩展和聚集方式。
由不同“构件”构建的生物膜
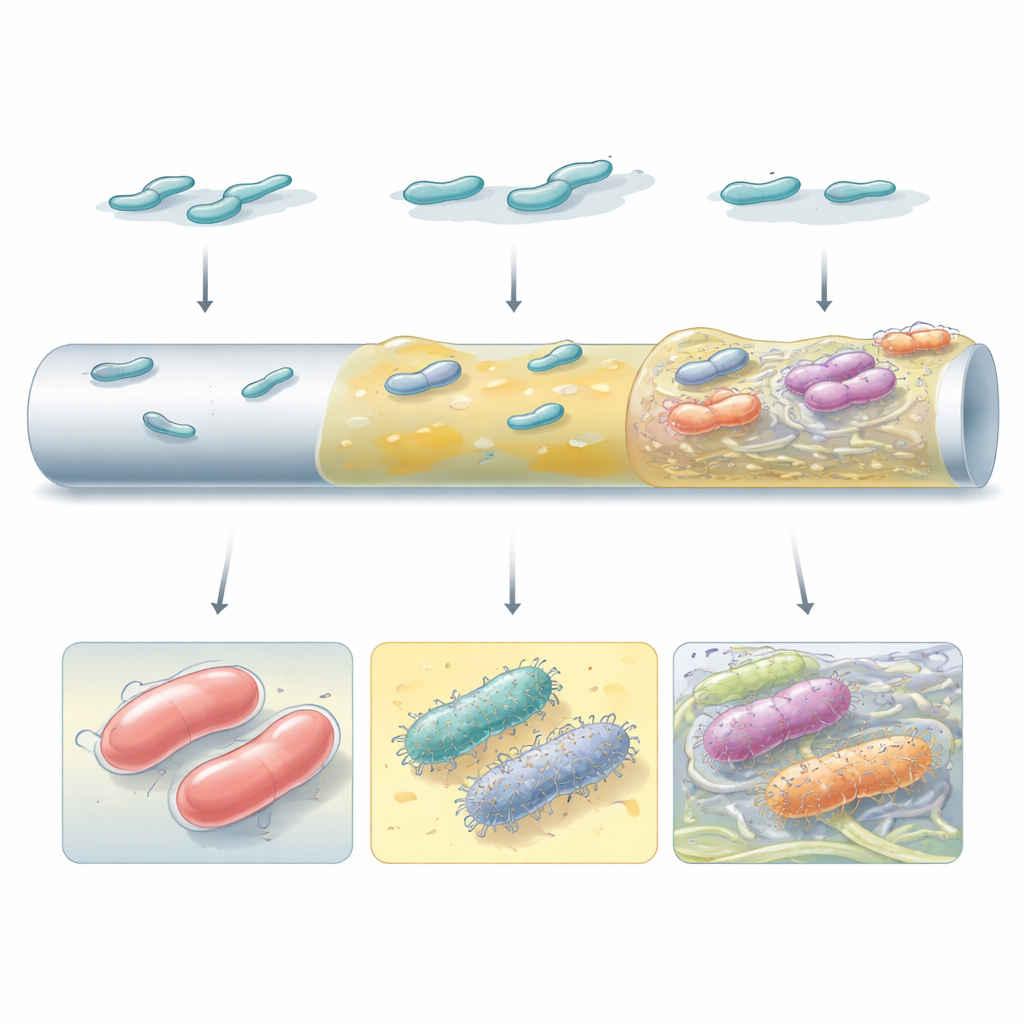
并非所有高效生物膜的外观或功能相同。有些突变体依赖厚实的荚膜物质在类似导管的表面形成光滑、连续的覆盖层。另一些,尤其是失去荚膜或通过小分子c‑di‑GMP重接线内部信号传导的菌株,则产生大量表面纤毛和纤维素纤维,将细胞束缚成离散的簇。电子显微镜显示这些不同策略产生了截然不同的结构:从均匀的粘液层到嵌入纤维基质中的片状、塔状聚集体。哪种策略占优取决于细菌株背景和表面类型,这强调了基因背景与局部环境共同塑造生物膜的进化路径。
“停留”与“致命”之间的权衡
成为更好的生物膜形成者也伴随着隐藏的代价。当以游离游动的形式在人体血清中培养时,无荚膜突变体和超黏Wzc变体更容易被补体系统——我们固有免疫的重要一环——杀死。然而一旦组织成生物膜,这些突变体就能免受血清攻击。在用蜡蛾幼虫的感染模型中,一些生物膜增强的突变体致死性降低,而另一些则没有变化甚至提高了毒力。这表明“更多生物膜”并不等同于“更严重的疾病”;具体的突变类型很关键。
与患者体内发生的情况相呼应
值得注意的是,在实验室中进化出的生物膜专化变体中观察到的许多相同基因——甚至相同的单个碱基变化——也出现在从真实医院暴发事件中收集的K. pneumoniae分离株中,尤其是涉及导管的泌尿道和伤口感染样本。这一高度重合表明,体内的导管表面施加的选择压力与实验室中的类似,持续偏向那些更能粘附、聚集并在器械上存活的变体。与此同时,这些适应有时会削弱细菌引发快速侵袭性疾病的能力,可能使其更倾向于持久存在和慢性感染。理解这些进化权衡有助于在这些适应巩固之前,设计能破坏适合生物膜形成路径的器械和治疗策略。
引用: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
关键词: 克雷伯菌(Klebsiella pneumoniae), 生物膜, 导管相关感染, 细菌进化, 抗生素耐药性