Clear Sky Science · es
Evolución rápida de los biofilms de Klebsiella pneumoniae in vitro que delimita cambios adaptativos seleccionados durante la infección
Por qué importan los microbios adhesivos en los hospitales
Muchas infecciones hospitalarias no se inician en nuestros tejidos, sino en las superficies de plástico y silicona de catéteres, tubos respiratorios y otros dispositivos médicos. En estas superficies artificiales, bacterias como Klebsiella pneumoniae pueden formar comunidades viscosas y protectoras llamadas biofilms, que son difíciles de eliminar y de tratar con antibióticos. Este estudio plantea una pregunta simple pero crucial: ¿con qué rapidez y de qué maneras evolucionan estos gérmenes comunes de hospital para mejorar su capacidad de formar biofilms en superficies tipo catéter, y qué implica eso para su potencial de causar enfermedad?
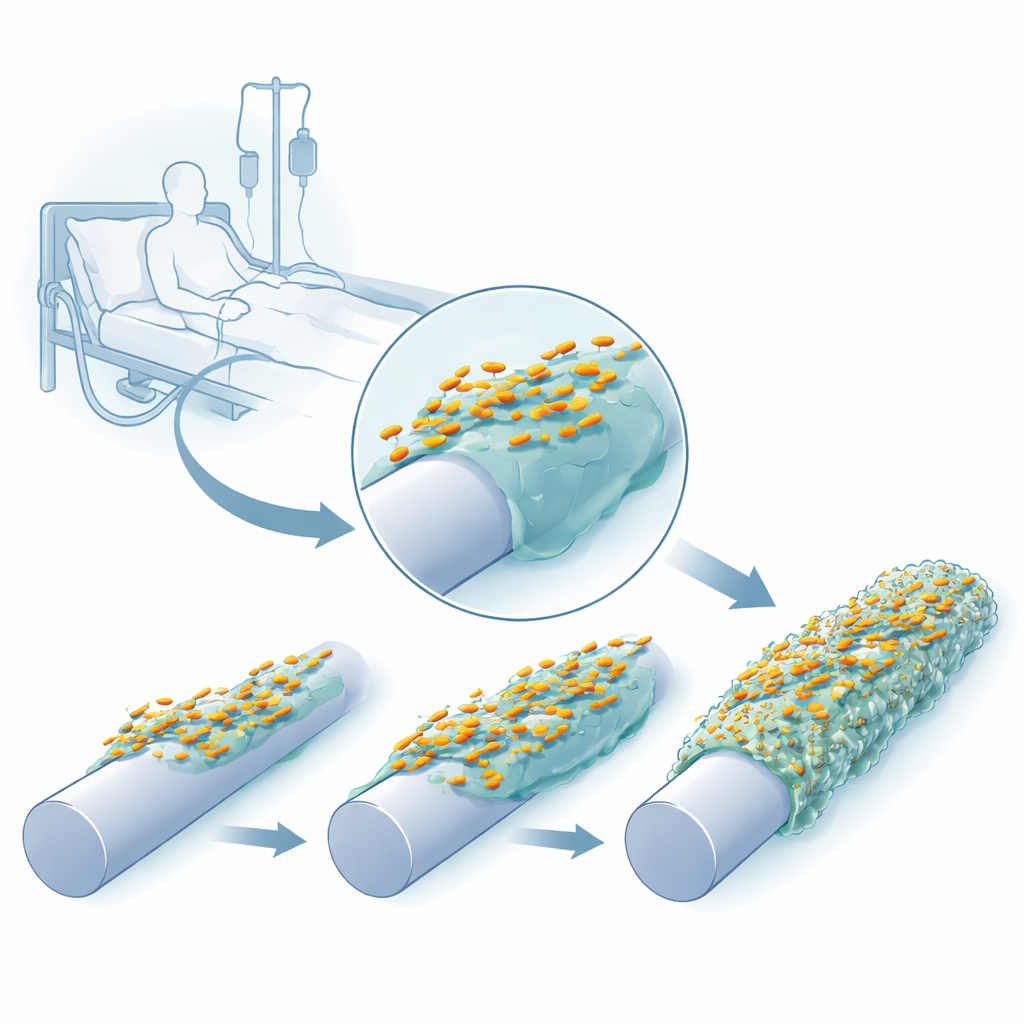
Siguiendo a las bacterias mientras se adaptan al plástico
Los investigadores recrearon en el laboratorio un entorno similar al de un catéter usando un dispositivo de clavijas cuyas superficies podían dejarse al descubierto, recubrirse con silicona o cubrirse con silicona y una proteína sanguínea humana, fibrinógeno, que se deposita de forma natural en los catéteres insertados. Hicieron crecer repetidamente tres cepas clínicas de K. pneumoniae en estas clavijas, cosecharon las células adheridas y las usaron para iniciar el siguiente ciclo. En solo unos pocos ciclos de crecimiento, las bacterias formaron biofilms más gruesos y robustos, y sus colonias en placas de agar empezaron a cambiar de aspecto: algunas se volvieron inusualmente viscosas y filamentosas, otras más translúcidas o con superficies arrugadas.
Atajos genéticos para volverse más adhesivas
Al secuenciar los genomas de más de un centenar de clones evolucionados, el equipo mostró que estas nuevas apariencias reflejaban cambios genéticos específicos que surgieron repetidamente en linajes independientes. Muchas mutaciones afectaron al sistema de cápsula, una cubierta azucarada que normalmente ayuda a las bacterias a evadir el ataque inmune. Alteraciones sutiles en una proteína clave de la cápsula (Wzc) produjeron células hiperviscosas y muy pegajosas que se expandían sobre superficies recubiertas de silicona y fibrinógeno, mientras que otras mutaciones apagaron por completo la producción de cápsula, dando lugar a células no viscosas pero fuertemente adhesivas. Un segundo objetivo importante fue la proteína de la punta (MrkD) de una estructura superficial en forma de pelo (fimbrias tipo 3) que actúa como gancho. Pequeños ajustes estructurales en esta proteína, o cambios en las redes de señalización que regulan estas fimbrias, aumentaron la adhesión temprana y modificaron cómo se extienden y agrupan los biofilms en distintas superficies.
Biofilms construidos a partir de bloques diferentes
No todos los biofilms de alto rendimiento se parecían ni funcionaban igual. Algunos mutantes dependían de una gruesa capa de material capsular para formar capas suaves y continuas sobre la superficie tipo catéter. Otros, especialmente los que habían perdido la cápsula o que habían reconfigurado la señalización interna mediante la pequeña molécula c‑di‑GMP, produjeron abundantes pelos superficiales y fibras de celulosa que ataban a las células en agregados discretos. La microscopía electrónica reveló que estas estrategias distintas dieron arquitecturas muy diferentes: desde recubrimientos uniformes de mucílago hasta agregados parcheados en forma de torre incrustados en una matriz fibrosa. Qué estrategia prevaleció dependió tanto de la cepa bacteriana como del tipo de superficie, subrayando que el trasfondo genético y el entorno local configuran conjuntamente cómo evolucionan los biofilms.
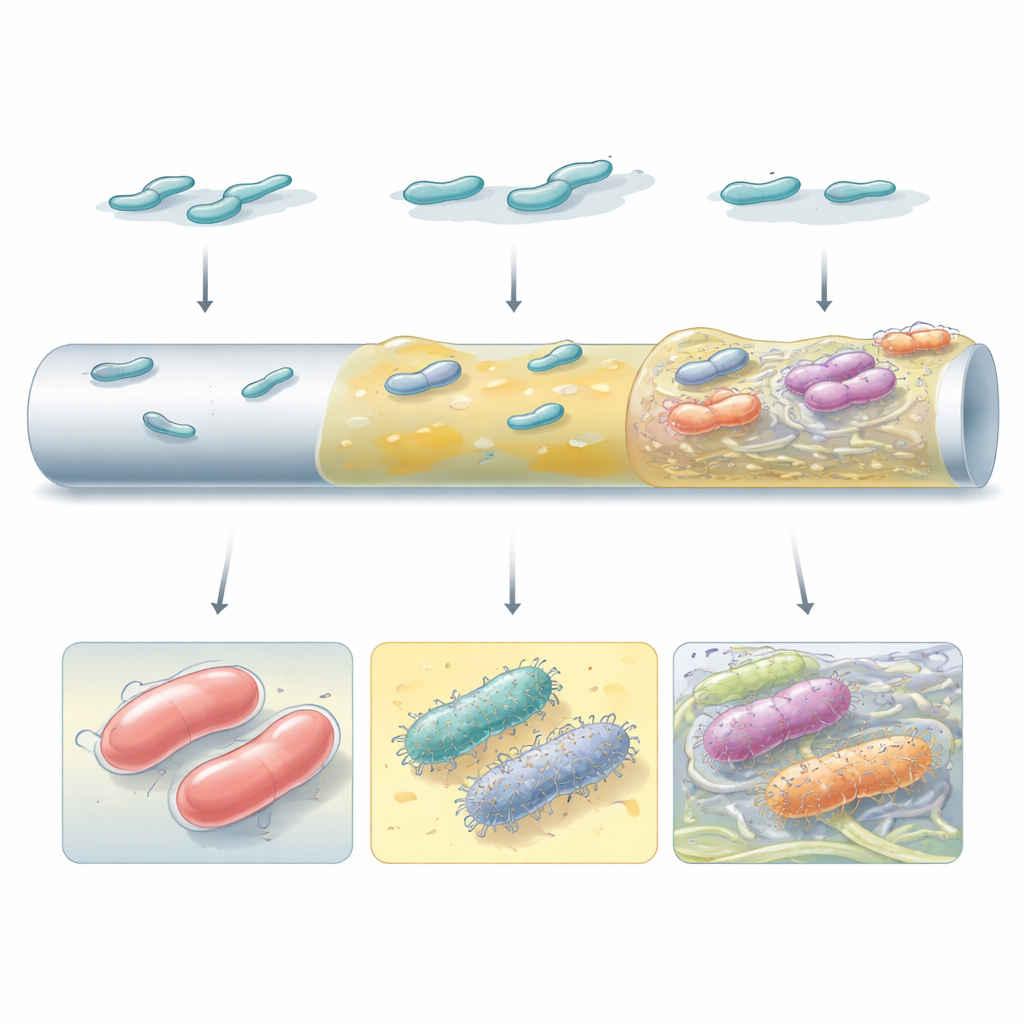
Un intercambio entre permanecer adherido y golpear con fuerza
Mejorar como formador de biofilms conllevó costes ocultos. Al crecer como células libres en suero humano, tanto los mutantes deficientes en cápsula como las variantes hiperviscosas de Wzc fueron mucho más susceptibles al complemento, una rama clave de nuestra inmunidad innata. Sin embargo, una vez organizados en un biofilm, esos mismos mutantes quedaban protegidos frente al ataque del suero. En un modelo de infección con larvas de gusano de cera, algunos mutantes con biofilms mejorados se volvieron menos letales, mientras que otros no cambiaron o incluso aumentaron su virulencia. Esto demuestra que “más biofilm” no equivale automáticamente a “enfermedad más grave”; la mutación exacta importa.
Reflejo de lo que ocurre en los pacientes
De manera llamativa, muchos de los mismos genes—e incluso cambios de una sola letra en el ADN—observados en los especialistas en biofilm evolucionados en el laboratorio también se encontraron en aislados de K. pneumoniae recogidos de pacientes durante un brote hospitalario real, especialmente en infecciones del tracto urinario y de heridas relacionadas con catéteres. Este solapamiento cercano sugiere que las superficies de los catéteres en el cuerpo ejercen presiones selectivas similares a las del laboratorio, favoreciendo de forma constante variantes más aptas para adherirse, agruparse y sobrevivir en dispositivos. Al mismo tiempo, algunas de estas adaptaciones pueden debilitar la capacidad de las bacterias para causar una enfermedad invasiva y rápida, cambiándolas potencialmente hacia la persistencia y la infección crónica. Comprender estos trade‑offs evolutivos puede ayudar a diseñar dispositivos y tratamientos que interrumpan las rutas favorables a los biofilms antes de que se consoliden.
Cita: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Palabras clave: Klebsiella pneumoniae, biofilms, infecciones asociadas a catéteres, evolución bacteriana, resistencia a antibióticos