Clear Sky Science · sv
Snabb evolution av Klebsiella pneumoniae-biofilmer in vitro beskriver adaptiva förändringar som selekteras under infektion
Varför klibbiga sjukhusbakterier spelar roll
Många sjukhusinfektioner börjar inte i våra vävnader utan på plast- och silikonytor på kanyler, andningsslangar och andra medicinska implantat. På dessa konstgjorda ytor kan bakterier som Klebsiella pneumoniae bygga slemiga, skyddande samhällen kallade biofilmer som är svåra att avlägsna och svåra att behandla med antibiotika. Den här studien ställer en enkel men avgörande fråga: hur snabbt, och på vilka sätt, utvecklas dessa vanliga sjukhusbakterier för att bli bättre på att bilda biofilmer på kateterliknande ytor — och vad innebär det för deras förmåga att orsaka sjukdom?
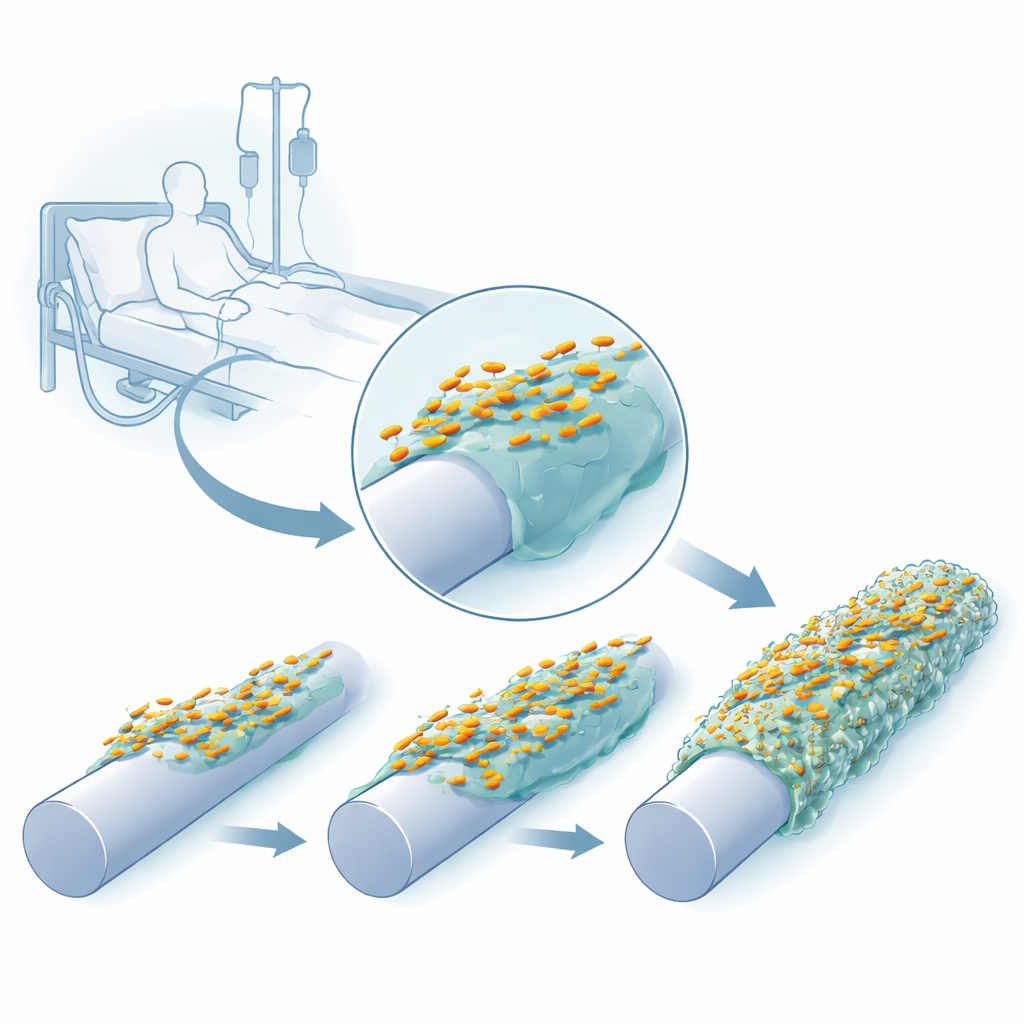
Följa bakterierna när de anpassar sig till plast
Forskarna återskapade en kateterliknande miljö i laboratoriet med en pigg-enhet vars ytor kunde lämnas nakna, täckas med silikon eller beläggas med både silikon och ett mänskligt blodprotein, fibrinogen, som naturligt samlas på insatta katetrar. De odlade upprepade gånger tre kliniska stammar av K. pneumoniae på dessa piggar, skördade de fästa cellerna och använde dem för att starta nästa cykel. Redan efter några få tillväxtcykler bildade bakterierna tjockare, mer robusta biofilmer, och deras kolonier på agarplattor började se annorlunda ut — vissa blev ovanligt slemmiga och trådiga, andra mer genomskinliga eller med veckade ytor.
Genetiska genvägar till ökad klibbighet
Genom att sekvensera genomerna hos över hundra evolverade kloner visade teamet att dessa nya utseenden speglade specifika genetiska förändringar som uppstod upprepade gånger i oberoende linjer. Många mutationer påverkade kapselsystemet, ett sockeraktigt hölje som normalt hjälper bakterien att undvika immunsvar. Subtila förändringar i ett nyckelprotein i kapseln (Wzc) gav hyper-slemmiga, mycket viskösa celler som spred sig längs silikon- och fibrinogenbelagda ytor, medan andra mutationer stängde av kapselproduktionen helt och hållet och gav icke-slemmiga men starkt adhesiva celler. Ett annat huvudmål var toppproteinet (MrkD) i en hår-liknande ytanordning (typ 3 fimbrier) som fungerar som en gripkrok. Små strukturella justeringar i detta protein, eller förändringar i de signalvägar som reglerar dessa fimbrier, ökade tidig vidhäftning och förändrade hur biofilmer spreds och klumpade sig på olika ytor.
Biofilmer byggda av olika byggstenar
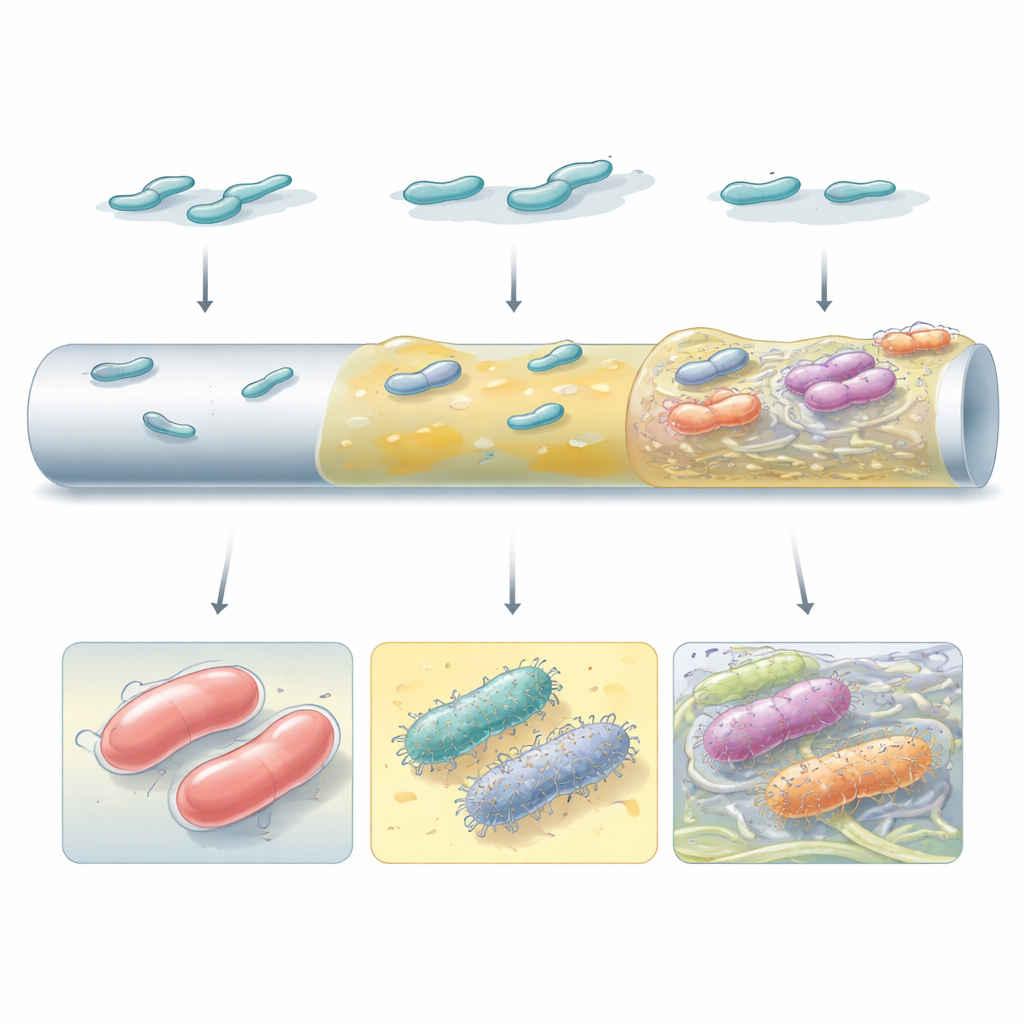
Inte alla högpresterande biofilmer såg likadana ut eller fungerade på samma sätt. Vissa mutanter förlitade sig på tjockt kapselmaterial för att bilda jämna, kontinuerliga skikt över den kateterliknande ytan. Andra, särskilt de som hade förlorat sin kapsel eller omkopplat intern signalering via småmolekylen c-di-GMP, producerade rikligt med ythår och cellulosa-fibrer som band ihop cellerna till diskreta kluster. Elektronmikroskopi visade att dessa olika strategier skapade mycket olika arkitekturer: från uniforma slemmiga höljen till fläckvisa, tornliknande aggregat inbäddade i en fibrös matris. Vilken strategi som segrade berodde både på den bakteriella stammen och yttypen, vilket understryker att genetisk bakgrund och lokal miljö tillsammans formar hur biofilmer utvecklas.
En avvägning mellan att sitta kvar och att slå hårt
Att bli en bättre biofilmbildare kom med dolda kostnader. När de odlades som fritt simmande celler i humant serum var både kapseldefekta mutanter och de hyper-slemmiga Wzc-varianterna mycket lättare att döda med komplement, en viktig del av vårt medfödda immunsystem. Men när de väl organiserades i en biofilm skyddades dessa samma mutanter från serumangrepp. I en infektionsmodell med vaxmottlarver blev vissa biofilmförstärkta mutanter mindre dödliga, medan andra inte förändrades eller till och med ökade i virulens. Det visade att »mer biofilm« inte automatiskt betyder »allvarligare sjukdom«; den exakta mutationen avgör.
Speglat i vad som händer hos patienter
Anmärkningsvärt nog hittades många av samma gener — och till och med identiska enstaka DNA-bokstavsändringar — som setts hos labbevolverade biofilmspecialister också i K. pneumoniae-isolat insamlade från patienter under ett verkligt sjukhusutbrott, särskilt från urinvägs- och sårinfektioner där katetrar var involverade. Denna nära överlappning tyder på att kateterytor i kroppen utövar liknande selektionstryck som de i laboratoriet och stadigt gynnar varianter som är bättre på att klänga, klustra och överleva på implantat. Samtidigt kan några av dessa anpassningar försvaga bakteriernas förmåga att orsaka snabb, invasiv sjukdom, och potentiellt förskjuta dem mot beständighet och kronisk infektion. Att förstå dessa evolutionära avvägningar kan hjälpa till att utforma enheter och behandlingar som stör biofilmvänliga vägar innan de rotar sig.
Citering: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Nyckelord: Klebsiella pneumoniae, biofilmer, kateterassocierade infektioner, bakteriell evolution, antibiotikaresistens