Clear Sky Science · de
Schnelle Evolution von Klebsiella pneumoniae‑Biofilmen in vitro legt adaptive Veränderungen offen, die während von Infektionen selektiert werden
Warum haftende Krankenhauskeime wichtig sind
Viele Krankenhausinfektionen beginnen nicht in unserem Gewebe, sondern auf den Kunststoff‑ und Silikonoberflächen von Kathetern, Beatmungsschläuchen und anderen medizinischen Geräten. Auf diesen künstlichen Oberflächen können Bakterien wie Klebsiella pneumoniae schleimige, schützende Gemeinschaften bilden, sogenannte Biofilme, die schwer zu entfernen sind und sich nur schlecht mit Antibiotika behandeln lassen. Diese Studie stellt eine einfache, aber entscheidende Frage: Wie schnell und auf welche Weise entwickeln sich diese häufigen Krankenhauskeime, um besser Biofilme auf katheterähnlichen Oberflächen zu bilden — und was bedeutet das für ihre Fähigkeit, Erkrankungen zu verursachen?
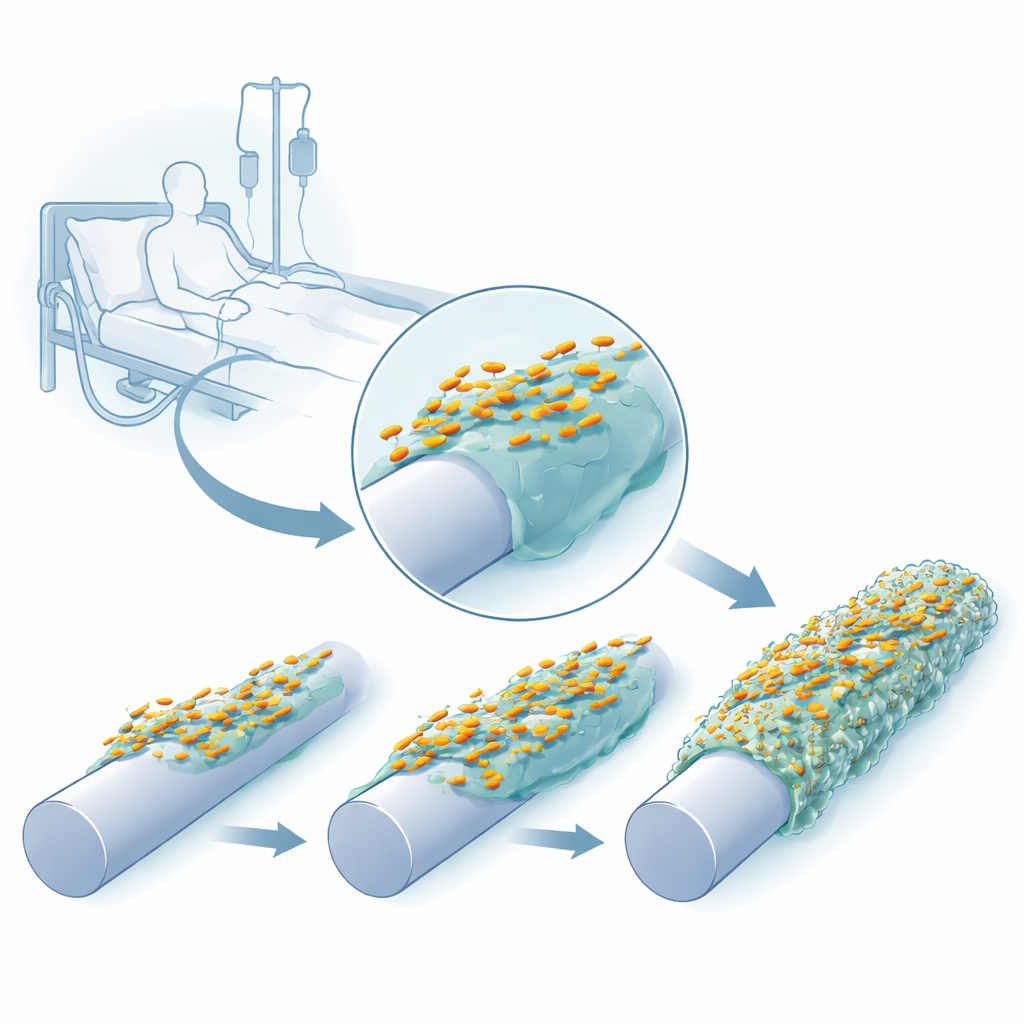
Bakterien verfolgen, während sie sich an Plastik anpassen
Die Forschenden stellten eine katheterähnliche Umgebung im Labor nach, indem sie eine Peg‑Vorrichtung verwendeten, deren Oberflächen unbeschichtet, mit Silikon überzogen oder zusätzlich mit dem menschlichen Blutprotein Fibrinogen bedeckt werden konnten, das sich natürlicherweise auf eingeführten Kathetern ablagert. Sie kultivierten wiederholt drei klinische Stämme von K. pneumoniae auf diesen Pegs, ernteten die angehefteten Zellen und nutzten sie als Ausgangspopulation für den nächsten Zyklus. Bereits nach wenigen Wachstumszyklen bildeten die Bakterien dichtere, robustere Biofilme, und ihre Kolonien auf Agarplatten veränderten ihr Aussehen — einige wurden ungewöhnlich schleimig und fadenförmig, andere fielen durch erhöhte Durchsichtigkeit auf oder zeigten runzelige Oberflächen.
Genetische Abkürzungen zur stärkeren Haftung
Durch die Sequenzierung der Genome von über hundert evolvierten Klonen zeigten die Autorinnen und Autoren, dass diese neuen Erscheinungsbilder spezifische genetische Veränderungen widerspiegeln, die wiederholt in unabhängigen Linien auftraten. Viele Mutationen betrafen das Kapselsystem, eine zuckerhaltige Hülle, die den Bakterien normalerweise hilft, Immunangriffe zu umgehen. Feine Veränderungen in einem Schlüsselprotein der Kapsel (Wzc) erzeugten hyper‑schleimige, hochviskose Zellen, die sich entlang von Silikon‑ und fibrinogenbeschichteten Oberflächen ausbreiten, während andere Mutationen die Kapselproduktion vollständig abschalteten und dadurch nicht‑schleimige, aber stark haftfähige Zellen entstanden. Ein zweites wichtiges Ziel war das Spitzeneiweiß (MrkD) einer haarähnlichen Oberflächenstruktur (Typ‑3‑Fimbrien), die als Greifhaken wirkt. Kleine strukturelle Anpassungen in diesem Protein oder Veränderungen in den Signalnetzwerken, die diese Fimbrien regulieren, stärkten die frühe Anheftung und veränderten, wie Biofilme sich auf unterschiedlichen Oberflächen ausbreiten und verklumpen.
Biofilme aus unterschiedlichen Bausteinen
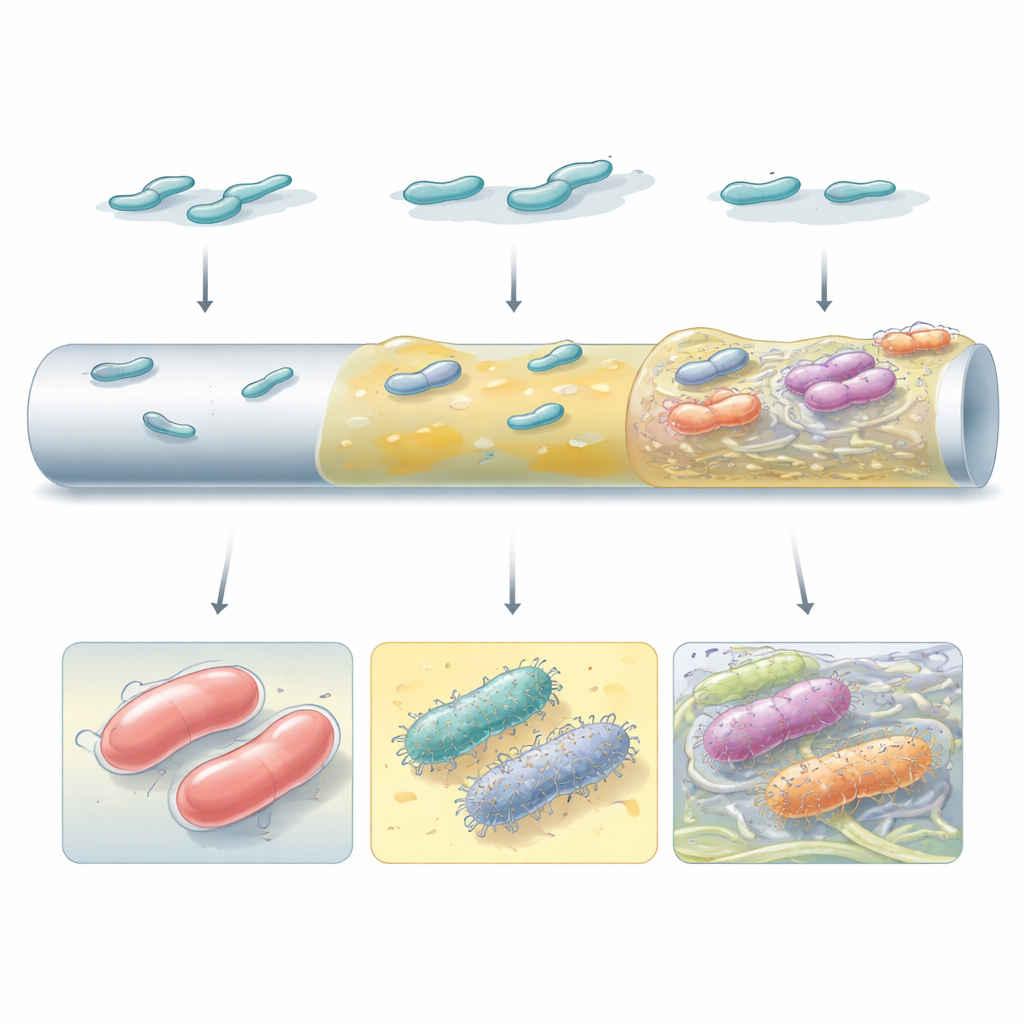
Nicht alle leistungsstarken Biofilme sahen gleich aus oder funktionierten identisch. Einige Mutanten setzten auf dickes Kapselmaterial, um glatte, durchgehende Schichten über der katheterähnlichen Oberfläche zu bilden. Andere, insbesondere solche, die ihre Kapsel verloren hatten oder die interne Signalwege über das kleine Molekül c‑di‑GMP umprogrammiert hatten, produzierten zahlreiche Oberflächenhaare und Zellulosefasern, die Zellen zu diskreten Clustern zusammenbanden. Elektronenmikroskopie zeigte, dass diese unterschiedlichen Strategien sehr verschiedene Architekturen schufen: von einheitlichen Schleimschichten bis zu fleckenhaften, turmartigen Aggregaten in einer faserigen Matrix. Welche Strategie sich durchsetzte, hing sowohl vom bakteriellen Stamm als auch vom Oberflächentyp ab und verdeutlicht, dass genetischer Hintergrund und lokale Umgebung gemeinsam formen, wie Biofilme evolvieren.
Ein Zielkonflikt zwischen Festhalten und Angreifen
Besserer Biofilmaufbau ging mit versteckten Kosten einher. Als frei schwimmende Zellen in menschlichem Serum gewachsen, waren sowohl kapseldefiziente Mutanten als auch die hyper‑schleimigen Wzc‑Varianten deutlich anfälliger für das Komplementsystem, einen zentralen Bestandteil unserer angeborenen Immunabwehr. Sobald sie jedoch in einem Biofilm organisiert waren, waren dieselben Mutanten vor Serumangriffen geschützt. In einem Infektionsmodell mit Wachsmottenlarven wurden einige biofilmverstärkte Mutanten weniger tödlich, während andere keine Veränderung zeigten oder sogar eine erhöhte Virulenz aufwiesen. Das zeigt, dass „mehr Biofilm“ nicht automatisch „schwerere Krankheit“ bedeutet; die genaue Mutation ist entscheidend.
Spiegelbildlich zu dem, was bei Patientinnen und Patienten passiert
Bemerkenswerterweise wurden viele derselben Gene — und sogar identische Einzelbuchstaben‑DNA‑Veränderungen —, die in den im Labor evolvierten Biofilmspezialisten beobachtet wurden, auch in K. pneumoniae‑Isolaten gefunden, die während eines echten Krankenhausausbruchs von Patientinnen und Patienten gesammelt wurden, insbesondere bei Harnwegs‑ und Wundinfektionen mit Katheterbeteiligung. Diese enge Übereinstimmung legt nahe, dass Katheteroberflächen im Körper ähnliche Selektionsdrücke ausüben wie im Labor und kontinuierlich Varianten begünstigen, die besser haften, clustern und auf Geräten überdauern. Gleichzeitig können einige dieser Anpassungen die Fähigkeit der Bakterien zu schneller, invasiver Krankheit schwächen und sie möglicherweise in Richtung Persistenz und chronischer Infektion verschieben. Das Verständnis dieser evolutiven Zielkonflikte könnte helfen, Geräte und Behandlungen zu entwerfen, die biofilmfreundliche Pfade unterbrechen, bevor sie sich etablieren.
Zitation: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Schlüsselwörter: Klebsiella pneumoniae, Biofilme, katheterassoziierte Infektionen, bakterielle Evolution, Antibiotikaresistenz