Clear Sky Science · ja
in vitroでのKlebsiella pneumoniaeバイオフィルムの急速な進化は感染中に選択される適応変化を描き出す
なぜ“粘着性”の病院内細菌が重要なのか
多くの病院感染は私たちの組織で始まるのではなく、カテーテルや人工呼吸チューブなどのプラスチックやシリコーン表面で始まります。これらの人工表面上で、Klebsiella pneumoniaeのような細菌はバイオフィルムと呼ばれる粘性の保護コミュニティを形成し、除去が難しく抗生物質での治療も困難になります。本研究は単純だが重要な問いを立てます:これらの日常的な病院内菌は、カテーテルに似た表面でバイオフィルム形成が上手くなるまで、どれほど速く、どのような方法で進化するのか—そしてそれは病原性にどう影響するのか?
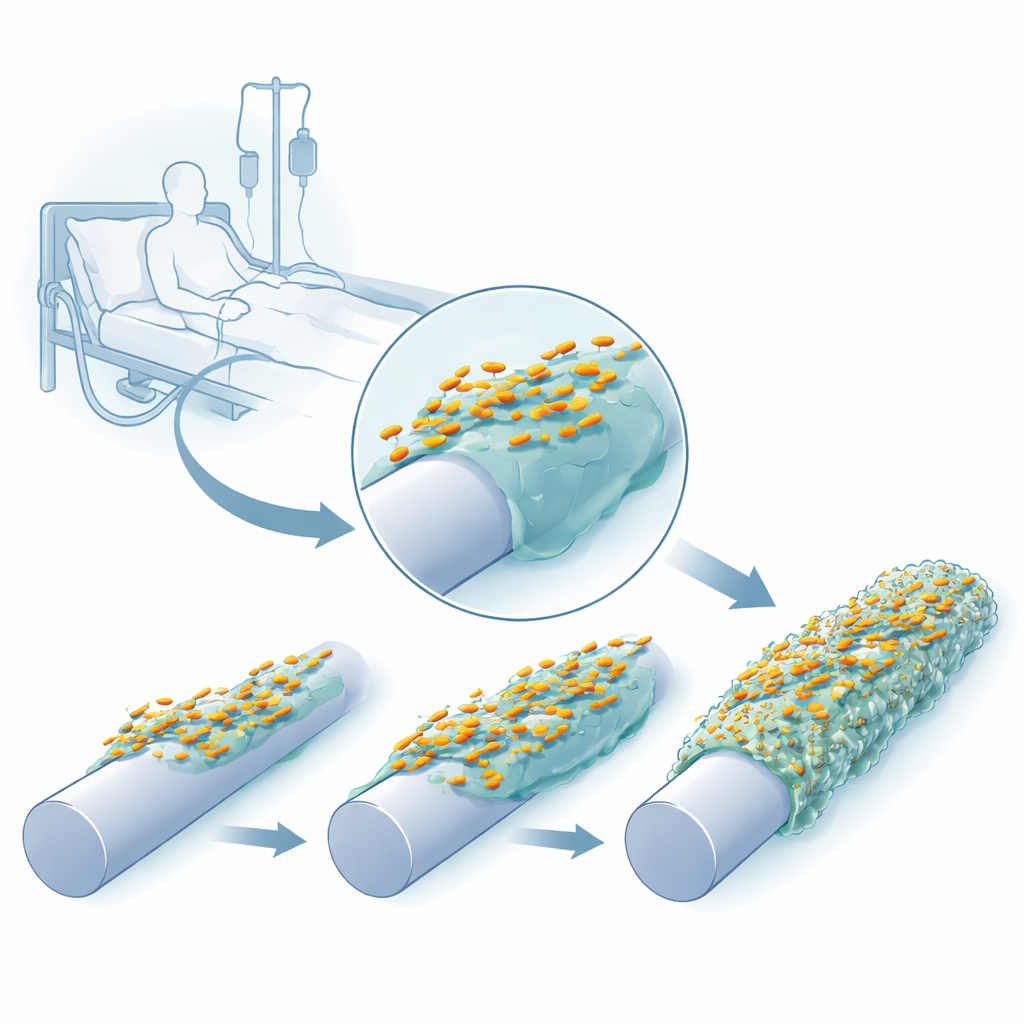
プラスチック適応を追う
研究者たちはラボでカテーテルに似た環境を再現し、表面を素地のまま、シリコーンでコーティング、あるいはシリコーン+挿入カテーテルに自然に付着するヒト血液タンパク質フィブリノーゲンで覆うことができるピッグデバイスを用いました。臨床由来のK. pneumoniaeの3株をこれらのピッグ上で繰り返し培養し、付着した細胞を回収して次のサイクルの開始に用いました。わずか数世代で、細菌はより厚く堅牢なバイオフィルムを形成し、寒天培地上のコロニー形態も変化しました—一部は異常に粘性で糸を引くようになり、他はやや透過性を帯びたり表面がしわ状になったりしました。
粘着性獲得への遺伝的近道
百を超える進化クローンのゲノムを解読した結果、これらの新しい形質は独立系統で繰り返し生じた特定の遺伝的変化を反映していることが示されました。多くの変異は、通常は細菌が免疫を逃れるのに役立つ糖質の被覆であるカプセル系に集中していました。主要なカプセルタンパク質(Wzc)の微細な変化は、シリコーンやフィブリノーゲン被覆面に広がる超粘性の細胞を生み出し、他の変異はカプセル産生を完全に止めて粘性を失う代わりに強く付着する細胞をもたらしました。もう一つの主要標的は、つかみかかるフックとして働く毛状表面構造(タイプ3線毛)の先端タンパク質MrkDでした。このタンパク質の小さな構造的改変や、これらの線毛を制御するシグナル伝達網の変化は、初期付着力を高め、異なる表面上でのバイオフィルムの広がり方や凝集の仕方を変えました。
異なる構成要素から作られるバイオフィルム
高性能のバイオフィルムがすべて同じ見た目や働きをするわけではありませんでした。ある変異体は厚いカプセル物質に依存してカテーテル様表面上に滑らかで連続した層を形成しました。特にカプセルを失ったものや小分子c‑di‑GMPを介して内部のシグナル伝達を書き換えたものは、豊富な表面の毛状構造やセルロース繊維を多量に産生し、それが細胞を離散的な塊に結びつけました。電子顕微鏡観察は、これらの異なる戦略が均一なぬめり被覆から繊維状マトリックスに埋め込まれた斑状の塔状凝集体まで、非常に異なる構造を生み出すことを示しました。どの戦略が優位になるかは細菌株と表面の種類の両方に依存しており、遺伝的背景と局所環境が共同でバイオフィルムの進化を形作ることを強調しています。
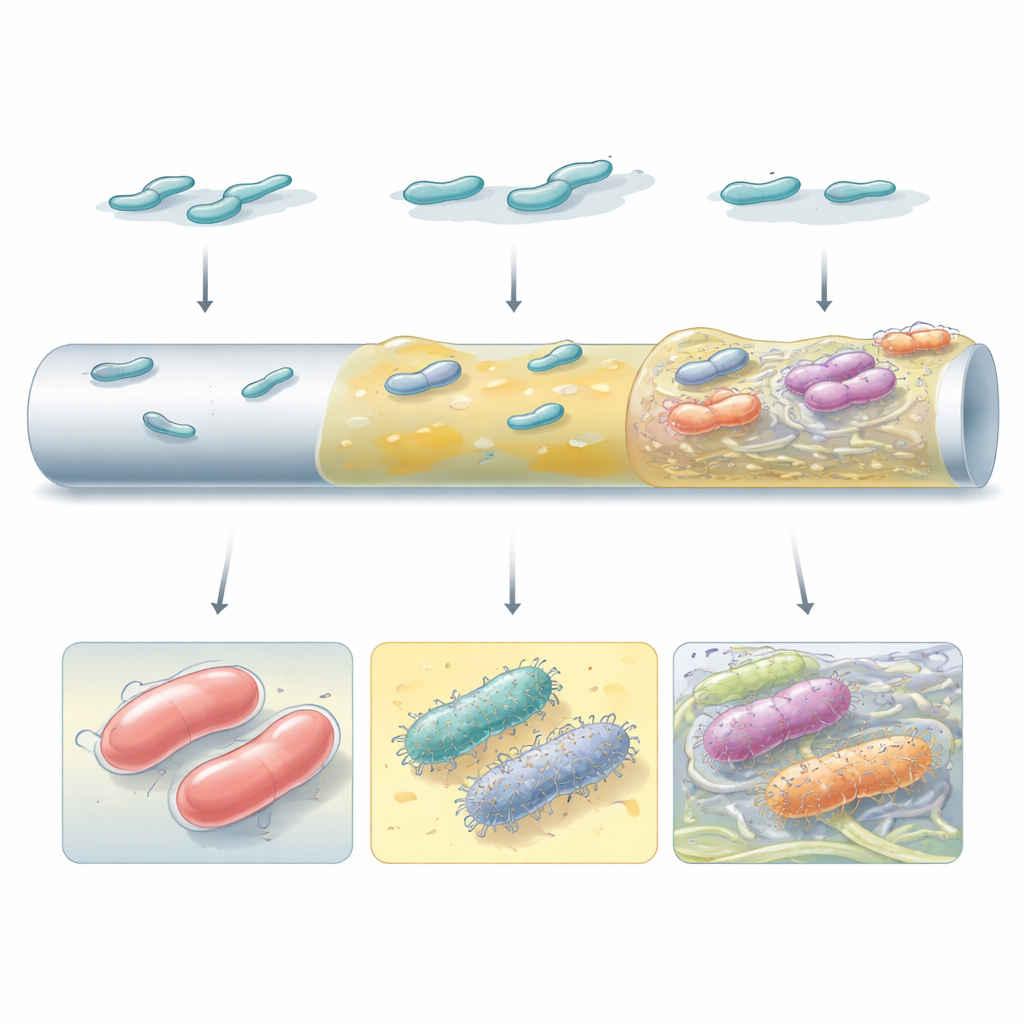
定着力と攻撃性のトレードオフ
より優れたバイオフィルム形成能の獲得には見えないコストが伴いました。ヒト血清中で浮遊性に増殖させると、カプセル欠損変異体と超粘性のWzc変異体は、自然免疫の重要な一部である補体によってはるかに簡単に殺されました。しかし一度バイオフィルムとして組織化されると、これらの変異体は血清攻撃から保護されました。ワックスモス幼虫を用いた感染モデルでは、バイオフィルム増強変異体の中には致死性が低下するものもあれば、変わらないものやむしろ増すものもありました。これは「バイオフィルムが増える=病気が重くなる」ではなく、どの変異が起きるかが重要であることを示しています。
患者内で起きていることを反映する
驚くべきことに、ラボで進化したバイオフィルム特化型で見られた多くの遺伝子――さらには同一の一塩基置換でさえ――が、実際の病院アウトブレイクで集められたK. pneumoniae分離株、特にカテーテルに関連する尿路や創傷感染から得られた分離株にも見つかりました。この密接な重なりは、体内のカテーテル表面がラボのものと同様の選択圧をかけ、デバイス上でよりよく付着し、凝集し、生き残る変異体を着実に有利にすることを示唆します。同時に、これらの適応の一部は細菌の速やかな侵襲性疾患を引き起こす能力を弱め、持続的で慢性の感染へと傾く可能性があります。これらの進化的トレードオフを理解することは、バイオフィルムに有利な経路が定着する前に妨げるようなデバイス設計や治療法の開発に役立つかもしれません。
引用: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
キーワード: Klebsiella pneumoniae, バイオフィルム, カテーテル関連感染, 細菌の進化, 抗生物質耐性