Clear Sky Science · pt
Evolução rápida de biofilmes de Klebsiella pneumoniae in vitro delineia mudanças adaptativas selecionadas durante a infecção
Por que germes pegajosos em hospitais importam
Muitas infecções hospitalares começam não em nossos tecidos, mas nas superfícies plásticas e de silicone de cateteres, tubos respiratórios e outros dispositivos médicos. Nessas superfícies artificiais, bactérias como Klebsiella pneumoniae podem construir comunidades protetoras e viscosas chamadas biofilmes, que são difíceis de remover e de tratar com antibióticos. Este estudo faz uma pergunta simples, porém crucial: com que rapidez e de que maneiras esses germes comuns de hospital evoluem para se tornarem melhores em formar biofilmes em superfícies semelhantes a cateteres — e o que isso significa para sua capacidade de causar doença?
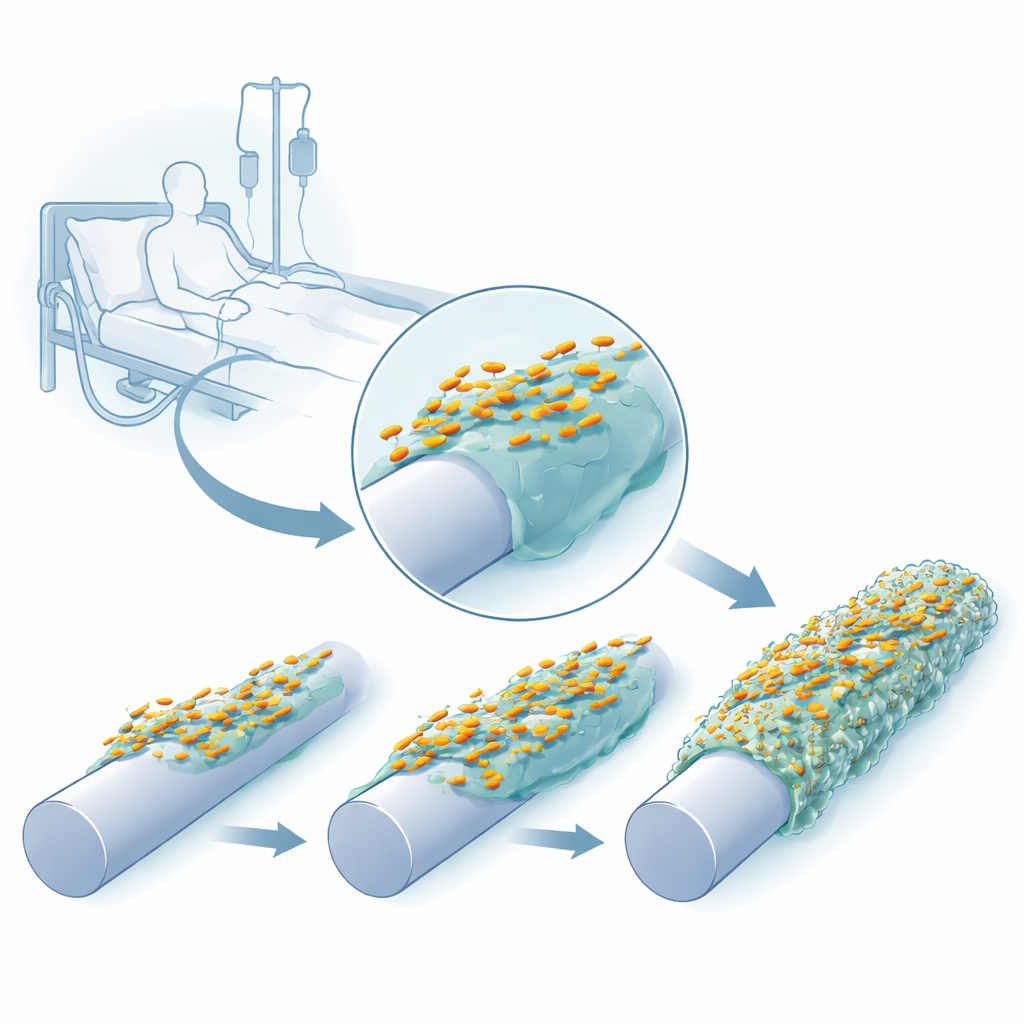
Acompanhando bactérias enquanto se adaptam ao plástico
Os pesquisadores recriaram um ambiente semelhante ao de um cateter no laboratório usando um dispositivo com pinos cujas superfícies podiam ficar nuas, revestidas de silicone ou cobertas com silicone e uma proteína sanguínea humana, a fibrinogena, que se acumula naturalmente em cateteres inseridos. Eles cultivaram repetidamente três cepas clínicas de K. pneumoniae nesses pinos, colheram as células aderidas e as usaram para iniciar o ciclo seguinte. Em apenas alguns ciclos de crescimento, as bactérias formaram biofilmes mais espessos e robustos, e suas colônias em placas de ágar começaram a ter aparência diferente — algumas ficando incomumente viscosas e filantosas, outras mais translúcidas ou formando superfícies enrugadas.
Atalhos genéticos para ficar mais pegajoso
Ao sequenciar os genomas de mais de cem clones evoluídos, a equipe mostrou que essas novas aparências refletiam mudanças genéticas específicas que surgiram repetidamente em linhagens independentes. Muitas mutações atingiram o sistema de cápsula, um revestimento açucarado que normalmente ajuda a bactéria a escapar do ataque imunológico. Alterações sutis em uma proteína chave da cápsula (Wzc) produziram células hiper‑viscosas que se espalhavam ao longo de superfícies revestidas de silicone e fibrinogênio, enquanto outras mutações desligaram totalmente a produção da cápsula, gerando células não viscosas, mas fortemente adesivas. Um segundo alvo importante foi a proteína da ponta (MrkD) de uma estrutura superficial em forma de pelo (fimbrias do tipo 3) que funciona como um gancho. Pequenos ajustes estruturais nessa proteína, ou mudanças nas redes de sinalização que regulam essas fimbrias, aumentaram a adesão inicial e alteraram como os biofilmes se espalham e se aglomeram em diferentes superfícies.
Biofilmes construídos a partir de blocos diferentes
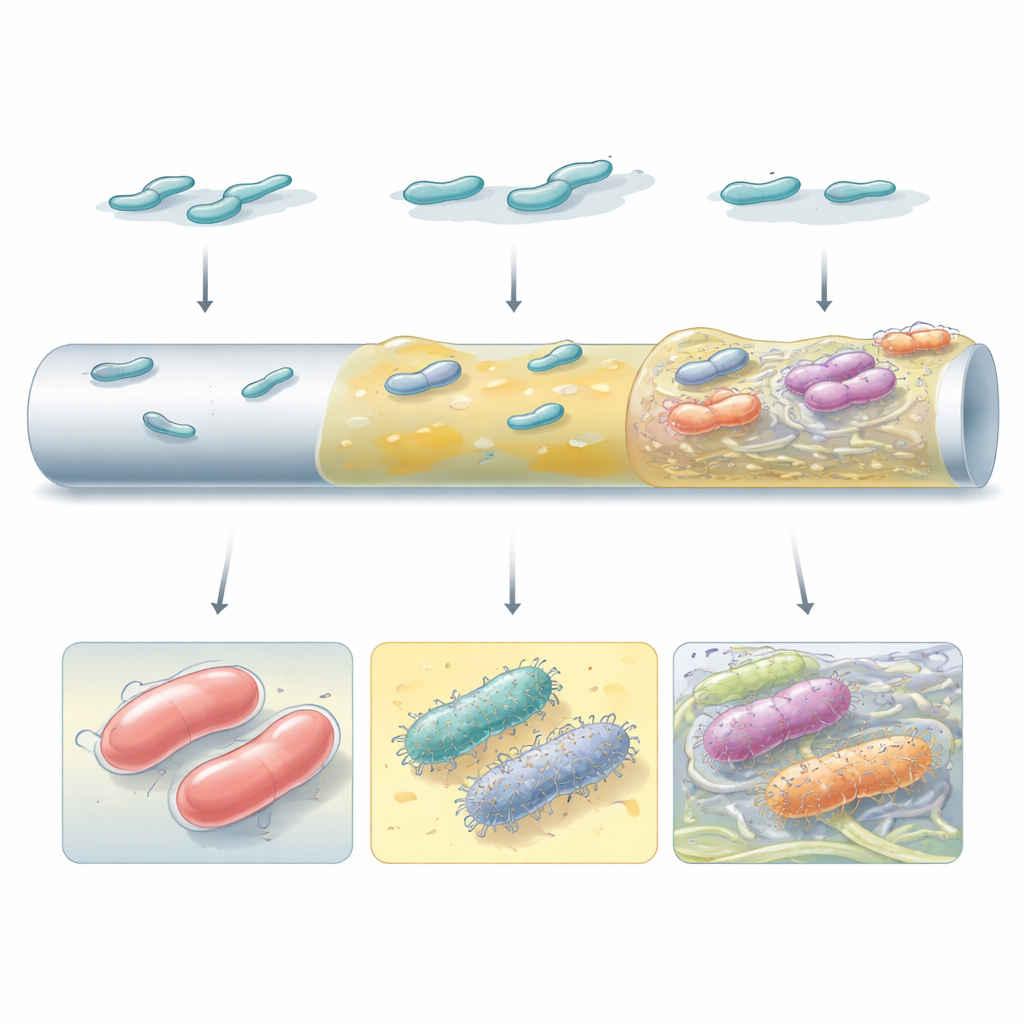
Nem todos os biofilmes de alto desempenho pareciam ou funcionavam da mesma forma. Alguns mutantes dependiam de material de cápsula espesso para formar camadas lisas e contínuas sobre a superfície semelhante a cateter. Outros, especialmente aqueles que perderam a cápsula ou reprogramaram a sinalização interna via a pequena molécula c‑di‑GMP, produziram muitos pelos de superfície e fibras de celulose que ligavam as células em aglomerados discretos. A microscopia eletrônica revelou que essas estratégias distintas criaram arquiteturas muito diferentes: desde revestimentos uniformes de muco até agregados irregulares em forma de torre embebidos em uma matriz fibrosa. Qual estratégia prevalecia dependia tanto da cepa bacteriana quanto do tipo de superfície, ressaltando que o pano de fundo genético e o ambiente local moldam conjuntamente como os biofilmes evoluem.
Um trade‑off entre permanecer e atacar com força
Tornar‑se um formador de biofilme melhor trouxe custos ocultos. Quando cultivados como células livres nadando em soro humano, tanto mutantes deficientes em cápsula quanto as variantes hiper‑viscosas Wzc foram muito mais facilmente mortos pelo complemento, uma via fundamental do nosso sistema imunológico inato. Ainda assim, uma vez organizados em um biofilme, esses mesmos mutantes ficaram protegidos do ataque do soro. Em um modelo de infecção usando larvas de mariposa‑cera, alguns mutantes com biofilme aprimorado tornaram‑se menos letais, enquanto outros não mudaram ou até aumentaram a virulência. Isso mostrou que “mais biofilme” não significa automaticamente “doença mais grave”; a mutação exata importa.
Espelhando o que acontece em pacientes
De forma impressionante, muitos dos mesmos genes — e até mudanças de uma única letra no DNA — observadas nos especialistas em biofilme evoluídos em laboratório também foram encontradas em isolados de K. pneumoniae coletados de pacientes durante um surto hospitalar real, especialmente em infecções do trato urinário e feridas envolvendo cateteres. Essa sobreposição próxima sugere que as superfícies de cateteres no corpo exercem pressões seletivas semelhantes às do laboratório, favorecendo de forma contínua variantes melhores em aderir, agrupar‑se e sobreviver em dispositivos. Ao mesmo tempo, algumas dessas adaptações podem enfraquecer a capacidade das bactérias de causar doenças invasivas rapidamente, potencialmente deslocando‑as para a persistência e infecções crônicas. Compreender esses trade‑offs evolutivos pode ajudar a projetar dispositivos e tratamentos que interrompam caminhos favoráveis a biofilmes antes que se tornem enraizados.
Citação: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Palavras-chave: Klebsiella pneumoniae, biofilmes, infecções associadas a cateter, evolução bacteriana, resistência a antibióticos