Clear Sky Science · nl
Snelle evolutie van Klebsiella pneumoniae-biofilms in vitro onthult adaptieve veranderingen geselecteerd tijdens infectie
Waarom kleverige ziekenhuiskiemen ertoe doen
Veel ziekenhuisinfecties beginnen niet in ons weefsel, maar op de kunststof- en siliconenoppervlakken van catheters, beademingsbuizen en andere medische hulpmiddelen. Op die kunstmatige oppervlakken kunnen bacteriën zoals Klebsiella pneumoniae slijmerige, beschermende gemeenschappen vormen die biofilms worden genoemd; die zijn moeilijk te verwijderen en lastig met antibiotica te behandelen. Deze studie stelt een eenvoudige maar cruciale vraag: hoe snel, en op welke manieren, evolueren deze veelvoorkomende ziekenhuiskiemen om beter biofilms te vormen op katheterachtige oppervlakken — en wat betekent dat voor hun vermogen om ziekte te veroorzaken?
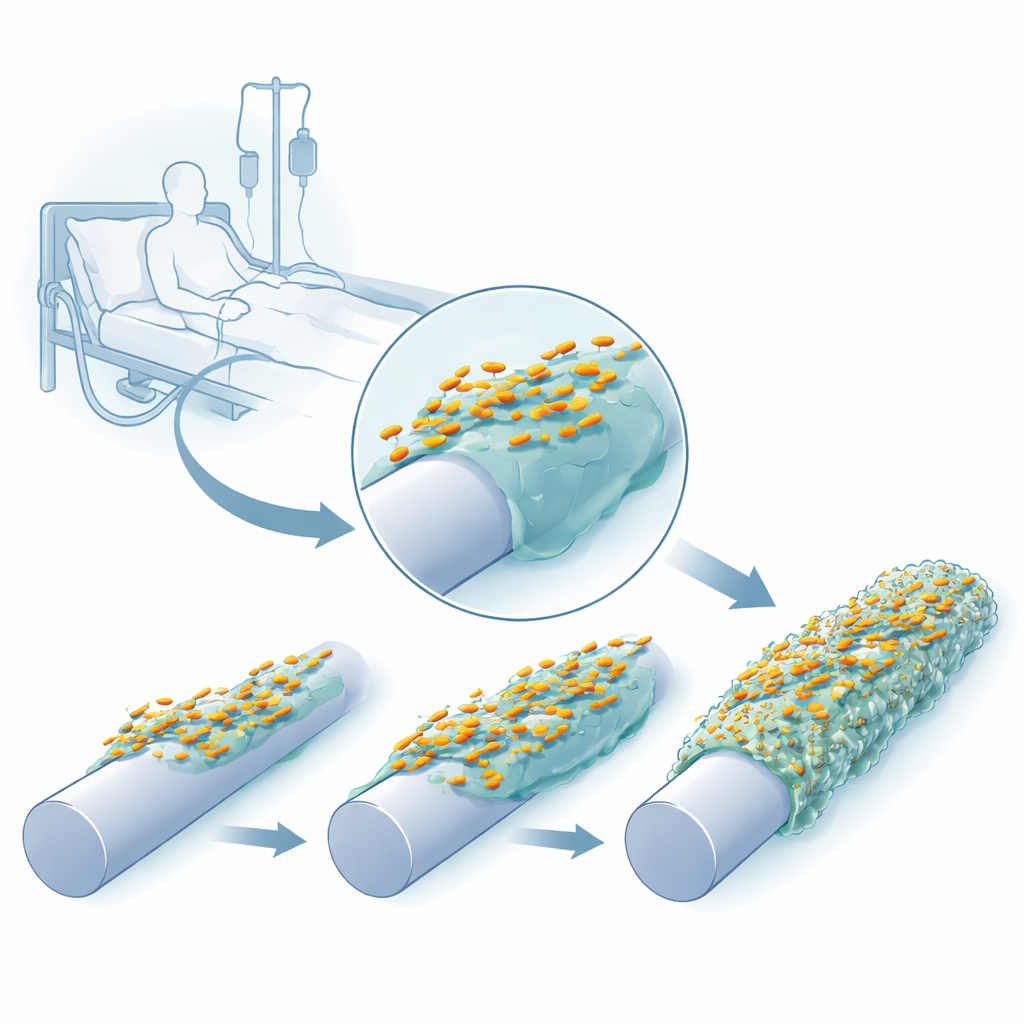
Bacteriën volgen terwijl ze zich aan plastic aanpassen
De onderzoekers recreëerden een katheterachtige omgeving in het laboratorium met een pinapparaat waarvan de oppervlakken kaal konden blijven, met siliconen konden worden gecoat of bedekt konden worden met zowel siliconen als het menselijke bloed‑eiwit fibrinogeen, dat zich van nature op ingebracht kathetermateriaal verzamelt. Ze lieten herhaaldelijk drie klinische stammen van K. pneumoniae op deze pennen groeien, oogstten de aangehechte cellen en gebruikten die om de volgende cyclus te starten. Al binnen enkele groeicycli vormden de bacteriën dikkere, robuustere biofilms en begonnen hun kolonies op agarplaatjes er anders uit te zien — sommige werden ongewoon slijmerig en snotterig, andere meer doorschijnend of met gegolfde, gerimpelde oppervlakken.
Genetische snelwegen naar meer kleverigheid
Door het genoom van meer dan honderd geëvolueerde klonen te sequencen, toonde het team aan dat deze nieuwe verschijningsvormen specifieke genetische veranderingen weerspiegelen die herhaaldelijk onafhankelijk in verschillende lijnen optraden. Veel mutaties troffen het kapselsysteem, een suikerrijk omhulsel dat de bacteriën normaal helpt immuunaanvallen te ontlopen. Subtiele veranderingen in een sleutelcapsuleiwit (Wzc) leverden hyper‑slijmerige, zeer viskeuze cellen op die zich over siliconen- en fibrinogeengeroerde oppervlakken verspreidden, terwijl andere mutaties de kapselproductie volledig uitschakelden en niet‑slijmerige maar sterk hechtende cellen opleverden. Een tweede belangrijk doelwit was het top‑eiwit (MrkD) van een haarachtige oppervlakte‑structuur (type 3 fimbriae) die als grijphaak fungeert. Kleine structurele aanpassingen in dit eiwit, of veranderingen in de signaalnetwerken die deze fimbriae reguleren, versterkten vroege aanhechting en veranderden hoe biofilms zich verspreidden en samenklonterden op verschillende oppervlakken.
Biofilms opgebouwd uit verschillende bouwstenen
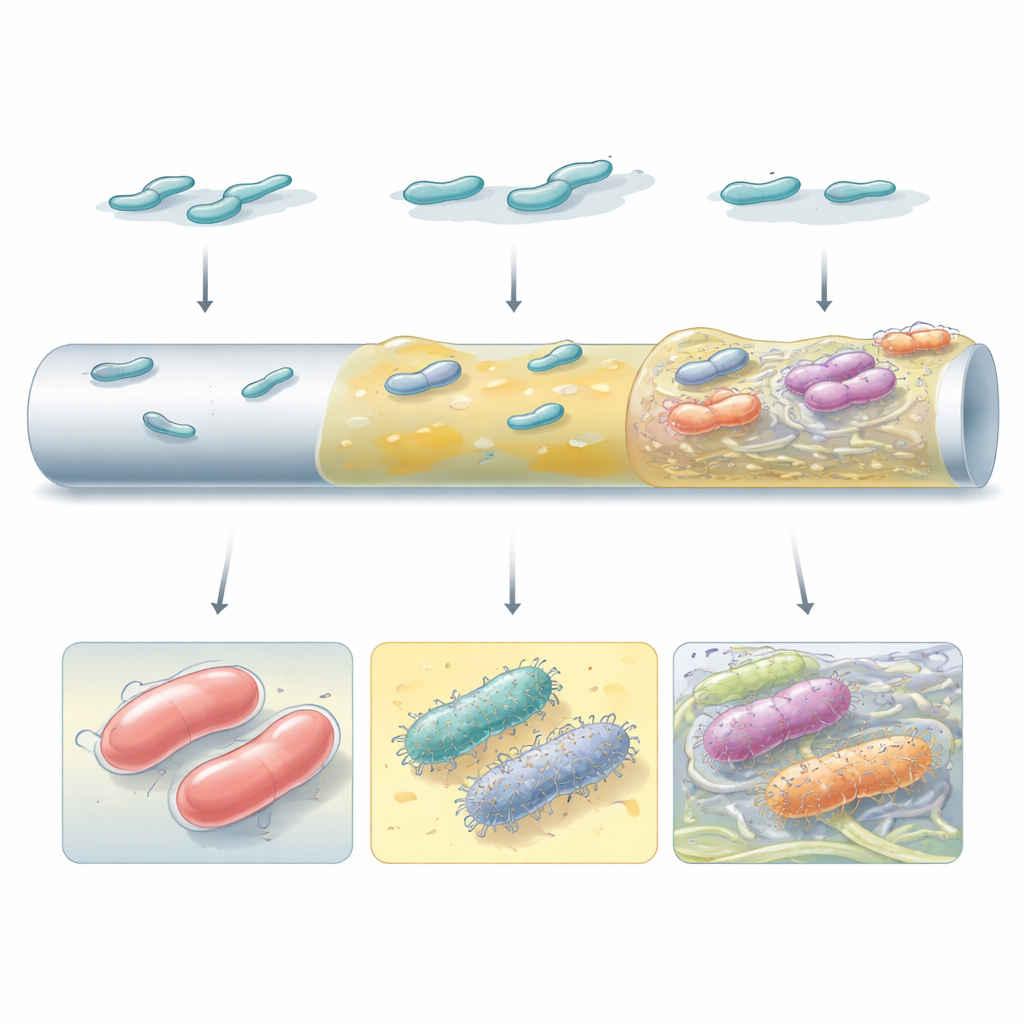
Niet alle hoogpresterende biofilms zagen er hetzelfde uit of functioneerden hetzelfde. Sommige mutanten vertrouwden op dik kapselmateriaal om gladde, continue lagen over het katheterachtige oppervlak te vormen. Andere, vooral diegenen die hun kapsel hadden verloren of hun interne signalering via het kleine molecuul c‑di‑GMP hadden herbedraad, produceerden overvloedige oppervlakteharen en cellulosevezels die cellen samenbonden tot discrete clusters. Elektronenmicroscopie toonde aan dat deze uiteenlopende strategieën zeer verschillende architecturen creëerden: van uniforme slijmlaag tot ongelijkmatige, torenachtige aggregaten ingebed in een vezelig matrix. Welke strategie de overhand kreeg, hing af van zowel de bacteriële stam als het oppervlakstype, wat onderstreept dat genetische achtergrond en lokale omgeving samen bepalen hoe biofilms evolueren.
Een afweging tussen blijven plakken en hard toeslaan
Beter worden in het vormen van biofilms ging gepaard met verborgen kosten. Wanneer als vrijzwemmende cellen in humaan serum gekweekt, werden zowel kapseldeficiënte mutanten als de hyper‑slijmerige Wzc‑varianten veel gemakkelijker gedood door complement, een belangrijk onderdeel van onze aangeboren afweer. Toch waren dezezelfde mutanten, eenmaal georganiseerd in een biofilm, beschermd tegen serumaanvallen. In een infectiemodel met wasmotlarven werden sommige biofilm‑versterkte mutanten minder dodelijk, terwijl andere geen verandering lieten zien of zelfs in virulentie toenamen. Dit liet zien dat “meer biofilm” niet automatisch “ernstigere ziekte” betekent; de specifieke mutatie is bepalend.
Een weerklank van wat er bij patiënten gebeurt
Opvallend was dat veel van dezelfde genen — en zelfs identieke single‑letter DNA‑veranderingen — die in de in het laboratorium geëvolueerde biofilmspecialisten werden gevonden, ook terugkwamen in K. pneumoniae‑isolaten die bij patiënten werden verzameld tijdens een echte ziekenhuisuitbraak, vooral bij urineweg‑ en wondinfecties waarbij katheters betrokken waren. Deze nauwe overlap suggereert dat katheteroppervlakken in het lichaam vergelijkbare selectiedruk uitoefenen als die in het laboratorium, en geleidelijk varianten bevoordelen die beter kunnen kleven, klonteren en overleven op apparaten. Tegelijkertijd kunnen sommige van deze aanpassingen het vermogen van de bacteriën om snelle, invasieve ziekte te veroorzaken verzwakken, waardoor ze mogelijk neigen naar persistentie en chronische infectie. Inzicht in deze evolutionaire afwegingen kan helpen bij het ontwerpen van hulpmiddelen en behandelingen die biofilmvriendelijke paden verstoren voordat ze zich vastzetten.
Bronvermelding: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Trefwoorden: Klebsiella pneumoniae, biofilms, katheter-geassocieerde infecties, bacteriële evolutie, antibioticaresistentie