Clear Sky Science · ru
Быстрая эволюция биопленок Klebsiella pneumoniae in vitro выявляет адаптивные изменения, отбираемые во время инфекции
Почему липкие госпитальные микробы имеют значение
Многие госпитальные инфекции начинаются не в тканях человека, а на пластиковых и силиконовых поверхностях катетеров, дыхательных трубок и других медицинских устройств. На этих искусственных поверхностях бактерии, такие как Klebsiella pneumoniae, могут формировать скользкие защитные сообщества — биопленки, которые трудно удалить и которые плохо поддаются лечению антибиотиками. В этом исследовании поставлен простой, но важный вопрос: как быстро и какими способами эти обычные госпитальные микробы эволюционируют, чтобы лучше образовывать биопленки на подобных катетеру поверхностях — и что это означает для их способности вызывать заболевание?
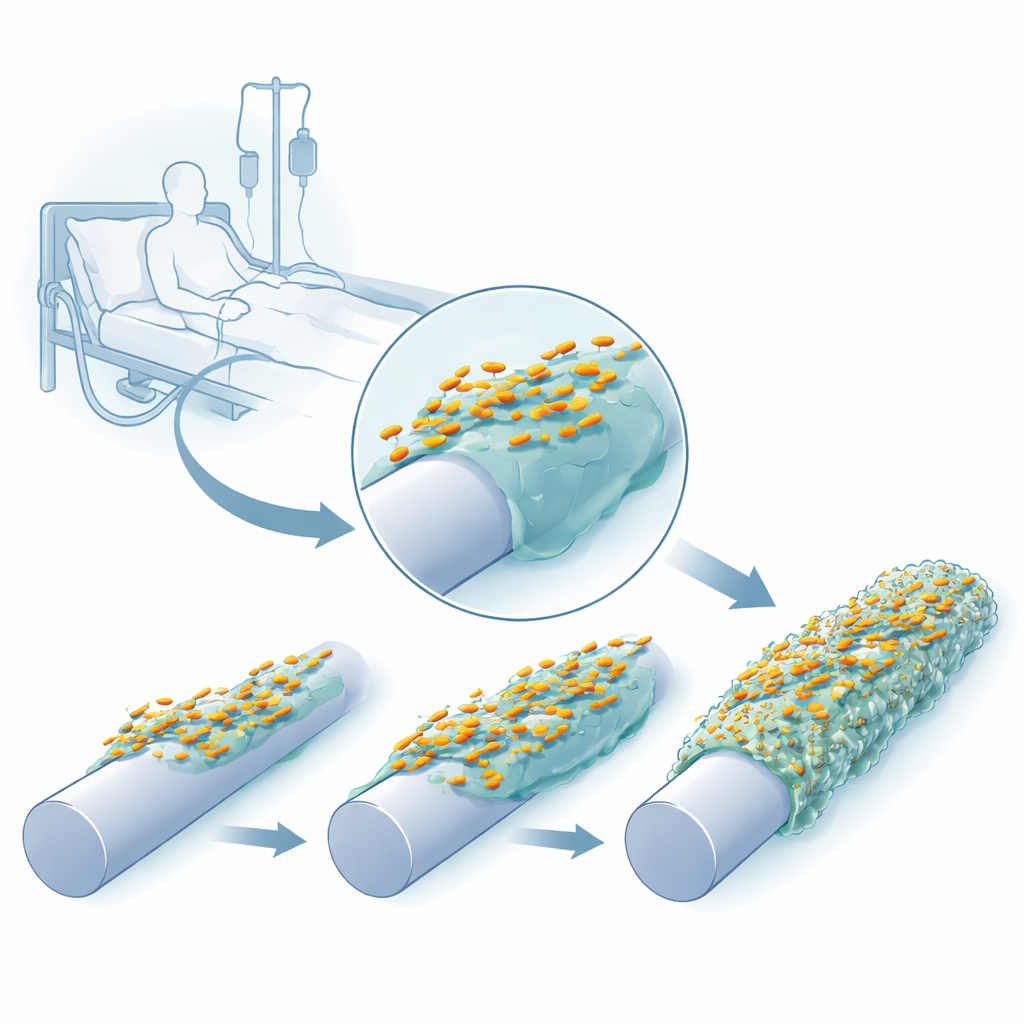
Наблюдая бактерии по мере их адаптации к пластику
Исследователи воссоздали в лаборатории среду, похожую на катетер, используя устройство с штифтами (peg), поверхности которых оставляли голыми, покрывали силиконовым слоем или покрывали одновременно силиконом и человеческим белком крови фибриногеном, который естественно оседает на вставленных катетерах. Они многократно выращивали три клинических штамма K. pneumoniae на этих штифтах, собирали прикрепившиеся клетки и использовали их для начала следующего цикла. Всего за несколько циклов роста бактерии образовали более густые, более прочные биопленки, а их колонии на агаре стали выглядеть иначе — некоторые стали необычно слизистыми и нитчатыми, другие — более прозрачными или образовали морщинистую поверхность.
Генетические короткие пути к большей липкости
Секвенируя геномы более сотни эволюционировавших клонов, команда показала, что эти новые внешние признаки отражают конкретные генетические изменения, которые многократно возникали в независимых линиях. Многие мутации затрагивали систему капсулы — сахаристую оболочку, которая обычно помогает бактериям уклоняться от иммунной атаки. Тонкие изменения в ключевом капсульном белке (Wzc) приводили к гиперслизистым, высоковязким клеткам, которые распространялись по силиконовым и фибриногеновым поверхностям, тогда как другие мутации полностью выключали производство капсулы, давая нелипкие, но сильно адгезивные клетки. Второй важной целью был концевой белок (MrkD) волосковидной поверхностной структуры (тип 3 фимбрий), действующий как крючок. Небольшие структурные изменения в этом белке или изменения в сигнальных сетях, регулирующих эти фимбрии, усиливали раннее прикрепление и меняли то, как биопленки распространяются и скапливаются на разных поверхностях.
Биопленки, построенные из разных «строительных блоков»
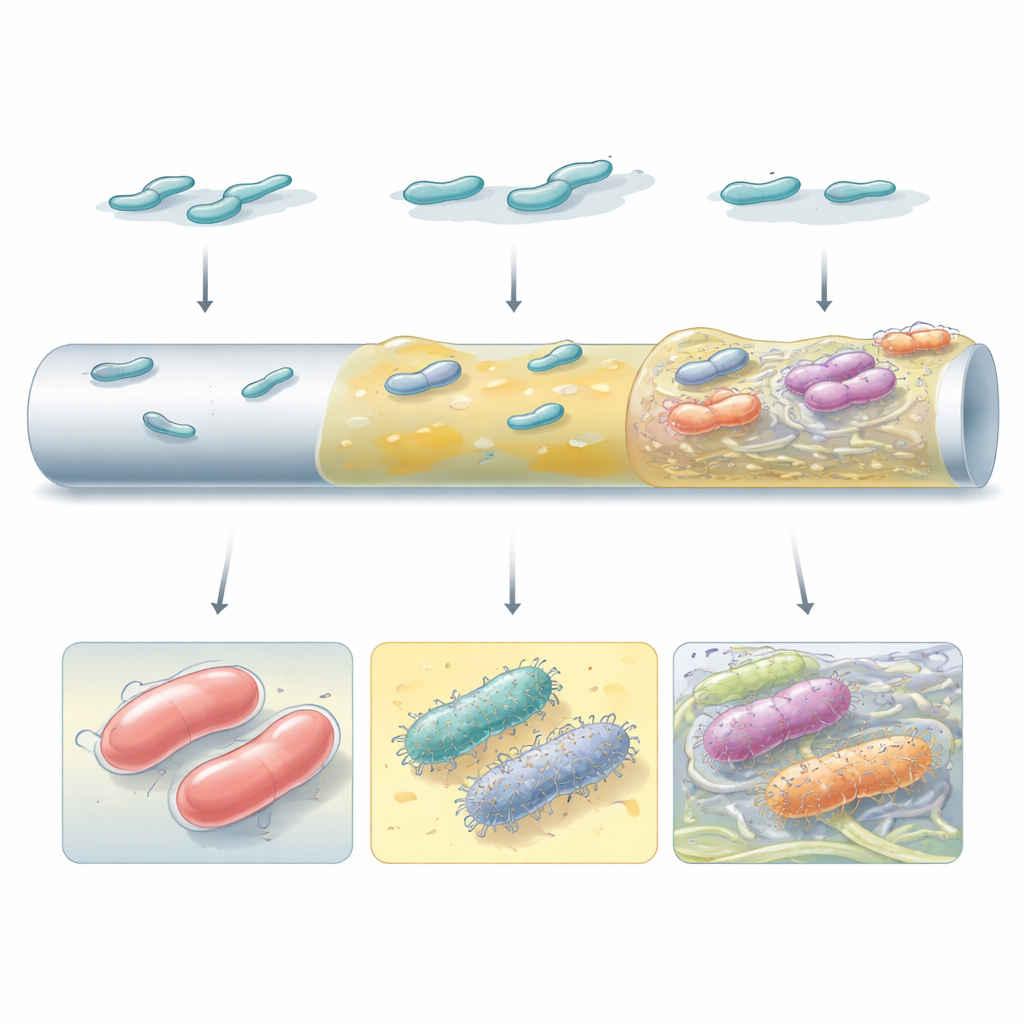
Не все высокоэффективные биопленки выглядели или работали одинаково. Некоторые мутанты полагались на толстый капсульный материал, чтобы формировать гладкие, непрерывные слои на поверхности, похожей на катетер. Другие, особенно те, что потеряли капсулу или перенастроили внутренняя сигнализацию через малую молекулу c-di-GMP, производили обилие поверхностных волосков и целлюлозных волокон, которые связывали клетки в отдельные кластеры. Сканирующая электронная микроскопия показала, что эти разные стратегии создают очень отличающуюся архитектуру: от однородных слизистых покровов до пятнистых, башневидных агрегатов, встроенных в фиброзную матрицу. Побеждавшая стратегия зависела как от бактериального штамма, так и от типа поверхности, что подчеркивает, что генетический фон и локальная среда совместно определяют путь эволюции биопленок.
Торговля — между умением прилипать и способностью наносить удар
Становление лучшим формирователем биопленок имело скрытые издержки. При выращивании в свободно плавающем состоянии в человеческой сыворотке как капсульно-дефицитные мутанты, так и гиперслизистые варианты Wzc гораздо легче убивались системой комплемента — ключевым звеном врожденного иммунитета. Однако, будучи организованы в биопленку, те же мутанты были защищены от атаки сыворотки. В модели инфекции с личинками восковой моли некоторые мутанты с усиленной биопленкообразующей способностью стали менее смертельными, тогда как другие не изменили вирулентность или даже повысили её. Это показало, что «больше биопленки» не обязательно означает «более тяжёлое заболевание»; значение имеет конкретная мутация.
Отражение того, что происходит у пациентов
Удивительно, но многие из тех же генов — и даже идентичные однобуквенные изменения в ДНК — обнаруженные у лабораторно эволюционировавших специалистов по биопленкам, встречались также в изолятах K. pneumoniae, собранных у пациентов во время реальной госпитальной вспышки, особенно при инфекциях мочевыводящих путей и раневых инфекциях с участием катетеров. Это близкое совпадение указывает на то, что катетерные поверхности в организме создают сходные селективные давления с лабораторными условиями, последовательно отбирая варианты, лучше приспособленные к прилипанию, слипанию и выживанию на устройствах. В то же время некоторые из этих адаптаций могут ослаблять способность бактерий вызывать быстрое инвазивное заболевание, смещая их в сторону персистенции и хронической инфекции. Понимание этих эволюционных компромиссов может помочь в проектировании устройств и терапии, которые прерывают благоприятные для биопленок пути до того, как они укоренятся.
Цитирование: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Ключевые слова: Klebsiella pneumoniae, биопленки, инфекции, связанные с катетером, эволюция бактерий, антибиотикорезистентность