Clear Sky Science · it
Evoluzione rapida dei biofilm di Klebsiella pneumoniae in vitro delinea i cambiamenti adattativi selezionati durante l’infezione
Perché i germi “appiccicosi” degli ospedali sono importanti
Molte infezioni ospedaliere non hanno inizio nei nostri tessuti, ma sulle superfici di plastica e silicone di cateteri, tubi respiratori e altri dispositivi medici. Su queste superfici artificiali batteri come Klebsiella pneumoniae possono costruire comunità viscide e protettive chiamate biofilm, difficili da rimuovere e da trattare con antibiotici. Questo studio pone una domanda semplice ma cruciale: quanto rapidamente, e in quali modi, questi comuni germi ospedalieri evolvono per diventare più abili nel formare biofilm su superfici simili a quelle dei cateteri — e cosa significa questo per la loro capacità di provocare malattia?
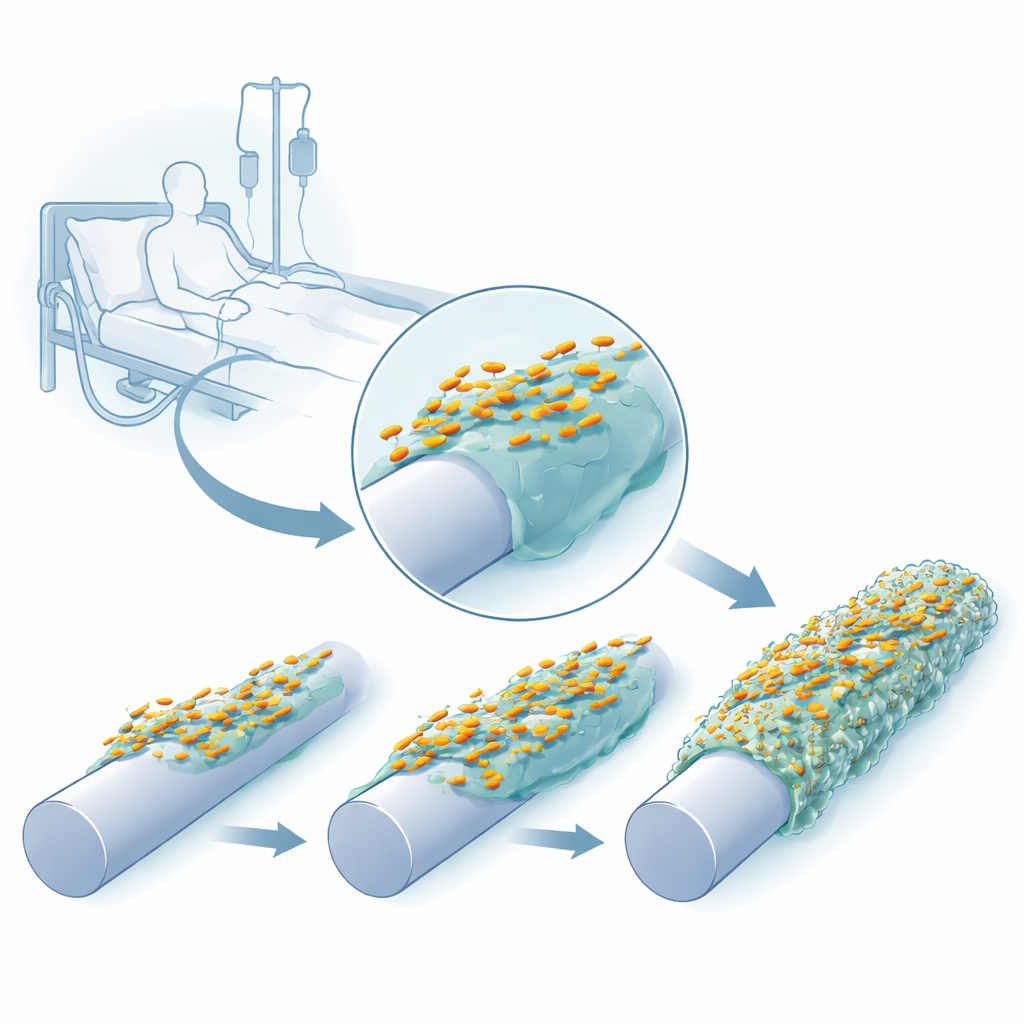
Seguire i batteri mentre si adattano alla plastica
I ricercatori hanno ricreato in laboratorio un ambiente simile a un catetere usando un dispositivo a perni le cui superfici potevano essere lasciate nude, ricoperte di silicone o coperte sia di silicone sia di una proteina umana presente nel sangue, la fibrinogena, che si deposita naturalmente sui cateteri inseriti. Hanno fatto crescere ripetutamente tre ceppi clinici di K. pneumoniae su questi perni, prelevato le cellule aderenti e usate per avviare il ciclo successivo. Nell’arco di poche replicazioni di crescita i batteri hanno formato biofilm più spessi e robusti, e le loro colonie su piastre di agar hanno cominciato ad apparire diverse — alcune diventando eccezionalmente viscide e filamentose, altre più traslucide o con superfici rugose.
Scorciatoie genetiche per diventare più “appiccicosi”
Sequenziando i genomi di oltre cento cloni evoluti, il team ha mostrato che questi nuovi aspetti corrispondevano a cambiamenti genetici specifici che sono ricomparsi in linee indipendenti. Molte mutazioni hanno colpito il sistema del capsula, un rivestimento zuccherino che normalmente aiuta i batteri a sfuggire all’attacco immunitario. Alterazioni sottili in una proteina chiave della capsula (Wzc) hanno prodotto cellule iperviscose che si diffondevano lungo superfici di silicone e rivestite di fibrinogeno, mentre altre mutazioni hanno spento completamente la produzione della capsula, dando luogo a cellule non viscide ma fortemente adesive. Un secondo bersaglio importante è stata la proteina terminale (MrkD) di una struttura superficiale simile a un pelo (fimbrie di tipo 3) che funge da uncino. Piccole modifiche strutturali in questa proteina, o cambiamenti nelle reti di segnalazione che regolano queste fimbrie, hanno aumentato l’attacco iniziale e alterato il modo in cui i biofilm si diffondono e aggregano su diverse superfici.
Biofilm costruiti con mattoni diversi
Non tutti i biofilm ad alte prestazioni avevano lo stesso aspetto o funzionamento. Alcuni mutanti facevano affidamento su uno spesso materiale di capsula per formare strati lisci e continui sulla superficie simile al catetere. Altri, specialmente quelli che avevano perso la capsula o che avevano riconfigurato la segnaling interna tramite la piccola molecola c‑di‑GMP, producevano abbondanti “peli” superficiali e fibre di cellulosa che legavano le cellule in ammassi distinti. La microscopia elettronica ha rivelato che queste strategie distinte hanno creato architetture molto diverse: da rivestimenti uniformi di muco ad aggregati a torretta incastonati in una matrice fibrosa. La strategia vincente dipendeva sia dal ceppo batterico sia dal tipo di superficie, sottolineando come il background genetico e l’ambiente locale plasmino congiuntamente l’evoluzione dei biofilm.
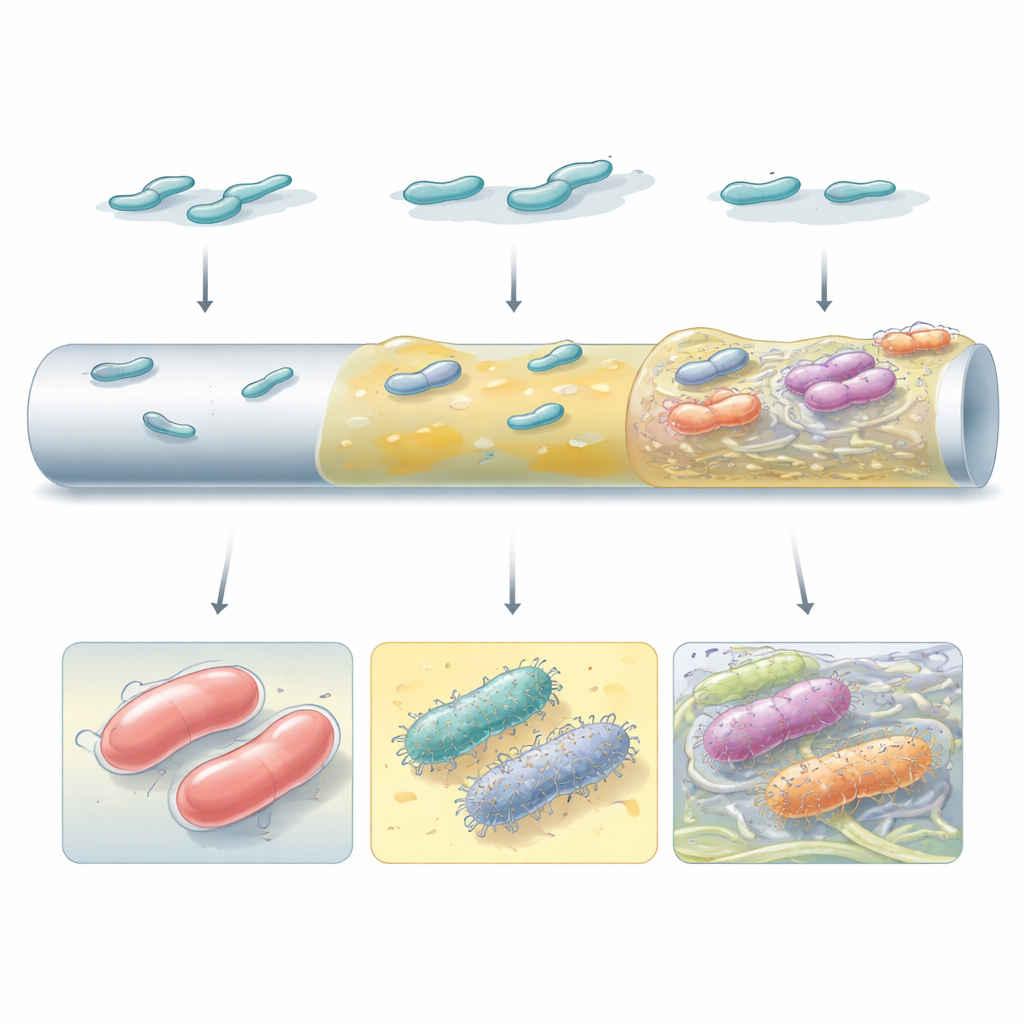
Un compromesso tra restare attaccati e colpire duramente
Diventare un migliore formatore di biofilm comportava costi nascosti. Quando cresciuti come cellule libere in siero umano, sia i mutanti privi di capsula sia le varianti iperviscose Wzc erano molto più facilmente uccise dal complemento, un braccio chiave del nostro sistema immunitario innato. Tuttavia, una volta organizzati in un biofilm, questi stessi mutanti erano protetti dall’attacco del siero. In un modello di infezione con larve di falena della cera, alcuni mutanti con biofilm potenziati sono diventati meno letali, mentre altri non sono cambiati o hanno mostrato un aumento di virulenza. Ciò dimostra che “più biofilm” non significa automaticamente “malattia più grave”; la mutazione precisa fa la differenza.
Specchio di ciò che avviene nei pazienti
È notevole che molti degli stessi geni — e persino identiche variazioni di singole lettere del DNA — osservati nei biofilm specialisti evoluti in laboratorio siano stati trovati anche in isolati di K. pneumoniae raccolti da pazienti durante un reale focolaio ospedaliero, in particolare nelle infezioni del tratto urinario e delle ferite associate a cateteri. Questo forte sovrapporsi suggerisce che le superfici dei cateteri nel corpo esercitino pressioni selettive simili a quelle del laboratorio, favorendo costantemente varianti più abili ad aderire, aggregarsi e sopravvivere sui dispositivi. Allo stesso tempo, alcune di queste adattazioni possono indebolire la capacità dei batteri di causare malattie invasive e rapide, spostandoli potenzialmente verso la persistenza e l’infezione cronica. Comprendere questi compromessi evolutivi può aiutare a progettare dispositivi e trattamenti che interrompano i percorsi favorevoli ai biofilm prima che si consolidino.
Citazione: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Parole chiave: Klebsiella pneumoniae, biofilm, infezioni associate a cateteri, <keyword>resistenza agli antibiotici