Clear Sky Science · fr
Évolution rapide des biofilms de Klebsiella pneumoniae in vitro décrivant les changements adaptatifs sélectionnés lors de l’infection
Pourquoi les germes collants en milieu hospitalier importent
Beaucoup d'infections nosocomiales commencent non pas dans nos tissus, mais sur les surfaces en plastique et en silicone des cathéters, des tubes respiratoires et d'autres dispositifs médicaux. Sur ces surfaces artificielles, des bactéries comme Klebsiella pneumoniae peuvent construire des communautés protectrices visqueuses appelées biofilms, difficiles à enlever et à traiter par les antibiotiques. Cette étude pose une question simple mais cruciale : à quelle vitesse, et de quelles manières, ces germes hospitaliers communs évoluent‑ils pour mieux former des biofilms sur des surfaces de type cathéter — et qu'est‑ce que cela signifie pour leur capacité à provoquer la maladie ?
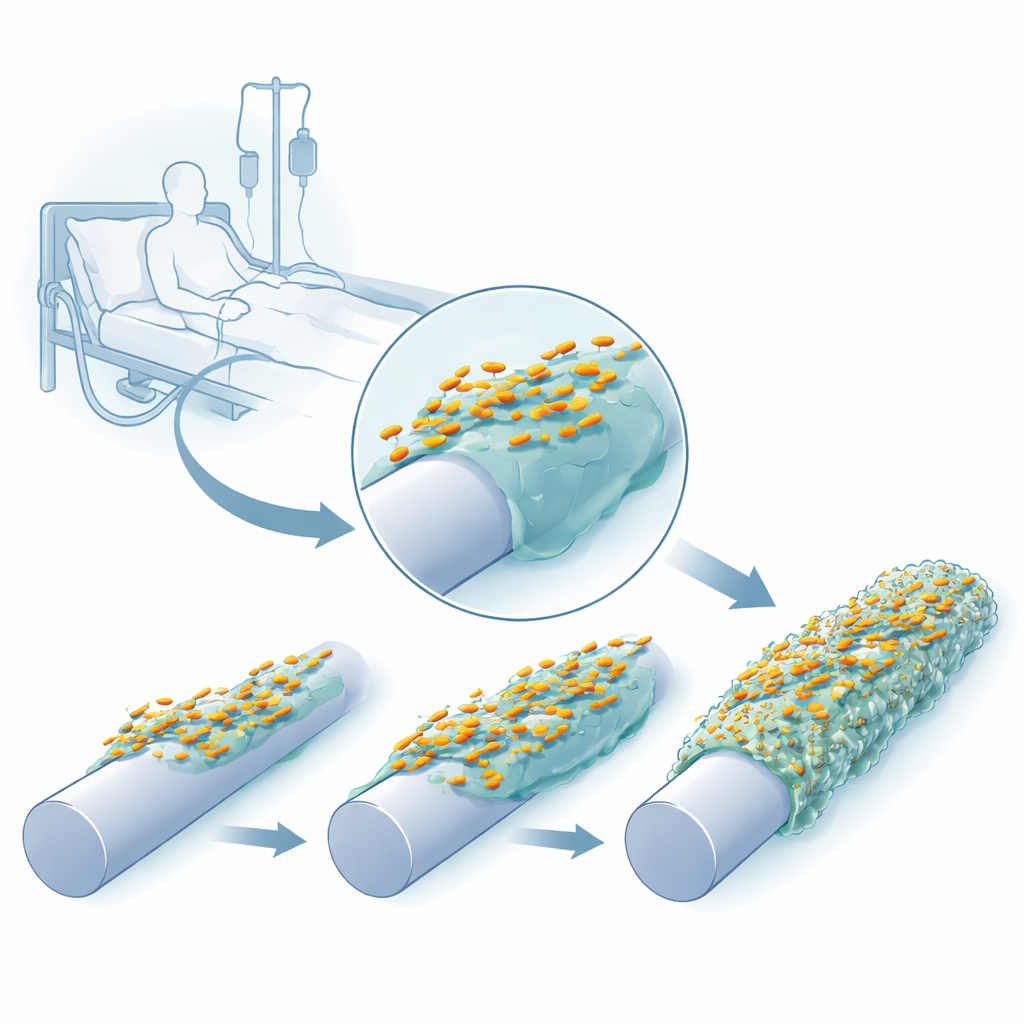
Suivre l’adaptation bactérienne au plastique
Les chercheurs ont recréé en laboratoire un environnement de type cathéter à l'aide d'un dispositif à broches dont les surfaces pouvaient rester nues, recouvertes de silicone, ou couvertes de silicone et d'une protéine sanguine humaine, la fibrinogène, qui se dépose naturellement sur les cathéters insérés. Ils ont fait croître à plusieurs reprises trois souches cliniques de K. pneumoniae sur ces broches, récolté les cellules attachées et les ont utilisées pour démarrer le cycle suivant. En seulement quelques cycles de croissance, les bactéries formaient des biofilms plus épais et plus robustes, et leurs colonies sur gélose ont commencé à changer d'aspect — certaines devenant anormalement visqueuses et filandreuses, d'autres plus translucides ou formant des surfaces ridées.
Raccourcis génétiques vers une plus grande adhérence
En séquençant les génomes de plus d'une centaine de clones évolués, l'équipe a montré que ces nouvelles apparences reflétaient des changements génétiques spécifiques qui surgissaient de façon répétée dans des lignées indépendantes. De nombreuses mutations touchaient le système de capsule, un revêtement sucré qui aide normalement les bactéries à échapper à l'attaque immunitaire. Des altérations subtiles d'une protéine clé de la capsule (Wzc) ont produit des cellules hyper‑visqueuses et très sirupeuses qui se répandaient le long des surfaces en silicone et recouvertes de fibrinogène, tandis que d'autres mutations interrompaient entièrement la production de capsule, donnant des cellules non visqueuses mais fortement adhésives. Une seconde cible majeure était la protéine de pointe (MrkD) d'une structure superficielle en forme de poil (les fimbriae de type 3) qui agit comme un grappin. De petites modifications structurelles de cette protéine, ou des changements dans les réseaux de signalisation qui régulent ces fimbriae, ont renforcé l'attachement précoce et modifié la façon dont les biofilms se propagent et s'agglomèrent sur différentes surfaces.
Biofilms construits à partir de blocs différents
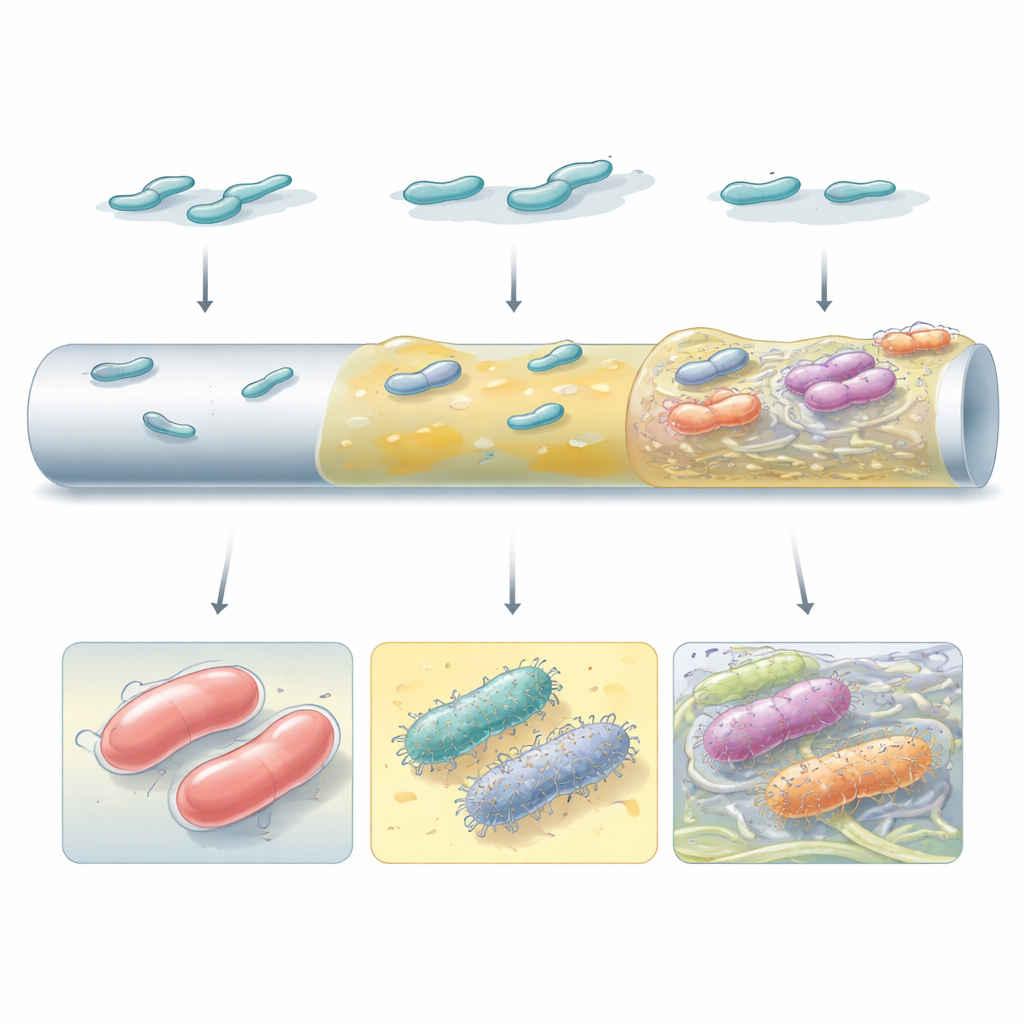
Tous les biofilms performants ne se ressemblaient pas et ne fonctionnaient pas de la même manière. Certains mutants s'appuyaient sur une grande quantité de matériau de capsule pour former des couches lisses et continues sur la surface de type cathéter. D'autres, en particulier ceux qui avaient perdu leur capsule ou reconfiguré la signalisation interne via la petite molécule c‑di‑GMP, produisaient de nombreux poils de surface et des fibres de cellulose qui reliaient les cellules en amas discrets. La microscopie électronique a révélé que ces stratégies distinctes créaient des architectures très différentes : des revêtements uniformes et visqueux à des agrégats ponctuels en forme de tours, nichés dans une matrice fibreuse. La stratégie retenue dépendait à la fois de la souche bactérienne et du type de surface, soulignant que le bagage génétique et l'environnement local façonnent conjointement l'évolution des biofilms.
Un compromis entre persistance et virulence aiguë
Devenir meilleur formateur de biofilm s’est accompagné de coûts cachés. Lorsqu'ils étaient cultivés comme cellules nageant librement dans le sérum humain, les mutants déficients en capsule et les variantes hyper‑visqueuses Wzc étaient bien plus facilement tués par le complément, un élément clé de notre système immunitaire inné. Pourtant, une fois organisés en biofilm, ces mêmes mutants étaient protégés de l'attaque du sérum. Dans un modèle d'infection utilisant des larves de ver à cire, certains mutants améliorés pour le biofilm sont devenus moins meurtriers, tandis que d'autres n'ont pas changé ou ont même augmenté en virulence. Cela montre que « plus de biofilm » ne signifie pas automatiquement « maladie plus sévère » ; la mutation précise importe.
Un reflet de ce qui se passe chez les patients
De manière frappante, beaucoup des mêmes gènes — et même des changements d'une seule lettre d'ADN identiques — observés chez les spécialistes du biofilm évolués en laboratoire ont également été trouvés dans des isolats de K. pneumoniae prélevés chez des patients lors d'une véritable flambée hospitalière, notamment dans des infections urinaires et des plaies liées aux cathéters. Ce recoupement étroit suggère que les surfaces de cathéters dans l'organisme exercent des pressions de sélection similaires à celles du laboratoire, favorisant progressivement des variantes meilleures pour s'accrocher, se regrouper et survivre sur les dispositifs. En parallèle, certaines de ces adaptations peuvent affaiblir la capacité des bactéries à provoquer une maladie invasive rapide, les orientant potentiellement vers la persistance et l'infection chronique. Comprendre ces compromis évolutifs peut aider à concevoir des dispositifs et des traitements qui perturbent les trajectoires favorables aux biofilms avant qu'elles ne s'installent.
Citation: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Mots-clés: Klebsiella pneumoniae, biofilms, infections associées aux cathéters, évolution bactérienne, résistance aux antibiotiques