Clear Sky Science · pl
Szybka ewolucja tworzących biofilm Klebsiella pneumoniae in vitro wyznacza adaptacyjne zmiany selekcjonowane podczas zakażenia
Dlaczego lepkie szpitalne zarazki mają znaczenie
Wiele zakażeń szpitalnych zaczyna się nie w naszych tkankach, lecz na plastikowych i silikonowych powierzchniach cewników, rur oddechowych i innych urządzeń medycznych. Na tych sztucznych powierzchniach bakterie takie jak Klebsiella pneumoniae mogą tworzyć śliskie, ochronne społeczności zwane biofilmami, które trudno usunąć i trudno leczyć antybiotykami. Badanie stawia proste, lecz kluczowe pytanie: jak szybko i w jaki sposób te powszechne szpitalne zarazki ewoluują, by lepiej tworzyć biofilmy na powierzchniach przypominających cewniki — i co to oznacza dla ich zdolności wywoływania choroby?
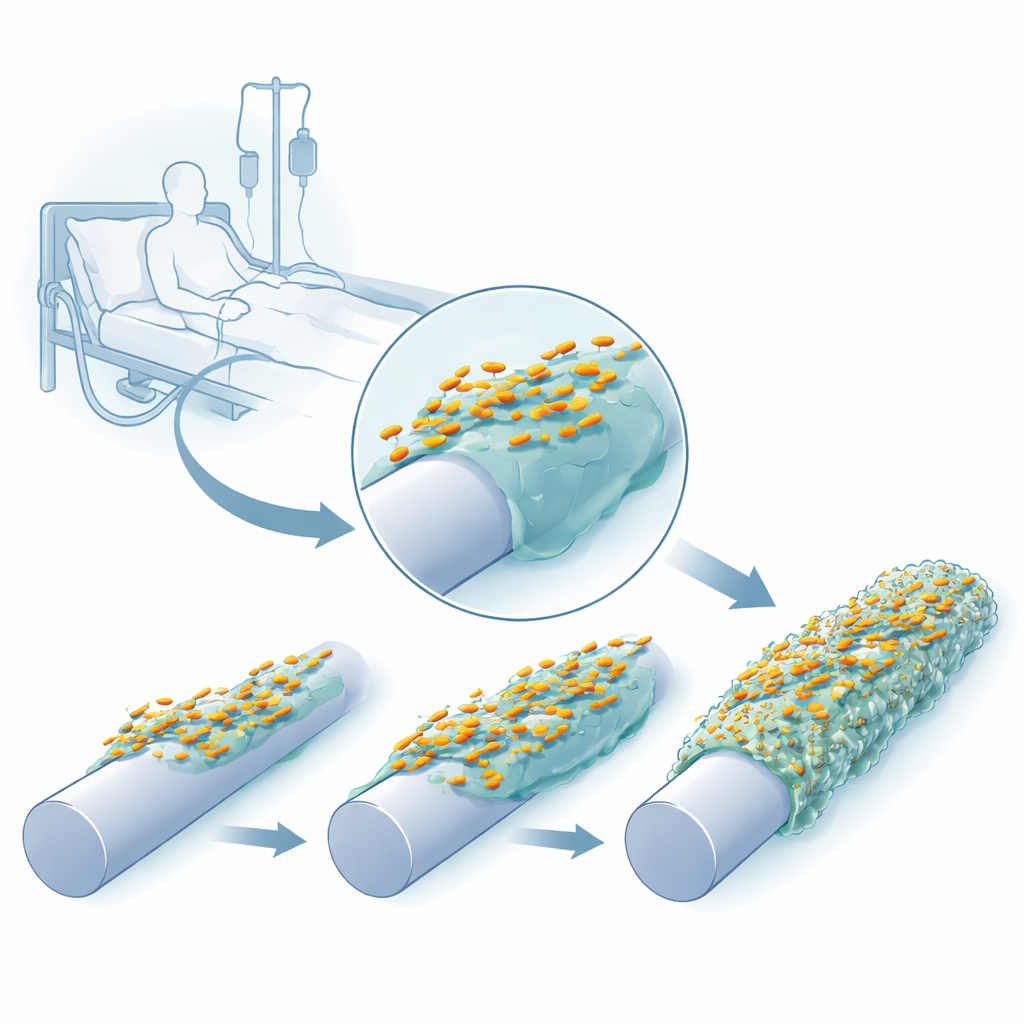
Śledzenie bakterii adaptujących się do plastiku
Naukowcy odtworzyli w laboratorium środowisko przypominające cewnik, używając urządzenia z bolcami, których powierzchnie pozostawiano gołe, pokryte silikonem lub pokryte zarówno silikonem, jak i ludzkim białkiem krwi — fibrynogenem — które naturalnie osadza się na założonych cewnikach. Wielokrotnie hodowali trzy szczepy kliniczne K. pneumoniae na tych bolcach, zbierali przylegające komórki i używali ich do rozpoczęcia kolejnego cyklu. Już po kilku cyklach wzrostu bakterie tworzyły grubsze, bardziej odporne biofilmy, a ich kolonie na agarze zaczęły wyglądać inaczej — niektóre stały się niezwykle śliskie i nitkowate, inne bardziej przezroczyste lub z pofałdowaną powierzchnią.
Genetyczne skróty do zwiększonej przyczepności
Sekwencjonując genom ponad stu wyewoluowanych klonów, zespół wykazał, że nowe fenotypy odzwierciedlały konkretne zmiany genetyczne, które wielokrotnie pojawiały się niezależnie w różnych liniach. Wiele mutacji dotyczyło systemu kapsuły — cukrowej powłoki, która zwykle pomaga bakteriom unikać ataku układu odpornościowego. Subtelne modyfikacje w kluczowym białku kapsuły (Wzc) dawały hiperśliskie, wysoce lepkie komórki, które rozprzestrzeniały się po powierzchniach pokrytych silikonem i fibrynogenem, podczas gdy inne mutacje całkowicie wyłączały produkcję kapsuły, prowadząc do niemal bezśliskich, lecz silnie adhezyjnych komórek. Drugim głównym celem była białkowa końcówka (MrkD) włosowatej struktury powierzchniowej (typ 3 fimbrii) działającej jak kotwica. Niewielkie zmiany strukturalne w tym białku albo zmiany w sieciach sygnalizacyjnych regulujących te fimbrie zwiększały wczesne przyczepianie i wpływały na sposób, w jaki biofilmy rozprzestrzeniały się i zbijały na różnych powierzchniach.
Biofilmy zbudowane z różnych elementów
Nie wszystkie wysoko wydajne biofilmy wyglądały lub działały tak samo. Niektóre mutanty polegały na grubej warstwie materiału kapsułowego, tworząc gładkie, ciągłe powłoki na powierzchni przypominającej cewnik. Inne, zwłaszcza te, które utraciły kapsułę lub przestawiły wewnętrzne sygnalizowanie poprzez małą cząsteczkę c‑di‑GMP, wytwarzały obfite włoski powierzchniowe i włókna celulozowe, które wiązały komórki w oddzielne skupiska. Mikroskopia elektronowa ujawniła, że te odrębne strategie tworzyły bardzo różne architektury: od jednolitych śluzowych powłok po łaciaste, wieżowate agregaty zatopione w włóknistej macierzy. To, która strategia przeważała, zależało zarówno od szczepu bakteryjnego, jak i rodzaju powierzchni, co podkreśla, że tło genetyczne i lokalne środowisko wspólnie kształtują ewolucję biofilmów.
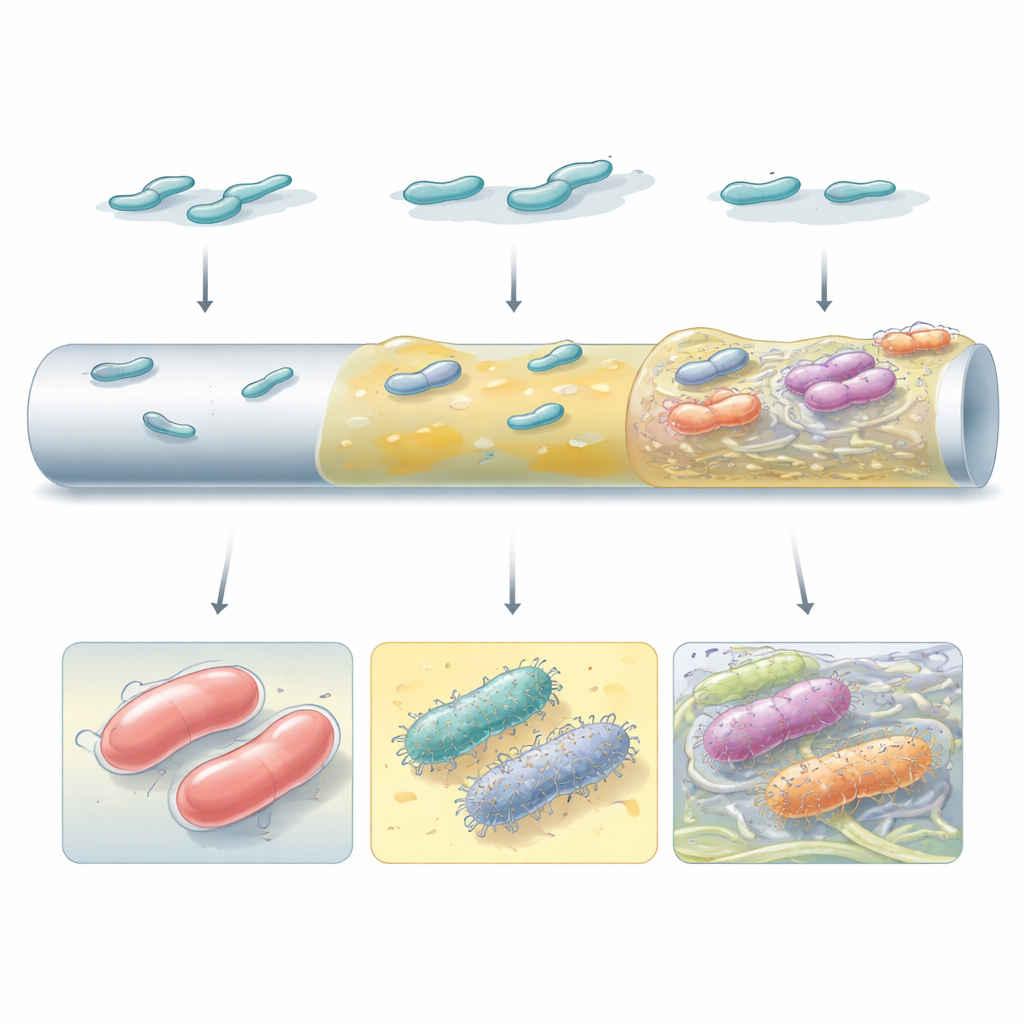
Kompromis między pozostawaniem a rażeniem
Lepsze tworzenie biofilmu wiązało się z ukrytymi kosztami. Hodowane jako wolnopływające komórki w ludzkim surowicy, zarówno mutanty pozbawione kapsuły, jak i hiperśliskie warianty Wzc były znacznie łatwiej zabijane przez dopełniacz — kluczowy element wrodzonej odporności. Jednak zorganizowane w biofilm te same mutanty były chronione przed atakiem surowicy. W modelu zakażenia z użyciem larw ćmy woskowej niektóre mutanty wzmocnione pod względem biofilmu stały się mniej zabójcze, podczas gdy inne nie zmieniły śmiertelności, a niektóre wręcz zwiększyły wirulencję. Pokazuje to, że „więcej biofilmu” nie oznacza automatycznie „poważniejszej choroby”; istotna jest konkretna mutacja.
Odwzorowanie tego, co dzieje się u pacjentów
Co zaskakujące, wiele z tych samych genów — a nawet identyczne jednoznakowe zmiany DNA — wykryto również w izolatach K. pneumoniae pochodzących od pacjentów podczas rzeczywistego ogniska szpitalnego, szczególnie w zakażeniach dróg moczowych i ran związanych z cewnikami. To bliskie pokrycie sugeruje, że powierzchnie cewników w organizmie wywierają podobne naciski selekcyjne jak te w laboratorium, stopniowo faworyzując warianty lepiej przylegające, grupujące się i przetrwające na urządzeniach. Jednocześnie niektóre z tych adaptacji mogą osłabiać zdolność bakterii do wywoływania szybkich, inwazyjnych zakażeń, potencjalnie przesuwając je w stronę utrzymywania się i przewlekłego zakażenia. Zrozumienie tych ewolucyjnych kompromisów może pomóc w projektowaniu urządzeń i terapii, które zakłócą sprzyjające biofilmom ścieżki, zanim się utrwalą.
Cytowanie: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Słowa kluczowe: Klebsiella pneumoniae, biofilmy, zakażenia związane z cewnikami, ewolucja bakterii, oporność na antybiotyki