Clear Sky Science · tr
Klebsiella pneumoniae biyofilmlerinin in vitro hızlı evrimi, enfeksiyon sırasında seçilen adaptif değişiklikleri belirliyor
Neden yapışkan hastane mikropları önemli?
Birçok hastane enfeksiyonu dokularımızda değil, kateterler, solunum tüpleri ve diğer tıbbi cihazların plastik veya silikon yüzeylerinde başlar. Bu yapay yüzeylerde Klebsiella pneumoniae gibi bakteriler, uzaklaştırılması zor ve antibiyotiklerle tedavisi güç olan koruyucu, sümüksü topluluklar olan biyofilmler oluşturabilir. Bu çalışma basit ama hayati bir soruyu gündeme getiriyor: bu yaygın hastane mikropları, kateter benzeri yüzeylerde biyofilm oluşturma yeteneklerini daha iyi hâle getirmek için ne kadar hızlı ve hangi yollarla evrimleşiyor—ve bunun hastalık yapma kapasiteleri için anlamı nedir?
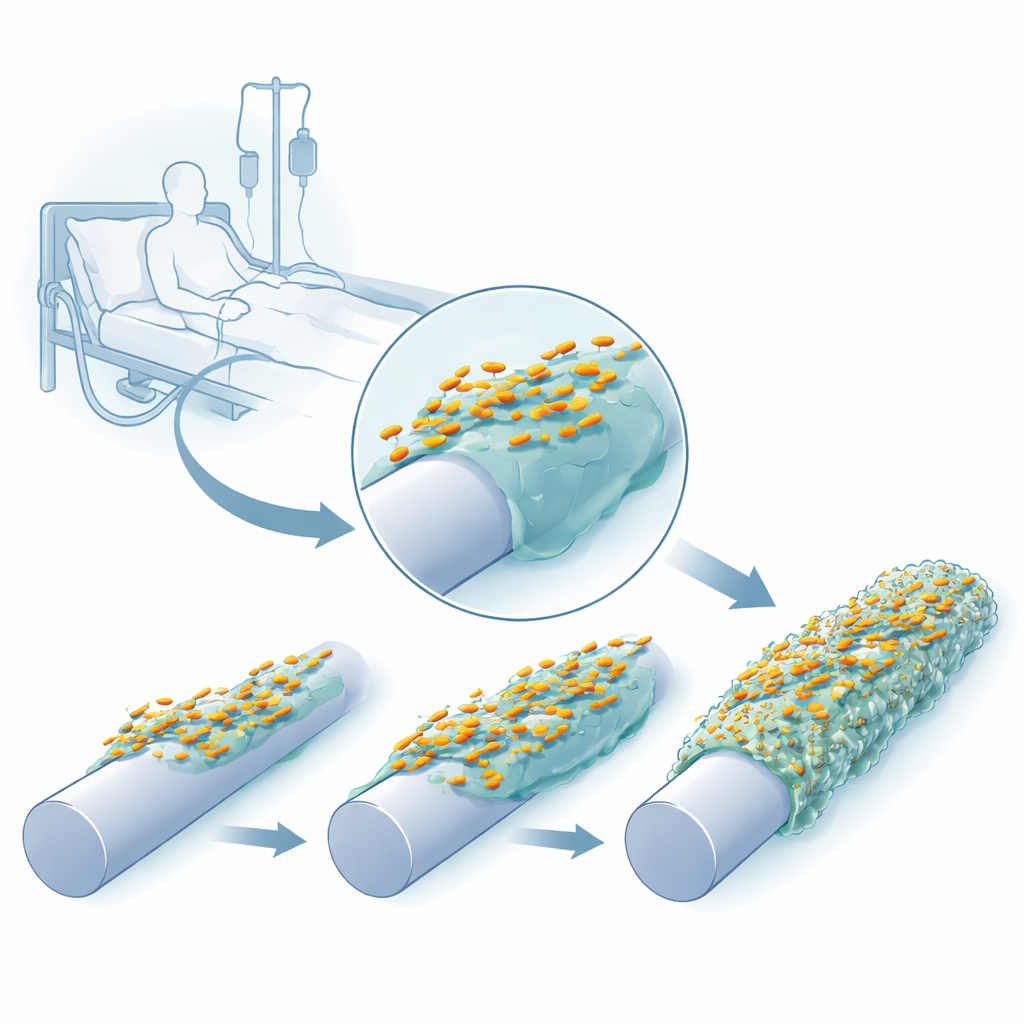
Bakterileri plastik üzerinde uyum sağlarken izlemek
Araştırmacılar laboratuvarda, yüzeyleri çıplak bırakılabilecek, silikonla kaplanmış veya hem silikon hem de kateterlere doğal olarak biriken insan kan proteini fibrinojen ile kaplanmış bir peg cihazı kullanarak kateter benzeri bir ortamı yeniden oluşturdu. Üç klinik K. pneumoniae suşunu bu peglerde tekrar tekrar büyüttüler, yapışmış hücreleri topladılar ve sonraki döngüyü başlatmak için kullandılar. Sadece birkaç büyüme döngüsü içinde bakteriler daha kalın, daha dayanıklı biyofilmler oluşturdu ve agar plaklarındaki kolonileri farklı görünmeye başladı—bazıları olağanüstü sümüksü ve ipliksi hale gelirken, diğerleri daha saydamlaşmış veya kırışık yüzeyler oluşturuyordu.
Daha yapışkan olmanın genetik kestirme yolları
Yüzün üzerinde yüz küsur evrimleşmiş klonun genomlarını dizileyerek ekip, bu yeni görünümlerin bağımsız soy hatlarında tekrar tekrar ortaya çıkan belirli genetik değişiklikleri yansıttığını gösterdi. Birçok mutasyon, bakterinin normalde bağışık saldırılarından kaçmasına yardımcı olan şekerli bir örtü olan kapsül sistemini hedef aldı. Anahtar bir kapsül proteini (Wzc) içindeki ince değişiklikler, silikon ve fibrinojen kaplı yüzeylerde yayılan hiper-sümüksü, yüksek viskoziteli hücreler üretti; diğer mutasyonlar ise kapsül üretimini tamamen kapatarak sümüksü olmayan ama güçlü yapışkan hücreler ortaya çıkardı. İkinci önemli hedef, kanca gibi iş gören saç benzeri yüzey yapısının (tip 3 fimbrialar) uç proteini (MrkD) oldu. Bu proteindeki küçük yapısal ayarlamalar veya bu fimbriaları düzenleyen sinyal ağlarındaki değişiklikler erken tutunmayı artırdı ve biyofilmlerin farklı yüzeylerde nasıl yayıldığını ve kümelendiğini değiştirdi.
Farklı yapı taşlarından inşa edilen biyofilmler
Tüm yüksek performanslı biyofilmler aynı görünmüyor veya aynı şekilde çalışmıyordu. Bazı mutantlar, kateter benzeri yüzey üzerinde düzgün, kesintisiz katmanlar oluşturmak için kalın kapsül maddesine dayanıyordu. Özellikle kapsüllerini kaybetmiş veya küçük molekül c-di-GMP aracılığıyla iç sinyalizasyonu yeniden düzenlemiş olanlar, hücreleri ayrık kümeler halinde birbirine bağlayan bol miktarda yüzey tüyü ve selüloz lifleri üretti. Elektron mikroskopisi, bu farklı stratejilerin çok farklı mimariler yarattığını ortaya koydu: tekdüze sümüksü örtülerden lifli bir matrise gömülmüş yamalı, kule benzeri agregalara kadar. Hangi stratejinin öne çıktığı hem bakteriyel suşa hem de yüzey tipine bağlıydı; bu da genetik arka plan ile yerel çevrenin birlikte biyofilmlerin nasıl evrimleştiğini şekillendirdiğini vurguluyor.
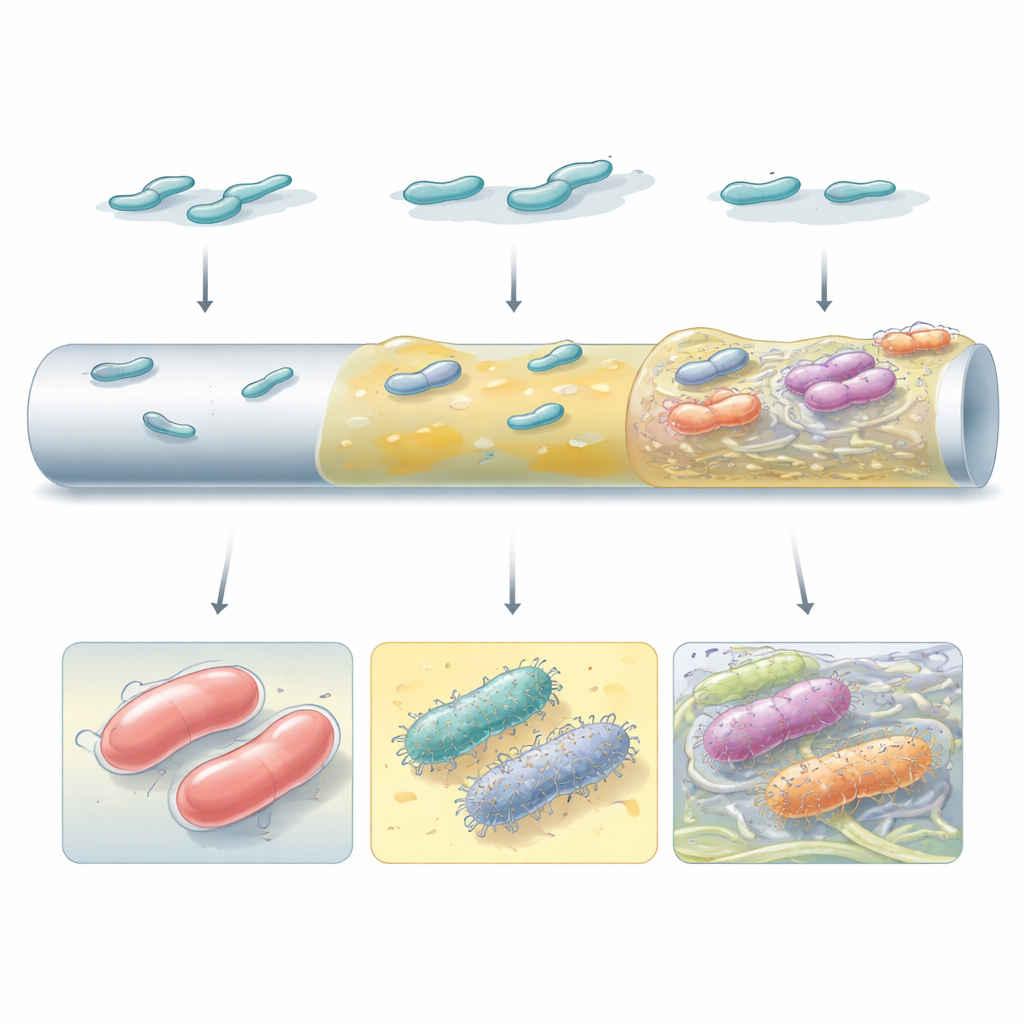
Orada kalmak ile sert vurmak arasında bir takas
Daha iyi bir biyofilm oluşturan hâle gelmenin gizli maliyetleri vardı. İnsan serumu içinde serbest yüzen hücreler olarak büyüdüklerinde, hem kapsül eksik mutantlar hem de hiper-sümüksü Wzc varyantları, doğuştan gelen bağışıklık sistemimizin önemli bir kolu olan kompleman tarafından çok daha kolay öldürüldü. Ancak aynı mutantlar bir biyofilm içinde organize olduklarında serum saldırısından korunuyordu. Balmumu güvesi larvaları kullanan bir enfeksiyon modelinde bazı biyofilm güçlendirilmiş mutantlar daha az öldürücü hale gelirken, diğerleri değişmedi veya hatta virülansı arttı. Bu, “daha fazla biyofilm”in otomatik olarak “daha şiddetli hastalık” anlamına gelmediğini; önemli olanın tam olarak hangi mutasyon olduğunun gösterdi.
Hastalar içinde olanlarla ayna tutmak
Çarpıcı bir şekilde, laboratuvarda evrimleşmiş biyofilm uzmanlarında görülen aynı genlerin—hatta bazen tek harflik DNA değişikliklerinin—birçok örneği, gerçek bir hastane salgını sırasında toplanan K. pneumoniae izolatlarında da bulundu; özellikle kateter içeren idrar yolu ve yara enfeksiyonlarından izole edilenlerde. Bu yakın örtüşme, vücut içindeki kateter yüzeylerinin laboratuvardakine benzer seçici baskılar uyguladığını ve cihazlarda tutunma, kümelenme ve hayatta kalma konusunda daha iyi olan varyantları sürekli olarak tercih ettiğini düşündürüyor. Aynı zamanda, bu adaptasyonların bazıları bakterinin hızlı, invaziv hastalık yapma yeteneğini zayıflatabilir; bu da onları kalıcılık ve kronik enfeksiyona doğru kaydırabilir. Bu evrimsel takasları anlamak, biyofilme elverişli yollar yerleşmeden önce bunları bozacak cihazlar ve tedaviler tasarlamada yardımcı olabilir.
Atıf: Zaborskytė, G., Coelho, P., Wrande, M. et al. Rapid evolution of Klebsiella pneumoniae biofilms in vitro delineates adaptive changes selected during infection. Nat Commun 17, 3454 (2026). https://doi.org/10.1038/s41467-026-71505-w
Anahtar kelimeler: Klebsiella pneumoniae, biyofilmler, kateter ilişkili enfeksiyonlar, bakteriyel evrim, antibiyotik direnci