Clear Sky Science · zh
通过亲和力组合平衡嵌合抗原受体T细胞疗法的疗效与安全性
这对未来癌症治疗的重要性
被工程化的免疫细胞——CAR T细胞——可以治愈某些血液系统恶性肿瘤,但它们也可能引发危险的副作用,并且有时在长期随访中疗效不足。本研究提出了一个看似简单但含义深远的问题:与其构建单一“超强”猎癌细胞,不如有意识地把对同一癌症靶点结合力强与弱的细胞混合,以更好地在杀伤力与安全性之间取得平衡,效果如何?
设计化免疫细胞如何抗癌
CAR T细胞是从患者体内分离出的常规T细胞,通过加入人工受体重新编程,使其能够识别并结合癌细胞表面的标志物并将其清除。大多数获批疗法针对B细胞表面的分子CD19,并采用远强于天然T细胞受体的结合能力。这种额外强的结合有助于识别并杀死癌细胞,但也会引发高度的激活反应,可能导致严重的免疫反应(如细胞因子释放综合征,CRS)、对健康细胞的损伤、CAR T细胞的早期耗竭,以及当肿瘤细胞丧失或降低CD19表达时的复发。
寻找受体强度的最佳区间
为探究结合强度如何影响CAR T行为,研究者把一种标准的高亲和力CD19 CAR(JCAR017)与一种低亲和力版本(JCAR021)进行了比较,并进一步构建了大量变体,其中一些的结合力更接近天然T细胞受体。在体外培养中,大多数这些CAR T细胞表现出出人意料的相似性:只要受体能稳定地展示在细胞表面,即便是结合力相当弱的变体仍然可以被激活、分泌关键免疫信号分子并杀死CD19阳性的靶细胞。只有那些非常弱、接近TCR样的变体在高挑战条件下(例如靶细胞仅携带极低量CD19)才开始表现出功能下降。
在生物体内会发生什么
当研究转入小鼠模型时,强弱结合体之间的差异变得更加明显。高亲和力的CAR T细胞扩增迅速,有效归巢到存在CD19阳性淋巴瘤细胞的骨髓,并且对肿瘤的控制最佳。低亲和力CAR虽然能延缓肿瘤生长,但很少能达到顶级表现者的效果,超弱结合体则大多无效。与此同时,强结合者引发的激活更强烈,T细胞分化更快,且——在具有重建免疫系统的人源化小鼠模型中尤为重要——出现剂量相关加重的类似CRS的疾病表现。
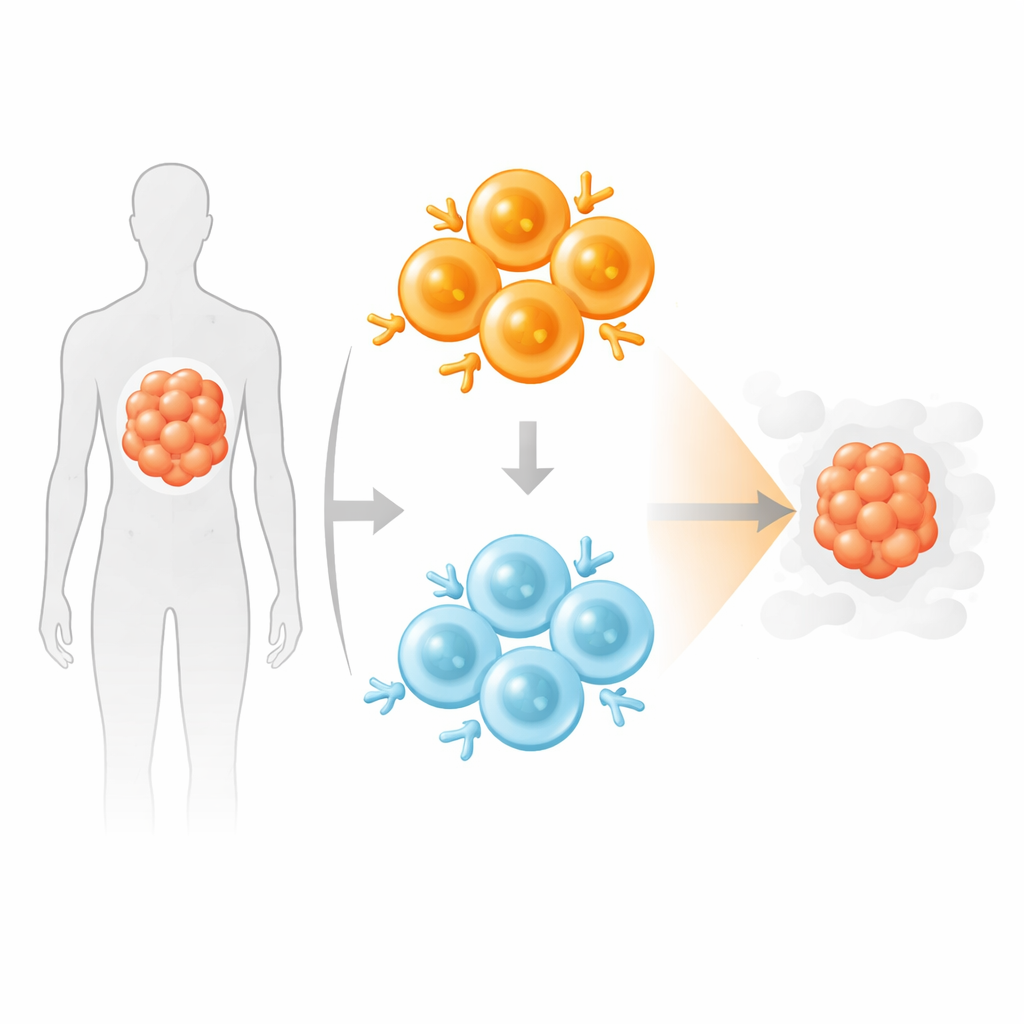
混合强力与温和的“猎手”
受到天然免疫系统同时动员高亲和力与低亲和力T细胞的启发,作者测试了一种“混合”CAR T产品,将等量的高亲和力与低亲和力CD19 CAR T细胞组合。在与癌细胞和人单核细胞的体外共培养中,这种混合产品以与足量高亲和力产品相当的效率杀死靶细胞,但释放的炎性细胞因子更少,其谱系类似于半剂量强CAR T细胞。在反复或慢性暴露于癌细胞的条件下,低亲和力CAR T细胞逐渐成为混合群体的优势群体,而单独使用的高亲和力CAR T细胞则表现出更多耗竭和应激标记。
混合如何改变长期行为
在带瘤小鼠中,混合产品再次总体表现最佳。高亲和力CAR T细胞仍然不可或缺:单独的低亲和力CAR即便在更高剂量下也无法完全清除肿瘤。但当以固定总剂量同时转移高亲和力与低亲和力细胞时,肿瘤缩小得更快、更彻底,相较于仅使用相同数量的高亲和力细胞。对回收的CAR T细胞进行单细胞RNA测序显示,混合组中的高亲和力细胞表达较少与耗竭和终末分化相关的基因,而更多表达与持续细胞毒功能和组织驻留相关的基因。这表明低亲和力的搭档细胞可能帮助“分担”抗原识别的负荷,限制对最强结合者的过度刺激。
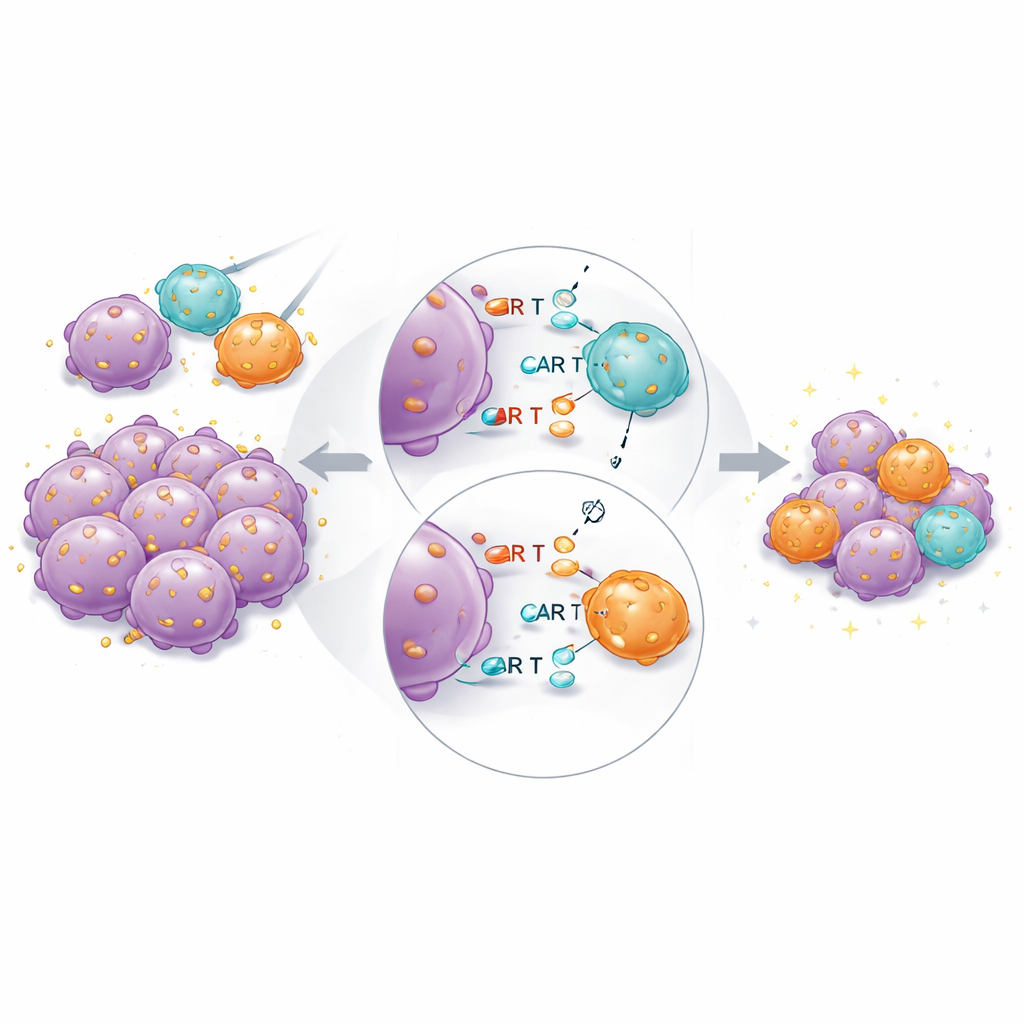
对患者意味着什么
这项研究表明,对于现有设计而言,CAR结合力存在一个实际的下限,低于该下限便无法有效工作;同时,能够最大限度杀伤肿瘤的结合强度往往也会放大毒性和耗竭。与其追求单一“完美”亲和力,不如将对同一癌症标志物具有不同结合强度的CAR T细胞混合,作为一种有前景的策略。在这一策略中,高亲和力细胞提供快速而强劲的攻击,而低亲和力细胞有助于抑制失控的炎症并维持长期控制。如果能在临床试验中得到验证,并扩展到CD19以外的其他靶点,这类亲和力组合的CAR T产品有望扩大治疗窗——使细胞疗法更安全、更持久,并适用于更广泛的癌症类型。
引用: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
关键词: CAR T细胞疗法, CD19, 受体亲和力, 细胞因子释放综合征, 癌症免疫治疗