Clear Sky Science · pl
Zrównoważenie skuteczności i bezpieczeństwa terapii limfocytami T z chimerycznym receptorem antygenowym przez łączenie powinowactw
Dlaczego to ma znaczenie dla przyszłej opieki onkologicznej
Zmodyfikowane komórki układu odpornościowego zwane limfocytami CAR T potrafią wyleczyć niektóre nowotwory krwi, ale mogą też wywoływać groźne skutki uboczne i czasem zawodzą w dłuższej perspektywie. W tym badaniu zadano pozornie proste pytanie o dużych implikacjach: zamiast tworzyć jedną „super-silną” komórkę tropiącą nowotwór, co się stanie, jeśli celowo zmieszamy komórki o silniejszym i słabszym wiązaniu z tym samym celem nowotworowym, aby lepiej wyważyć moc i bezpieczeństwo?
Jak zaprojektowane komórki odpornościowe zwalczają nowotwory
CAR T to zwykłe limfocyty T pobrane od pacjenta, przeprogramowane poprzez wprowadzenie sztucznego receptora, dzięki któremu mogą rozpoznawać markery na komórkach nowotworowych i je niszczyć. Większość zatwierdzonych terapii celuje w cząsteczkę CD19 na limfocytach B i używa receptorów, które wiążą ten marker o wiele mocniej niż naturalne receptory T. To dodatkowo silne wiązanie pomaga rozpoznawać i zabijać komórki nowotworowe, ale także napędza bardzo intensywną aktywację. Może to prowadzić do ciężkich reakcji immunologicznych, takich jak zespół uwalniania cytokin (CRS), uszkodzenia zdrowych komórek, wczesnego wyczerpania limfocytów CAR T oraz nawrotów nowotworu, gdy komórki nowotworowe tracą lub obniżają ekspresję CD19.
Poszukiwanie optymalnej siły wiązania
Aby zbadać, jak siła wiązania kształtuje zachowanie CAR T, autorzy porównali standardowy CAR przeciw CD19 o wysokim powinowactwie (JCAR017) z wersją o niższym powinowactwie (JCAR021), a następnie skonstruowali dużą panel dalszych wariantów, niektóre z wiązaniem bardziej przypominającym naturalny receptor T. W hodowlach laboratoryjnych większość tych CAR T wyglądała zaskakująco podobnie: dopóki receptor był stabilnie obecny na powierzchni komórki, nawet dość słabe wiążące warianty potrafiły się aktywować, wydzielać kluczowe mediatory odpornościowe i zabijać cele z ekspresją CD19. Tylko najsłabsze, przypominające TCR warianty zaczynały wykazywać obniżoną funkcję w wymagających warunkach, na przykład gdy komórki docelowe miały bardzo mało CD19.
Co się dzieje w żywych organizmach
Gdy zespół przeniósł badania do modeli mysich, różnice między silnymi a słabymi wiązaczami stały się znacznie bardziej wyraźne. CAR T o wysokim powinowactwie namnażały się szybko, sprawnie przemieszczając się do szpiku kostnego, gdzie znajdowały się komórki chłoniaka z CD19, i najlepiej kontrolowały guzy. CAR o niższym powinowactwie opóźniały wzrost guza, ale rzadko dorównywały najlepszym, a ultra-słabe warianty były w dużej mierze nieskuteczne. Jednocześnie silne wiązania napędzały intensywniejszą aktywację, szybszą differentiację komórek T i — co istotne w zhumanizowanym modelu myszy z odbudowanym układem odpornościowym — poważniejsze objawy przypominające CRS, które nasilały się wraz ze wzrostem dawki CAR T.
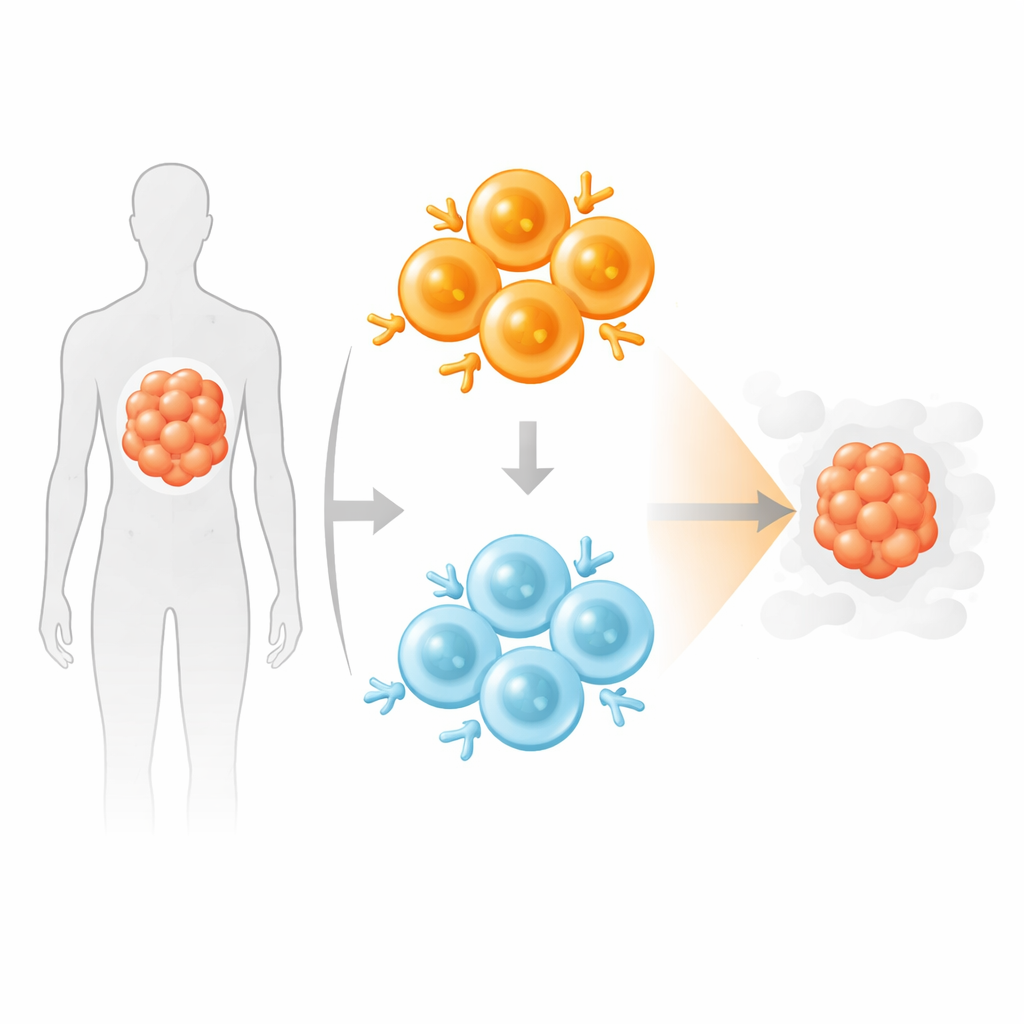
Mieszanie silnych i łagodnych łowców
Zainspirowani tym, jak nasz naturalny układ odpornościowy rekrutuje mieszankę limfocytów o wysokim i niskim powinowactwie, autorzy przetestowali „mieszany” produkt CAR T, który łączył równe liczby komórek o wysokim i niskim powinowactwie przeciw CD19. W hodowlach z komórkami nowotworowymi i ludzkimi monocytami produkty mieszane zabijały cele równie skutecznie jak pełna dawka produktu o wysokim powinowactwie, ale wydzielały mniej prozapalnych cytokin, przypominając profil półdawki silnych CAR T. Przy powtarzającej się lub przewlekłej ekspozycji na komórki nowotworowe komórki o niskim powinowactwie stopniowo stawały się dominującą populacją w mieszance, podczas gdy same komórki o wysokim powinowactwie wykazywały więcej markerów wyczerpania i stresu.
Jak mieszanka zmienia zachowanie w długim terminie
U myszy z guzami produkt łączony ponownie wypadł najlepiej ogólnie. Komórki o wysokim powinowactwie wciąż były niezbędne: same komórki o niskim powinowactwie nie radziły sobie z pełnym oczyszczeniem guzów, nawet przy wyższych dawkach. Jednak gdy komórki o wysokim i niskim powinowactwie podawano razem przy stałej łącznej dawce, guzy kurczyły się szybciej i bardziej kompletne niż przy tej samej liczbie jedynie komórek o wysokim powinowactwie. Sekwencjonowanie RNA pojedynczych komórek odzyskanych CAR T wykazało, że komórki o wysokim powinowactwie w grupach mieszanych wyrażały mniej genów związanych z wyczerpaniem i terminalną różnicą oraz więcej genów kojarzonych z trwałą funkcją cytotoksyczną i przebywaniem w tkankach. Sugeruje to, że komórki o niskim powinowactwie pomagają „dzielić obciążenie” rozpoznawania antygenu, ograniczając nadmierną stymulację najsilniejszych wiążących.
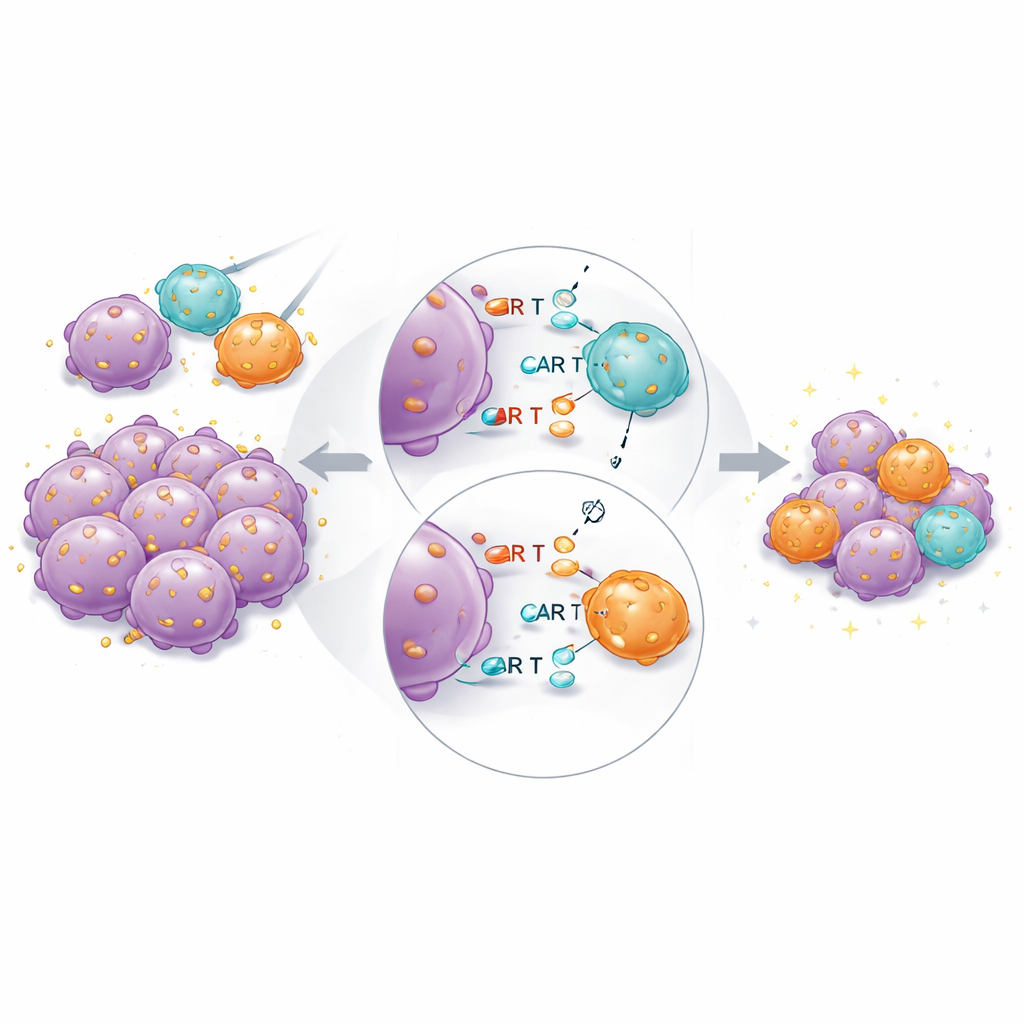
Co to oznacza dla pacjentów
Badanie pokazuje, że istnieje praktyczny dolny próg, jak słabo CAR może wiązać i nadal dobrze działać w obecnych projektach, oraz że powinowactwo maksymalizujące zabijanie guza zwykle też potęguje toksyczność i wypalenie. Zamiast szukać pojedynczego idealnego powinowactwa, mieszanie komórek CAR T o różnych siłach wiązania do tego samego markera nowotworowego wyłania się jako obiecująca strategia. W takim podejściu komórki o wysokim powinowactwie zapewniają szybki, potężny atak, podczas gdy komórki o niższym powinowactwie pomagają stłumić wymykające się spod kontroli zapalenie i podtrzymać długotrwałą kontrolę. Jeśli potwierdzą to badania kliniczne i rozszerzy na inne cele poza CD19, takie produkty CAR T łączące powinowactwa mogłyby poszerzyć okno terapeutyczne — czyniąc terapie komórkowe bezpieczniejszymi, trwalszymi i stosownymi w szerszym spektrum nowotworów.
Cytowanie: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Słowa kluczowe: terapia CAR T, CD19, powinowactwo receptora, zespół uwalniania cytokin, immunoterapia nowotworów