Clear Sky Science · de
Ausbalancieren von Wirksamkeit und Sicherheit der chimären Antigenrezeptor-T-Zelltherapie durch Affinitätskombination
Warum das für die künftige Krebsbehandlung wichtig ist
Ingenieurmäßig veränderte Immunzellen, sogenannte CAR-T-Zellen, können einige Blutkrebserkrankungen heilen, sie können aber auch gefährliche Nebenwirkungen hervorrufen und langfristig versagen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenschwere Frage: Anstatt eine einzelne „superstarke“ Krebsjägerzelle zu bauen, was wäre, wenn man bewusst Zellen mit stärkerer und schwächerer Bindung an dasselbe Krebsziel mischt, um Schlagkraft und Sicherheit besser auszubalancieren?
Wie Designer-Immunzellen Krebs bekämpfen
CAR-T-Zellen sind normale T-Zellen eines Patienten, die mit einem künstlichen Rezeptor umprogrammiert werden, damit sie Marker auf Krebszellen erkennen und diese zerstören können. Die meisten zugelassenen Therapien zielen auf ein Molekül namens CD19 auf B-Zellen und verwenden Rezeptoren, die diesen Marker deutlich fester greifen als natürliche T-Zell-Rezeptoren. Diese besonders starke Bindung hilft, Krebszellen zu erkennen und zu töten, führt aber auch zu intensiver Aktivierung. Das kann zu schweren Immunreaktionen wie dem Zytokinfreisetzungssyndrom (CRS), Schäden an gesunden Zellen, frühzeitiger Erschöpfung der CAR-T-Zellen und Rückfällen führen, wenn Tumorzellen CD19 verlieren oder reduzieren.
Die richtige Stärke des Rezeptors finden
Um zu untersuchen, wie die Bindungsstärke das Verhalten von CAR-T-Zellen prägt, verglichen die Forschenden einen standardmäßigen hochaffinen CD19-CAR (JCAR017) mit einer niedrigeren Affinitätsversion (JCAR021) und entwickelten anschließend ein großes Panel weiterer Varianten, einige mit Bindungseigenschaften ähnlich natürlichen T-Zell-Rezeptoren. In Zellkulturen sahen die meisten dieser CAR-T-Zellen überraschend ähnlich aus: Solange der Rezeptor stabil an der Zelloberfläche vorhanden war, konnten selbst ziemlich schwache Binder noch aktivieren, wichtige Immunbotenstoffe ausschütten und CD19-positive Zielzellen töten. Nur die allerunschärfsten, TCR-ähnlichen Varianten zeigten unter anspruchsvollen Bedingungen reduzierte Funktion, etwa wenn Zielzellen nur sehr wenig CD19 trugen.
Was in lebenden Organismen passiert
Als das Team in Mausmodelle wechselte, wurden die Unterschiede zwischen starken und schwachen Bindern deutlich ausgeprägter. Hochaffine CAR-T-Zellen expandierten zügig, wanderten effizient ins Knochenmark, wo sich CD19-positive Lymphomzellen befanden, und kontrollierten die Tumoren am besten. Niedrigaffine CARs verzögerten das Tumorwachstum, erreichten aber selten die Leistung des Spitzenreiters, und ultraschwa-che Binder waren weitgehend unwirksam. Gleichzeitig führten die starken Binder zu intensiverer Aktivierung, schnellerer Differenzierung der T-Zellen und—wichtig in einem humanisierten Mausmodell mit rekonstituiertem Immunsystem—zu einer stärkeren CRS-ähnlichen Erkrankung, die sich mit steigender CAR-T-Zell-Dosis verschlimmerte.
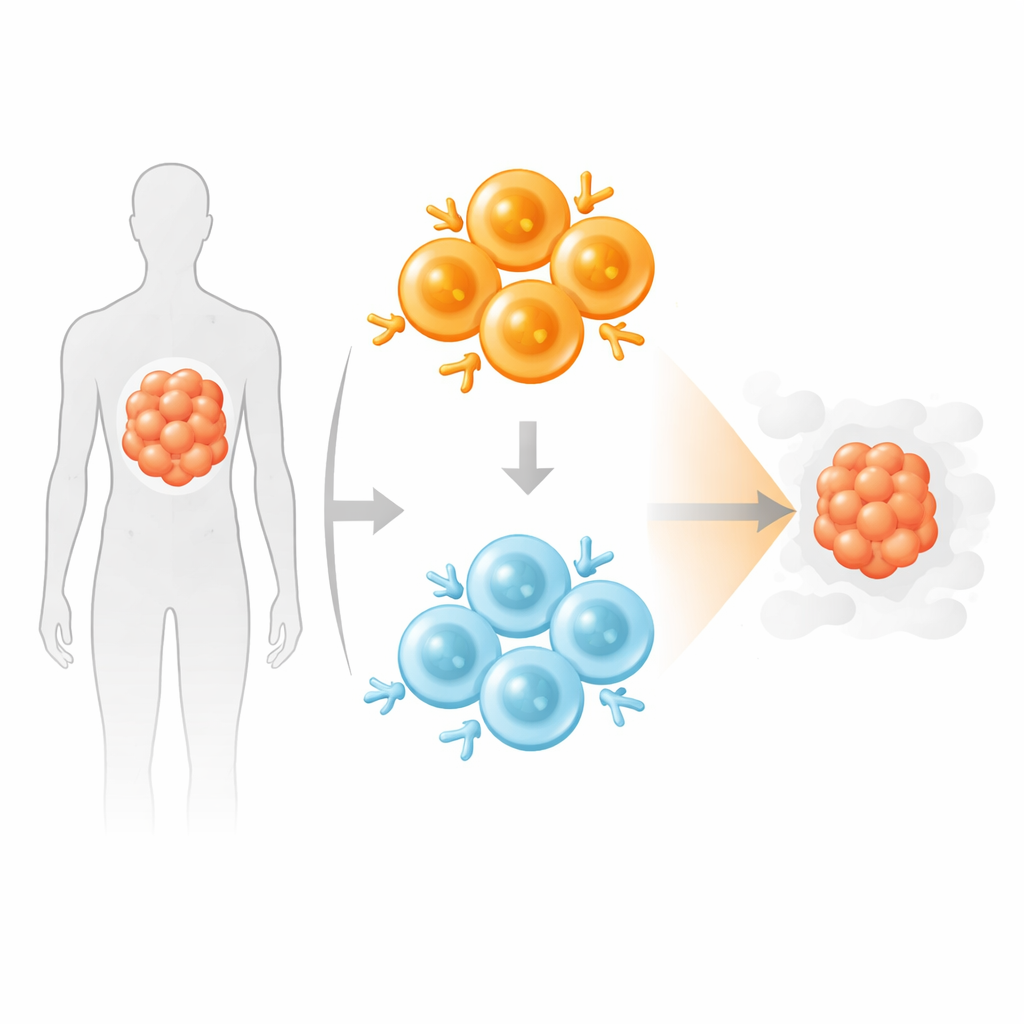
Starke und sanfte Jäger mischen
In Anlehnung an die natürliche Immunantwort, die eine Mischung aus hoch- und niedrigaffinen T-Zellen rekrutiert, testeten die Autoren ein „geblendetetes“ CAR-T-Produkt, das gleiche Anzahlen hoch- und niedrigaffiner CD19-CAR-T-Zellen kombinierte. In Laborkokulturen mit Krebszellen und humanen Monozyten töteten diese Mischprodukte Ziele genauso effektiv wie eine volle Dosis hochaffiner Zellen, setzten jedoch weniger entzündungsfördernde Zytokine frei und ähnelten damit dem Profil einer halben Dosis starker CAR-T-Zellen. Bei wiederholter oder chronischer Exposition gegenüber Krebszellen wurde in der Mischung allmählich die niedrigaffine Population dominant, während hochaffine CAR-T-Zellen allein stärker Erschöpfungs- und Stressmarker zeigten.
Wie Mischung das Langzeitverhalten verändert
Bei tumorbefallenen Mäusen schnitt das kombinierte Produkt erneut insgesamt am besten ab. Hochaffine CAR-T-Zellen blieben entscheidend: Niedrigaffine CARs allein konnten Tumoren selbst bei höheren Dosen nicht vollständig beseitigen. Wenn jedoch hoch- und niedrigaffine Zellen zusammen bei gleicher Gesamtdosis übertragen wurden, schrumpften die Tumoren schneller und vollständiger als bei der gleichen Anzahl hochaffiner Zellen allein. Einzelzell-RNA-Sequenzierung der rekrutierten CAR-T-Zellen offenbarte, dass hochaffine Zellen in den gemischten Gruppen weniger Gene exprimierten, die mit Erschöpfung und terminaler Differenzierung assoziiert sind, und mehr Gene, die mit anhaltender zytotoxischer Funktion und Gewebeverweildauer verknüpft sind. Das deutet darauf hin, dass niedrigaffine Partnerzellen helfen, die Antigenerkennung „mitzutragen“ und eine Überstimulation der stärksten Binder zu begrenzen.
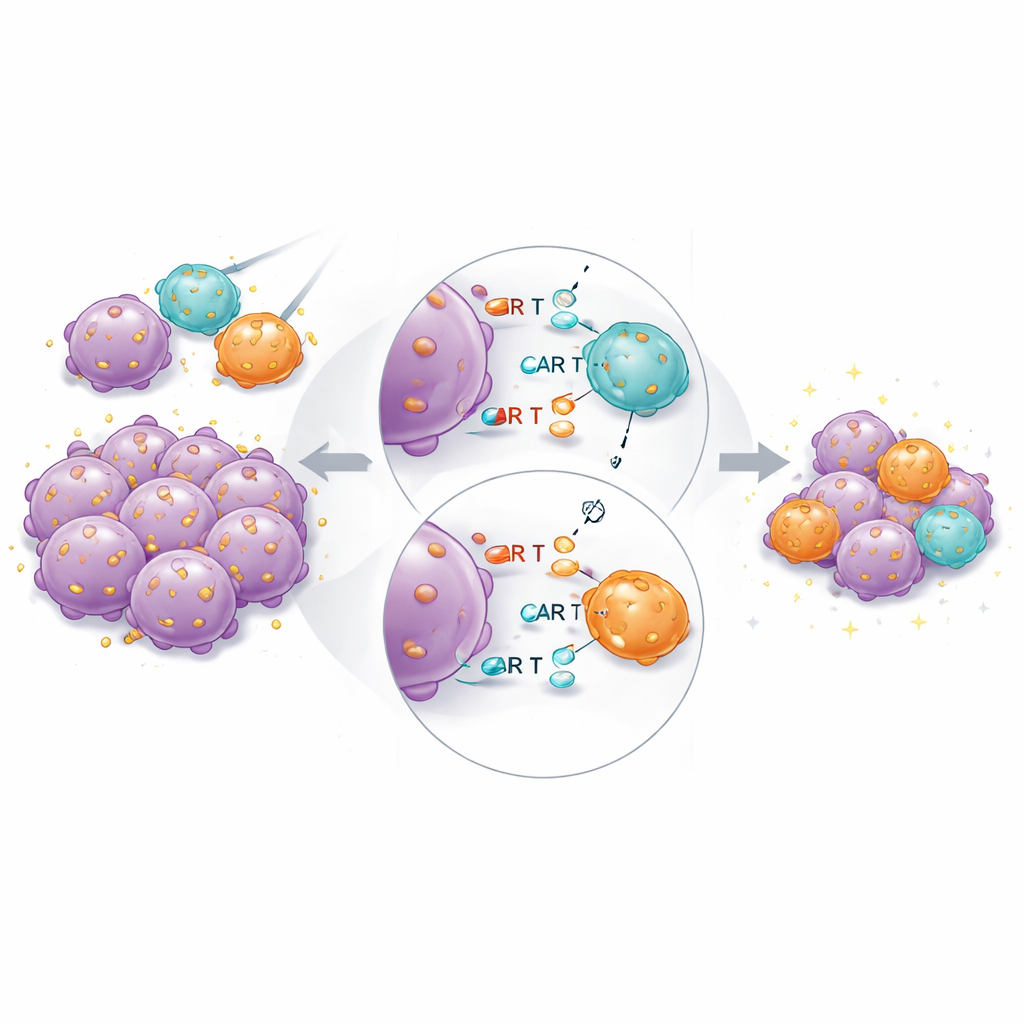
Was das für Patientinnen und Patienten bedeutet
Die Studie zeigt, dass es eine praktische Untergrenze dafür gibt, wie schwach ein CAR binden kann und immer noch in aktuellen Designs gut funktioniert, und dass die Bindungsstärke, die das Tumorkilling maximiert, tendenziell auch Toxizität und Erschöpfung verstärkt. Statt nach einer einzelnen perfekten Affinität zu suchen, erweist sich das Mischen von CAR-T-Zellen mit unterschiedlicher Bindungsstärke gegen denselben Krebsmarker als vielversprechende Strategie. Dabei liefern hochaffine Zellen einen schnellen, kraftvollen Angriff, während niedrigaffine Zellen helfen, die eskalierende Entzündungsreaktion zu dämpfen und eine langfristige Kontrolle aufrechtzuerhalten. Wenn dies in klinischen Studien bestätigt und auf andere Ziele als CD19 ausgeweitet wird, könnten derartige affinitätskombinierte CAR-T-Produkte das therapeutische Fenster erweitern—und Zelltherapien sicherer, langlebiger und für ein breiteres Spektrum von Krebserkrankungen geeignet machen.
Zitation: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Schlüsselwörter: CAR-T-Zelltherapie, CD19, Rezeptoraffinität, Zytokinsturm (CRS), Krebsimmuntherapie