Clear Sky Science · nl
Balanceren van de werkzaamheid en veiligheid van chimere antigeenreceptor T-celtherapie door affiniteitcombinatie
Waarom dit belangrijk is voor toekomstige kankerzorg
Gemanipuleerde immuuncellen, zogeheten CAR T-cellen, kunnen sommige bloedkankers genezen, maar ze kunnen ook gevaarlijke bijwerkingen veroorzaken en soms op de lange termijn falen. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote gevolgen: in plaats van één "supersterke" cel die kanker opspoort, wat als we opzettelijk cellen met sterkere en zwakkere binding aan hetzelfde kankermarker mengen om zo kracht en veiligheid beter in balans te brengen?
Hoe ontworpen immuuncellen kanker bestrijden
CAR T-cellen zijn gewone T-cellen van een patiënt die worden geherprogrammeerd met een kunstmatige receptor, zodat ze zich kunnen hechten aan merkers op kankercellen en die kunnen vernietigen. De meeste goedgekeurde therapieën richten zich op een molecuul dat CD19 heet op B-cellen en gebruiken receptoren die dit merker veel steviger vastgrijpen dan natuurlijke T-celreceptoren. Die extra sterke binding helpt bij het herkennen en doden van kankercellen, maar zorgt ook voor zeer intense activatie. Dit kan leiden tot ernstige immuunreacties zoals cytokine release syndrome (CRS), schade aan gezonde cellen, voortijdige uitputting van de CAR T-cellen en kankerrecidieven wanneer tumorcellen CD19 verliezen of verminderen.
Het vinden van de juiste receptorsterkte
Om te onderzoeken hoe bindingssterkte het gedrag van CAR T beïnvloedt, vergeleken de onderzoekers een standaard hoge-affiniteits CD19 CAR (JCAR017) met een versie met lagere affiniteit (JCAR021) en maakten vervolgens een groot aantal verdere varianten, sommige met binding die meer leek op een natuurlijke T-celreceptor. In kweekschalen leken de meeste van deze CAR T-cellen verrassend vergelijkbaar: zolang de receptor stabiel op het celoppervlak aanwezig was, konden zelfs tamelijk zwakke binders nog activeren, belangrijke immuunboodschappers uitscheiden en CD19-positieve doelcellen doden. Alleen de allerkleinste, TCR-achtige varianten begonnen verminderde functies te vertonen onder veeleisende omstandigheden, zoals wanneer doelcellen zeer weinig CD19 droegen.
Wat er gebeurt in levende organismen
Toen het team overstapte naar muismodellen, werden de verschillen tussen sterke en zwakke binders veel duidelijker. Hoge-affiniteits CAR T-cellen breidden zich snel uit, gingen efficiënt naar het beenmerg waar CD19-positieve lymfoomcellen zich bevonden, en controleerden tumoren het best. Lager-affiniteits CARs vertraagden de tumorgroei maar haalden zelden de prestaties van de beste uit, en ultra-zwakke binders waren grotendeels ineffectief. Tegelijkertijd veroorzaakten de sterke binders intensere activatie, snellere differentiatie van T-cellen en—belangrijk in een gehumaniseerd muismodel met een gereconstitueerd immuunsysteem—ernstigere CRS-achtige ziektebeelden die verergerden naarmate de dosis CAR T-cellen toenam.
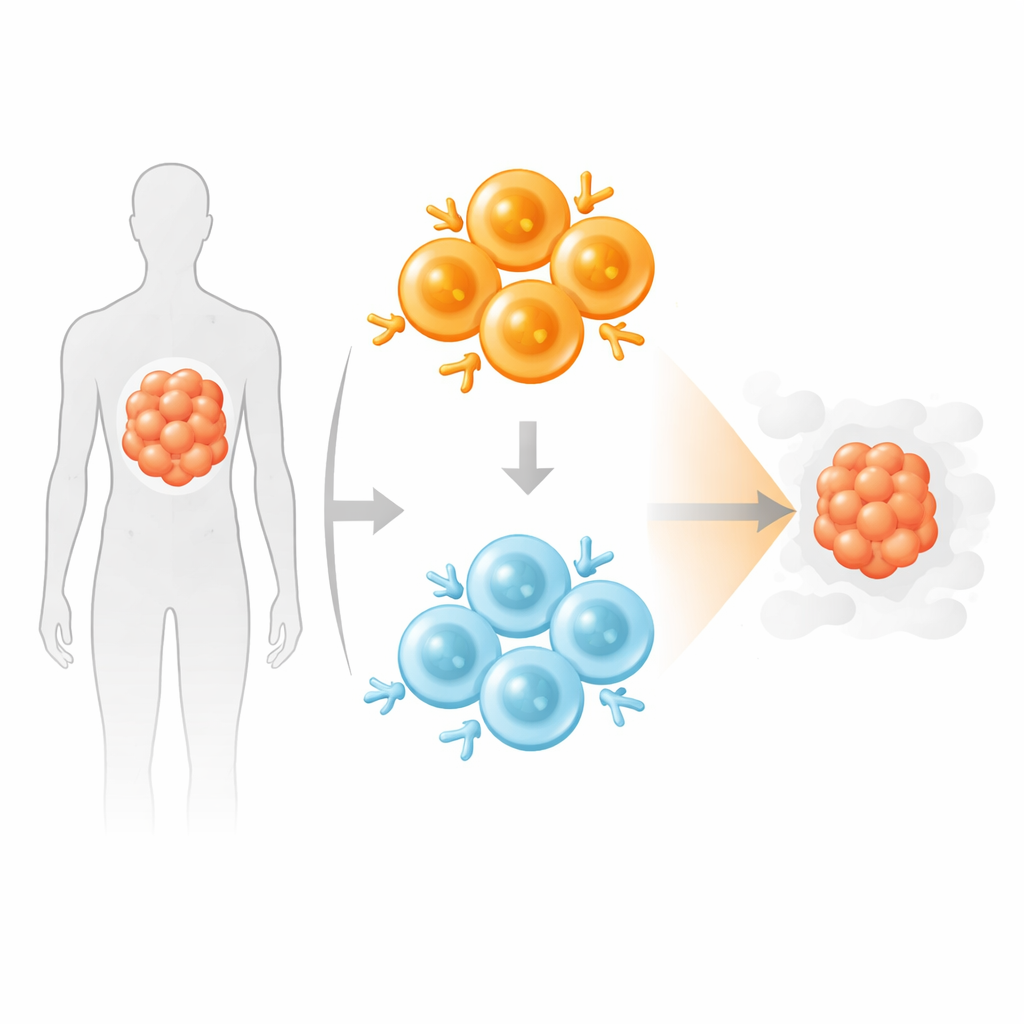
Meng sterke en milde jagers
Geïnspireerd door hoe ons natuurlijke immuunsysteem een mix van hoge- en lage-affiniteits T-cellen rekruteert, testten de auteurs een "geblend" CAR T-product dat gelijke aantallen hoge- en lage-affiniteits CD19 CAR T-cellen combineerde. In laboratoriumco-culturen met kankercellen en humane monocyten doodden deze gemengde producten doelcellen net zo effectief als een volledige dosis hoog-affiniteitsproduct, maar gaven ze minder ontstekingsbevorderende cytokines af, overeenkomend met het profiel van een halve dosis sterke CAR T-cellen. Bij herhaalde of chronische blootstelling aan kankercellen werden lage-affiniteits CAR T-cellen geleidelijk de dominante populatie in het mengsel, terwijl hoge-affiniteits CAR T-cellen alleen meer merkers van uitputting en stress toonden.
Hoe mengen het gedrag op lange termijn verandert
Bij muizen met tumoren presteerde het gecombineerde product opnieuw het beste overall. Hoge-affiniteits CAR T-cellen bleven essentieel: lage-affiniteits CARs alleen konden tumoren niet volledig uitroeien, zelfs niet bij hogere doses. Maar wanneer hoge- en lage-affiniteitscellen samen werden overgedragen bij vaste totale dosissen, krompen tumoren sneller en vollediger dan met hetzelfde aantal hoge-affiniteitscellen alleen. Enkelcel-RNA-sequencing van teruggewonnen CAR T-cellen toonde dat hoge-affiniteitscellen in de gemengde groepen minder genen tot expressie brachten die gekoppeld zijn aan uitputting en terminale differentiatie, en meer genen geassocieerd met aanhoudende cytotoxische functie en weefselresidentie. Dit suggereert dat lage-affiniteitspartnercellen helpen de last van antigeenherkenning te delen, waardoor overstimulatie van de sterkste binders wordt beperkt.
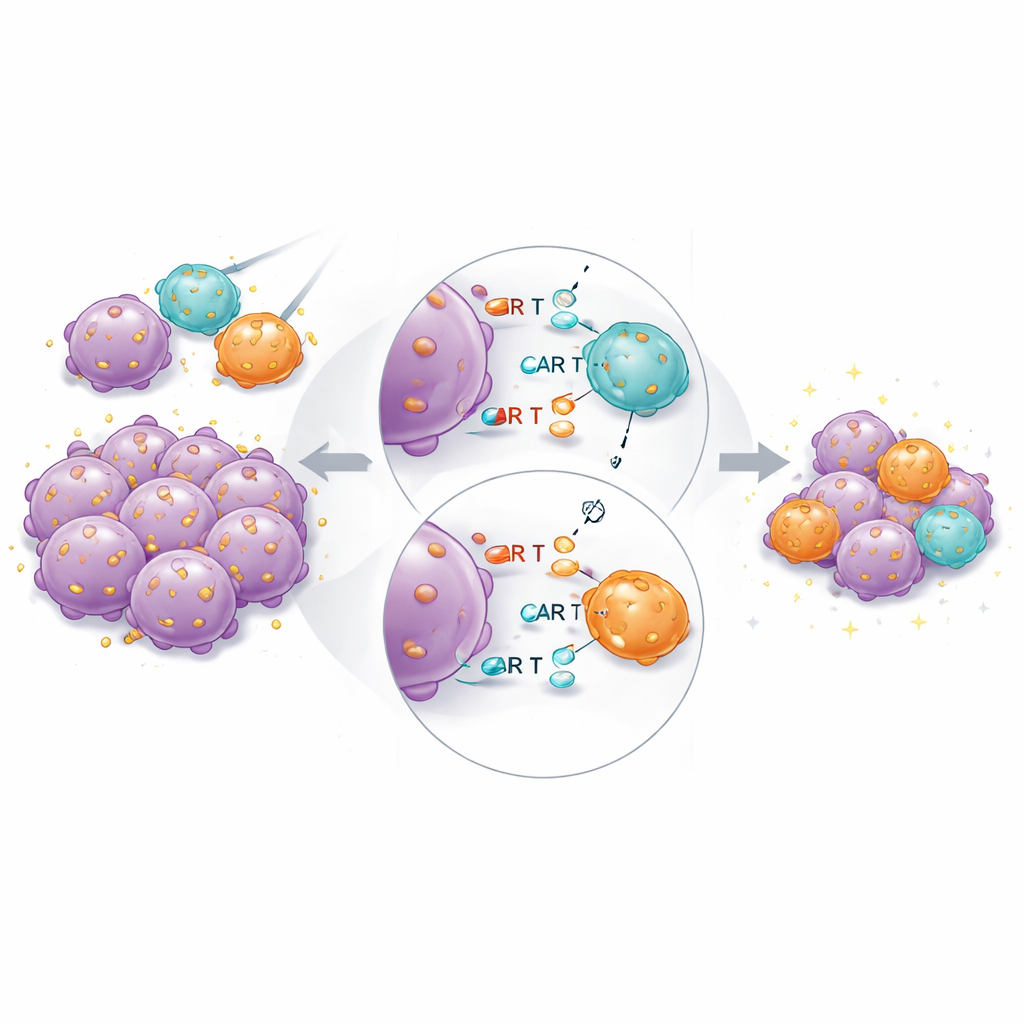
Wat dit betekent voor patiënten
De studie laat zien dat er een praktische ondergrens is voor hoe zwak een CAR kan binden en toch goed kan werken in de huidige ontwerpen, en dat bindingssterkte die de tumordoding maximaliseert ook de toxiciteit en uitputting vergroot. In plaats van te zoeken naar één perfecte affiniteit, komt het mengen van CAR T-cellen met verschillende bindingssterkten aan hetzelfde kankermarker naar voren als een veelbelovende strategie. In deze aanpak leveren hoge-affiniteitscellen een snelle, krachtige aanval, terwijl lagere-affiniteitscellen helpen woedende ontsteking te dempen en langdurige controle te ondersteunen. Als dit wordt bevestigd in klinische proefen en uitgebreid naar andere doelwitten buiten CD19, zouden dergelijke affiniteit-gecombineerde CAR T-producten het behandelvenster kunnen vergroten—waardoor celtherapieën veiliger, duurzamer en geschikt voor een bredere reeks kankers zouden worden.
Bronvermelding: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Trefwoorden: CAR T-celtherapie, CD19, receptoraffiniteit, cytokinestorm, kankerimmunotherapie