Clear Sky Science · ar
موازنة الفاعلية والسلامة في علاج الخلايا التائية ذات مستقبلات المستضد المهجنة عبر توليفة التماسك
لماذا هذا مهم لرعاية السرطان في المستقبل
الخلايا المناعية المهندسة المسماة خلايا CAR T يمكن أن تشفي بعض سرطانات الدم، لكنها قد تتسبب أيضاً في آثار جانبية خطيرة وأحياناً تفشل على المدى الطويل. تطرح هذه الدراسة سؤالاً بسيطاً ظاهرياً لكنه ذا تبعات كبيرة: بدل بناء خلية مفردة «شديدة القوة» لاصطياد السرطان، ماذا لو قمنا عمداً بخلط خلايا ذات ارتباط أقوى وأضعف لنفس هدف السرطان للحصول على توازن أفضل بين القوة والسلامة؟
كيف تقاتل الخلايا المناعية المصممة السرطان
خلايا CAR T هي خلايا تائية مأخوذة من مريض أُعيد برمجتها بمستقبل صناعي لتتمكن من الالتصاق بعلامات على خلايا السرطان وتدميرها. تستهدف معظم العلاجات المعتمدة جزيئاً يسمى CD19 على الخلايا البائية وتستخدم مستقبلات تقبض على هذه العلامة بقوة تفوق بكثير مستقبلات الخلايا التائية الطبيعية. هذه القوة الإضافية تساعدها على تمييز وخَلق خلايا السرطان، لكنها أيضاً تُحدث تنشيطاً شديداً. وقد يؤدي ذلك إلى تفاعلات مناعية حادة مثل متلازمة إطلاق السيتوكينات (CRS)، وإصابة الخلايا السليمة، واستنفاد مبكر لخلايا CAR T، وارتفاع احتمال انتكاس السرطان عندما تفقد الخلايا الورمية CD19 أو تقلل منه.
البحث عن نقطة التوازن في قوة المستقبل
لاستكشاف كيف يؤثر قوة الارتباط على سلوك خلايا CAR T، قارن الباحثون مستقبل CD19 CAR قياسي عالي التماسك (JCAR017) بنسخة أقل تماسكاً (JCAR021)، ثم صنّعوا لوحة واسعة من المتغيرات الإضافية، بعضها يقترب في تماسكه من مستقبل الخلايا التائية الطبيعي. في الأطباق المخبرية بدا أن معظم خلايا CAR T هذه متشابهة بشكل مدهش: طالما أن المستقبل معروض بثبات على سطح الخلية، حتى الرابطات الضعيفة جداً تمكنت من التفعيل وإفراز رُسُل مناعية رئيسية وقتل الخلايا المستهدفة الإيجابية لـ CD19. فقط المتغيرات الضعيفة جداً، الشبيهة بمستقبلات TCR، بدأت تُظهر وظائف مخفضة في ظروف متطلبة، مثل عندما تحمل الخلايا الهدفية كمية ضئيلة جداً من CD19.
ما الذي يحدث داخل الكائن الحي
عندما انتقل الفريق إلى نماذج الفئران، أصبحت الفروقات بين الرابطات القوية والضعيفة أكثر وضوحاً. توسعت خلايا CAR T عالية التماسك بسرعة، وتوجهت بكفاءة إلى نخاع العظم حيث كانت خلايا اللمفوما الإيجابية لـ CD19 موجودة، وكانت أفضل في السيطرة على الأورام. أجلت CARs الأقل تماسكاً نمو الورم لكنها نادراً ما نافست الأفضل أداءً، وكانت الرابطات فائقة الضعف غير فعالة إلى حد كبير. وفي الوقت نفسه، دفعت الرابطات القوية تنشيطاً أكثر حدة، وتمايزاً أسرع للخلايا التائية، و– والأهم في نموذج فأري مُؤنسَن ذو جهاز مناعي أعيد بناؤه—مرضاً أشبه بمتلازمة إطلاق السيتوكينات أكثر شدة ازداد سوءاً مع زيادة جرعة خلايا CAR T.
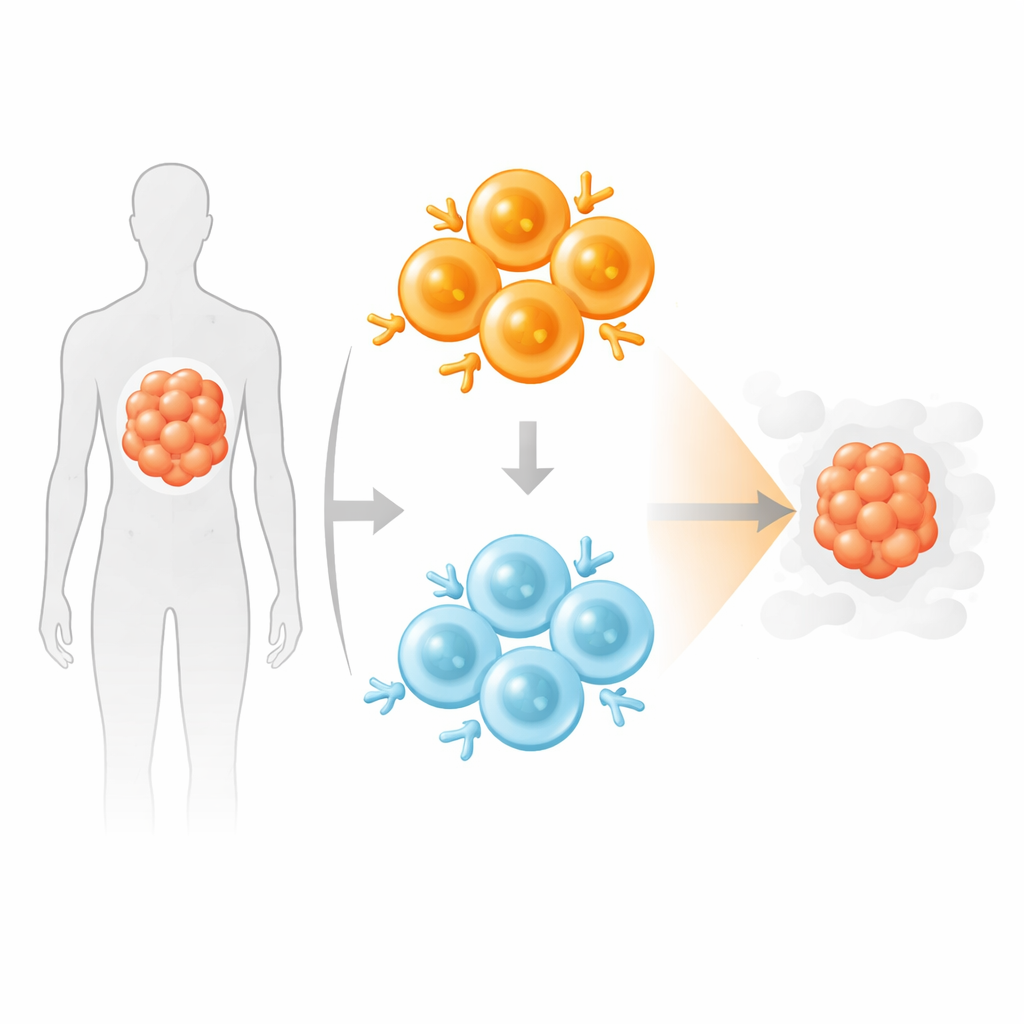
مزج الصيادين الأقوياء واللطيفين
مستوحين من طريقة عمل جهازنا المناعي الطبيعي الذي يستدعي مزيجاً من الخلايا التائية عالية ومنخفضة التماسك، اختبر المؤلفون منتج CAR T «مختلط» جمع أعداداً متساوية من خلايا CAR T CD19 عالية ومنخفضة التماسك. في تَعايشات مخبرية مع خلايا السرطان والخلايا الوحيدة البشرية، قتلت هذه المنتجات المختلطة الأهداف بفعالية مماثلة لجرعة كاملة من المنتج عالي التماسك، لكنها أفرزت سيتوكينات التهابية أقل، مشبهةً بمظهر نصف جرعة من خلايا CAR T القوية. تحت التعرض المتكرر أو المزمن لخلايا السرطان، أصبحت خلايا CAR T منخفضة التماسك تدريجياً هي الفئة المهيمنة في الخليط، بينما أظهرت خلايا CAR T عالية التماسك وحدها مزيداً من علامات الإرهاق والضغط.
كيف يغيّر المزج السلوك طويل الأمد
في الفئران الحاملة للأورام، كان المنتج المجمّع الأفضل أداءً مجدداً بشكل عام. ظلت خلايا CAR T عالية التماسك ضرورية: لم تستطع CARs منخفضة التماسك وحدها مسح الأورام بالكامل، حتى بجرعات أعلى. لكن عندما نُقلت الخلايا عالية ومنخفضة التماسك معاً بجرعات كلية ثابتة، تقلصت الأورام أسرع وبشكل أكمل مقارنةً بنفس عدد الخلايا عالية التماسك وحدها. أظهر تسلسل RNA أحادي الخلية للخلايا CAR T المسترجعة أن الخلايا عالية التماسك في المجموعات المختلطة عبرت عن جينات أقل مرتبطة بالإرهاق والتمايز النهائي، ومزيداً من الجينات المرتبطة بوظيفة سامة مستمرة والإقامة النسيجية. هذا يشير إلى أن الخلايا الشريكة منخفضة التماسك تساعد على «تقاسم الحمل» في التعرف على المستضد، مما يحد من فرط تنشيط الأقوى بينها.
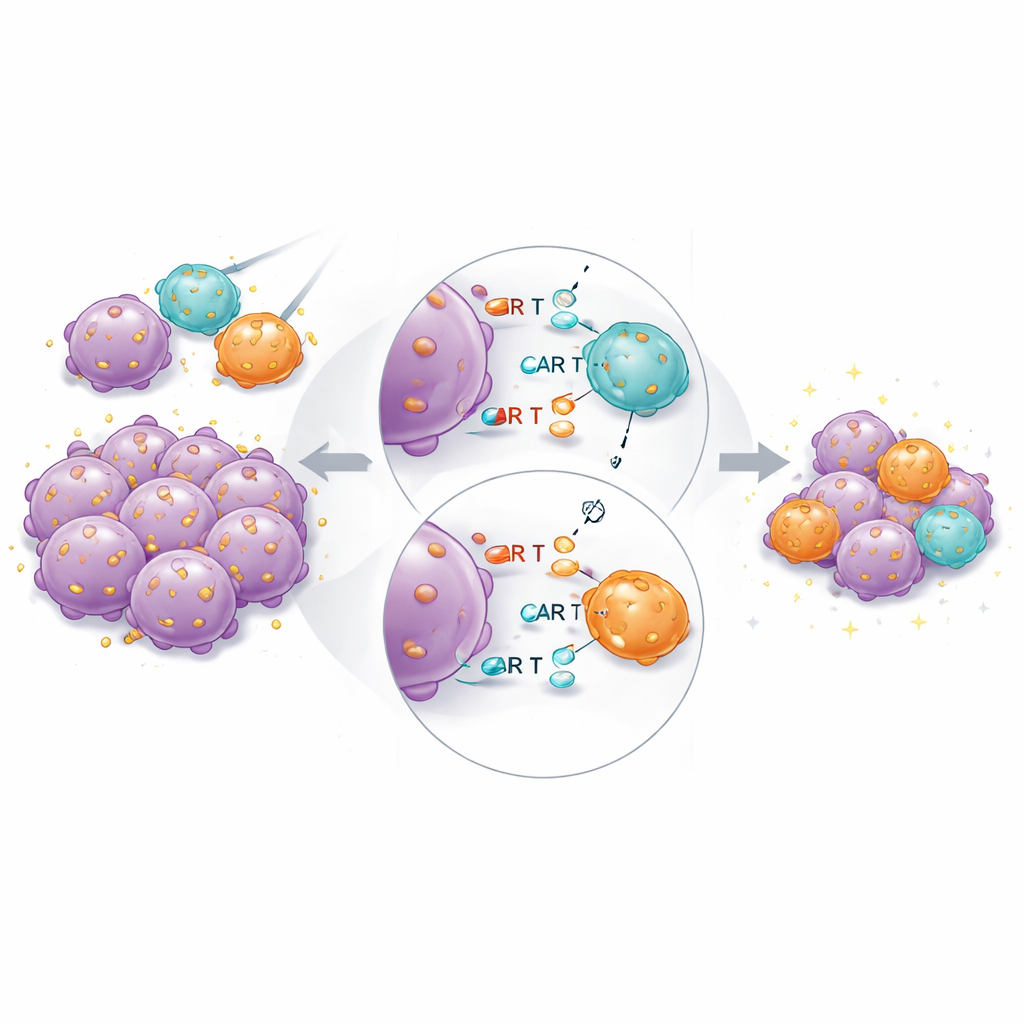
ما الذي يعنيه ذلك للمرضى
تُظهر الدراسة أن هناك حدّاً عملياً أدنى لمدى ضعف ارتباط CAR يمكن أن يظل فعالاً في التصاميم الحالية، وأن قوة الارتباط التي تعظم قتل الورم تميل أيضاً إلى تضخيم السمية والاحتراق. بدلاً من البحث عن تماسك مثالي واحد، يظهر مزج خلايا CAR T ذات قوى ارتباط مختلفة لنفس علامة السرطان كاستراتيجية واعدة. في هذا النهج توفر الخلايا عالية التماسك هجوماً سريعاً وقوياً، بينما تساعد الخلايا الأقل تماسكاً في تهدئة الالتهاب الجامح والحفاظ على السيطرة طويلة الأمد. إذا أكدت التجارب السريرية هذه النتائج ووسعت التطبيق إلى أهداف أخرى بخلاف CD19، فقد توسع منتجات CAR T المولفة بالتماسك نافذة العلاج — مما يجعل علاجات الخلايا أكثر أماناً وأكثر دواماً ومناسبة لمجموعة أوسع من السرطانات.
الاستشهاد: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
الكلمات المفتاحية: علاج الخلايا التائية CAR, CD19, تماسك المستقبل, متلازمة إطلاق السيتوكينات, مناعة السرطان