Clear Sky Science · ru
Баланс между эффективностью и безопасностью терапии CAR-Т-клеток за счёт сочетания аффинности рецепторов
Почему это важно для будущего лечения рака
Инженерные иммунные клетки — CAR-Т-клетки — могут вылечивать некоторые заболевания крови, но они также могут вызывать опасные побочные эффекты и иногда со временем перестают действовать. В этом исследовании поставлен на первый взгляд простой, но важный вопрос: вместо создания одной «супер-сильной» охотничьей клетки, что если целенаправленно смешать клетки с более высокой и более низкой аффинностью к одной и той же мишени на раковых клетках, чтобы лучше сбалансировать мощь и безопасность?
Как дизайнерские иммунные клетки борются с раком
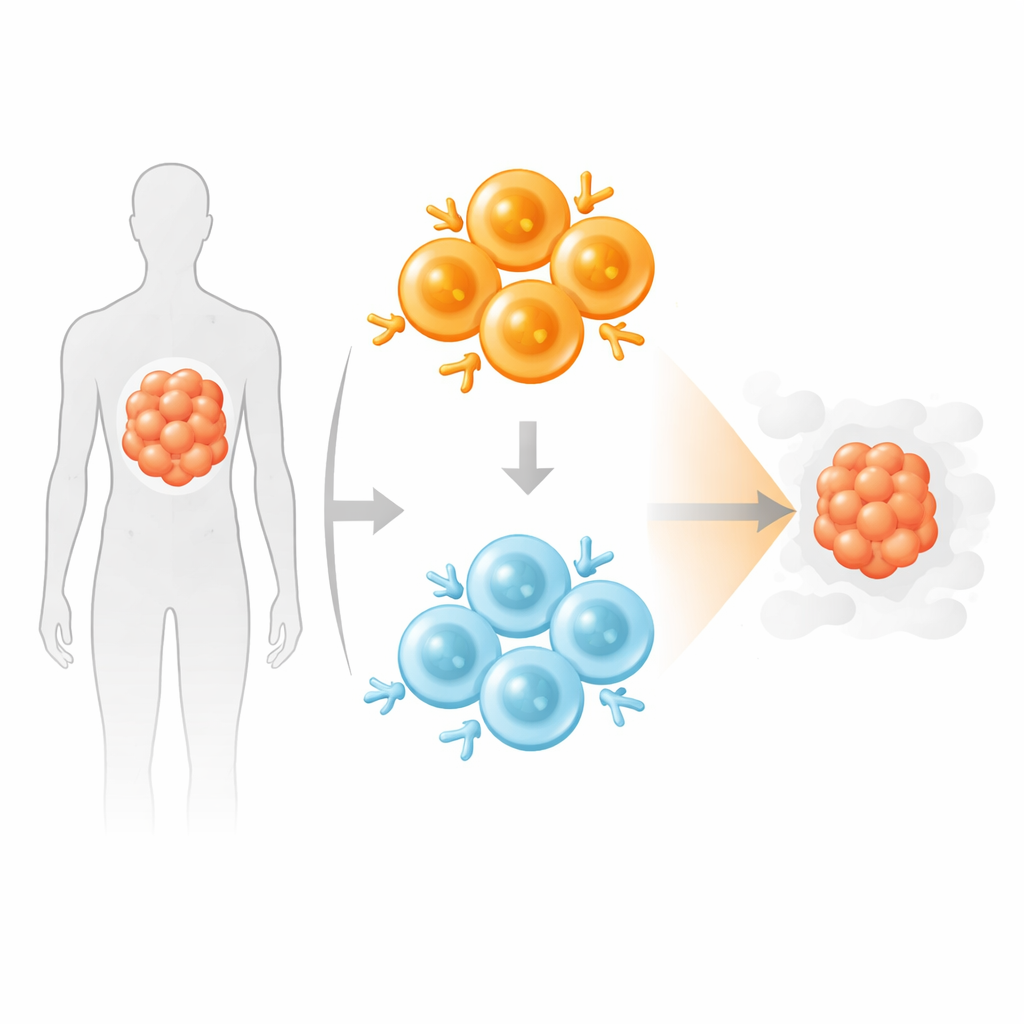
CAR-Т-клетки — это обычные Т-клетки пациента, перепрограммированные с помощью искусственного рецептора, чтобы захватывать маркеры на раковых клетках и уничтожать их. Большинство одобренных препаратов нацелены на молекулу CD19 на B-клетках и используют рецепторы, которые связываются с этим маркером намного сильнее, чем естественные Т-клеточные рецепторы. Такое усиленное связывание помогает распознавать и убивать раковые клетки, но также вызывает очень интенсивную активацию. Это может привести к тяжелым иммунным реакциям, таким как синдром высвобождения цитокинов (CRS), повреждению здоровых клеток, раннему выгоранию CAR-Т-клеток и рецидивам рака при потере или снижении экспрессии CD19 опухолевыми клетками.
Поиск «золотой середины» в силе связывания
Чтобы исследовать, как сила связывания влияет на поведение CAR-Т, учёные сравнили стандартный высокоаффинный CD19-CAR (JCAR017) с низкоаффинной версией (JCAR021), а затем создали большую панель вариантов, некоторые из которых по аффинности приближались к естественным ТCR. В лабораторных условиях большинство этих CAR-Т-клеток выглядели на удивление похоже: при условии стабильного экспонирования рецептора на поверхности клетки даже достаточно слабые связыватели могли активироваться, выделять ключевые иммунные медиаторы и уничтожать CD19-положительные клетки-мишени. Только самые слабые, TCR-подобные варианты начали демонстрировать снижение функции в жестких условиях, например при очень низкой экспрессии CD19 на мишенях.
Что происходит в живых организмах
При переходе к модельным мышам разница между сильными и слабыми связывателями стала гораздо более выраженной. Высокоаффинные CAR-Т-клетки быстро проливали популяцию, эффективно мигрировали в костный мозг, где находились CD19-положительные лимфомные клетки, и лучше контролировали опухоль. Низкоаффинные CAR задерживали рост опухоли, но редко соответствовали лидеру по эффективности, а ультра-слабые связыватели были по большей части неэффективными. При этом сильные связыватели вызывали более интенсивную активацию, более быструю дифференцировку Т-клеток и — что важно для гуманизированной модели мыши с восстановленной иммунной системой — более тяжёлое CRS-подобное заболевание, которое усугублялось при увеличении дозы CAR-Т-клеток.
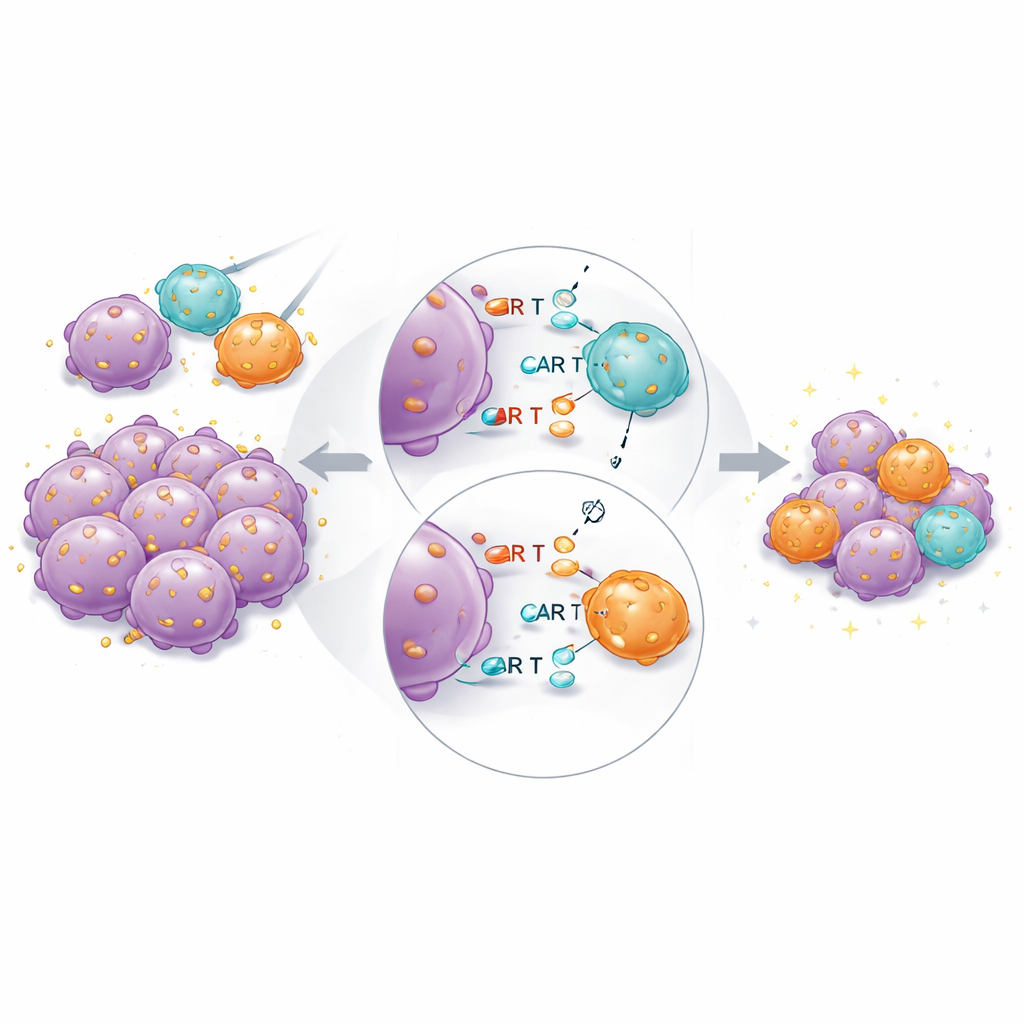
Смешивание сильных и «мягких» охотников
Вдохновившись тем, как наша естественная иммунная система рекрутирует смесь Т-клеток с высокой и низкой аффинностью, авторы проверили «смещённый» продукт CAR-Т, который сочетал равные доли высоко- и низкоаффинных CD19 CAR-Т-клеток. В лабораторных ко-культурах с раковыми клетками и человеческими моноцитами такие смешанные продукты уничтожали мишени так же эффективно, как и полный дозовый продукт с высокоаффинными клетками, но при этом выделяли меньше провоспалительных цитокинов, напоминая профиль половинной дозы сильных CAR-Т. При повторном или хроническом контакте с раковыми клетками низкоаффинные CAR-Т постепенно становились доминирующей популяцией в смеси, тогда как высокоаффинные CAR-Т в одиночку демонстрировали больше маркеров истощения и стресса.
Как смешение меняет долгосрочное поведение
В мышах с опухолями комбинированный продукт снова показал наилучшую общую эффективность. Высокоаффинные CAR-Т-клетки оставались необходимыми: низкоаффинные CAR одни не могли полностью очистить опухоль, даже при повышенных дозах. Но когда высоко- и низкоаффинные клетки переносили вместе при фиксированной общей дозе, опухоли сокращались быстрее и более полностью, чем при той же численности только высокоаффинных клеток. РНК-секвенирование отдельных CAR-Т-клеток, извлечённых после лечения, показало, что высокоаффинные клетки в смешанных группах экспрессировали меньше генов, связанных с истощением и терминальной дифференцировкой, и больше генов, ассоциированных с поддерживаемой цитотоксической функцией и тканевой резидентностью. Это указывает на то, что низкоаффинные партнёрные клетки помогают «разделять нагрузку» по распознаванию антигена, ограничивая переактивацию сильнейших связывателей.
Что это значит для пациентов
Исследование показывает, что существует практический нижний предел слабости связывания, при котором CAR в текущих конструкциях ещё эффективно работает, и что сила связывания, максимизирующая уничтожение опухоли, как правило, также усиливает токсичность и выгорание. Вместо поиска одной «идеальной» аффинности сочетание CAR-Т-клеток с разной силой связывания к одной и той же опухолевой мишени предстает как перспективная стратегия. В таком подходе высокоаффинные клетки обеспечивают быстрый мощный удар, а низкоаффинные клетки помогают смягчать неуправляемое воспаление и поддерживать долгосрочный контроль. Если это подтвердят клинические испытания и расширят на мишени, отличные от CD19, такие продукты с комбинированной аффинностью могут расширить терапевтическое окно — сделав клеточные терапии безопаснее, долговечнее и применимее к более широкому кругу злокачественных заболеваний.
Цитирование: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Ключевые слова: терапия CAR-Т-клетками, CD19, аффинность рецептора, синдром высвобождения цитокинов, раковая иммунотерапия