Clear Sky Science · tr
Affinite kombinasyonu ile kimerik antijen reseptörlü T hücre tedavisinin etkinliği ve güvenliğinin dengelenmesi
Geleceğin kanser bakımında bunun önemi nedir
Kimerik antijen reseptörlü (CAR) T hücreleri adı verilen mühendislik ürünü bağışıklık hücreleri bazı kan kanserlerini iyileştirebilir, ancak tehlikeli yan etkilere yol açabilir ve bazen uzun vadede başarısız olur. Bu çalışma, büyük sonuçları olabilecek yanıltıcı derecede basit bir soruyu soruyor: tek bir “aşırı güçlü” kanser avcısı hücre yerine, aynı kanser hedefine daha güçlü ve daha zayıf bağlanan hücreleri kasıtlı olarak karıştırmak, güç ve güvenliği daha iyi dengeleyebilir mi?
Tasarımcı bağışıklık hücreleri kanseri nasıl yok eder
CAR T hücreleri, hastadan alınan normal T hücrelerinin yapay bir reseptörle yeniden programlanmasıyla elde edilir; böylece kanser hücrelerindeki belirteçlere tutunup onları yok edebilirler. Onaylı çoğu tedavi, B hücrelerindeki CD19 adlı molekülü hedefler ve doğal T hücre reseptörlerinden çok daha sıkı tutunan reseptörler kullanır. Bu ekstra güçlü bağlanma kanser hücrelerini tanıyıp yok etmelerine yardımcı olur, ancak aynı zamanda çok yoğun aktivasyona neden olur. Bu durum, sitookin salınım sendromu (CRS) gibi şiddetli bağışıklık reaksiyonlarına, sağlıklı hücre hasarına, CAR T hücrelerinin erken tükenmesine ve tümör hücreleri CD19’u kaybettiğinde veya azalttığında nükslere yol açabilir.
Reseptör gücünde tatlı noktayı bulmak
Bağlanma gücünün CAR T davranışını nasıl şekillendirdiğini araştırmak için araştırmacılar, standart yüksek afiniteli CD19 CAR (JCAR017) ile daha düşük afiniteli bir versiyon (JCAR021) karşılaştırdı ve ardından bazıları doğal T hücre reseptörüne daha çok benzeyen geniş bir varyant paneli mühendislik etti. Laboratuvar ortamında, bu CAR T hücrelerinin çoğu şaşırtıcı derecede benzer görünüyordu: reseptör hücre yüzeyinde stabil şekilde sunulduğu sürece, oldukça zayıf bağlananlar bile CD19-pozitif hedef hücreleri aktive edebiliyor, önemli bağışıklık habercilerini salgılıyor ve öldürebiliyordu. Sadece en zayıf, TCR-benzeri varyantlar, hedef hücrelerde çok az CD19 bulunduğunda gibi zorlayıcı koşullarda azalmış fonksiyon göstermeye başladılar.
Canlı organizmalarda neler oluyor
Araştırma ekibi fare modellerine geçtiğinde güçlü ve zayıf bağlananlar arasındaki farklar çok daha belirgin hale geldi. Yüksek afiniteli CAR T hücreleri hızla çoğaldı, CD19-pozitif lenfoma hücrelerinin bulunduğu kemik iliğine verimli şekilde göç etti ve tümörleri en iyi şekilde kontrol etti. Daha düşük afiniteli CAR’lar tümör büyümesini geciktirdi ama nadiren en iyi performansa yetişti; ultra-zayıf bağlananlar ise büyük ölçüde etkisizdi. Aynı zamanda güçlü bağlananlar daha yoğun aktivasyon, T hücrelerinin daha hızlı farklılaşması ve—yeniden yapılanmış bir bağışıklık sistemi olan insanize fare modelinde—CAR T hücre dozu arttıkça kötüleşen daha şiddetli CRS-benzeri hastalığa yol açtı.
Güçlü ve nazik avcıları karıştırmak
Doğal bağışıklık sistemimizin yüksek ve düşük afiniteli T hücrelerini nasıl bir arada kullandığından ilham alarak, yazarlar eşit sayıda yüksek ve düşük afiniteli CD19 CAR T hücresini birleştiren “karışık” bir CAR T ürünü test ettiler. Kanser hücreleri ve insan monositleri ile yapılan laboratuvar ortak kültürlerinde, bu karışık ürünler tam doz yüksek afiniteli ürünü kadar etkili hedef öldürdü ancak daha az inflamatuar sitokin saldı; bu profil güçlü CAR T hücrelerinin yarım dozu ile benzerlik gösteriyordu. Kanser hücrelerine tekrarlayan veya kronik maruz kalma altında, düşük afiniteli CAR T hücreleri karışımda giderek baskın popülasyon haline gelirken, yalnız yüksek afiniteli CAR T hücreleri daha fazla tükenme ve stres belirteci gösterdi.
Karıştırmanın uzun vadeli davranışı nasıl değiştirdiği
Tümörlü farelerde, birleşik ürün yine genel olarak en iyi performansı gösterdi. Yüksek afiniteli CAR T hücreleri hâlâ esastı: yalnız düşük afiniteli CAR’lar, daha yüksek dozlarda bile tümörleri tamamen temizleyemedi. Ancak yüksek ve düşük afiniteli hücreler sabit toplam dozlarda birlikte verildiğinde, tümörler yalnızca aynı sayıda yüksek afiniteli hücreyle kıyaslandığında daha hızlı ve daha eksiksiz küçüldü. Geri kazanılan CAR T hücrelerinin tek hücre RNA dizilemesi, karışık gruplardaki yüksek afiniteli hücrelerin tükenme ve terminal farklılaşma ile ilişkili daha az gen; sürdürülebilir sitotoksik fonksiyon ve doku yerleşimi ile ilişkili daha fazla gen ifade ettiğini ortaya koydu. Bu, düşük afiniteli partner hücrelerin antijen tanımayı “paylaşarak” en güçlü bağlananların aşırı uyarımını sınırladığını düşündürüyor.
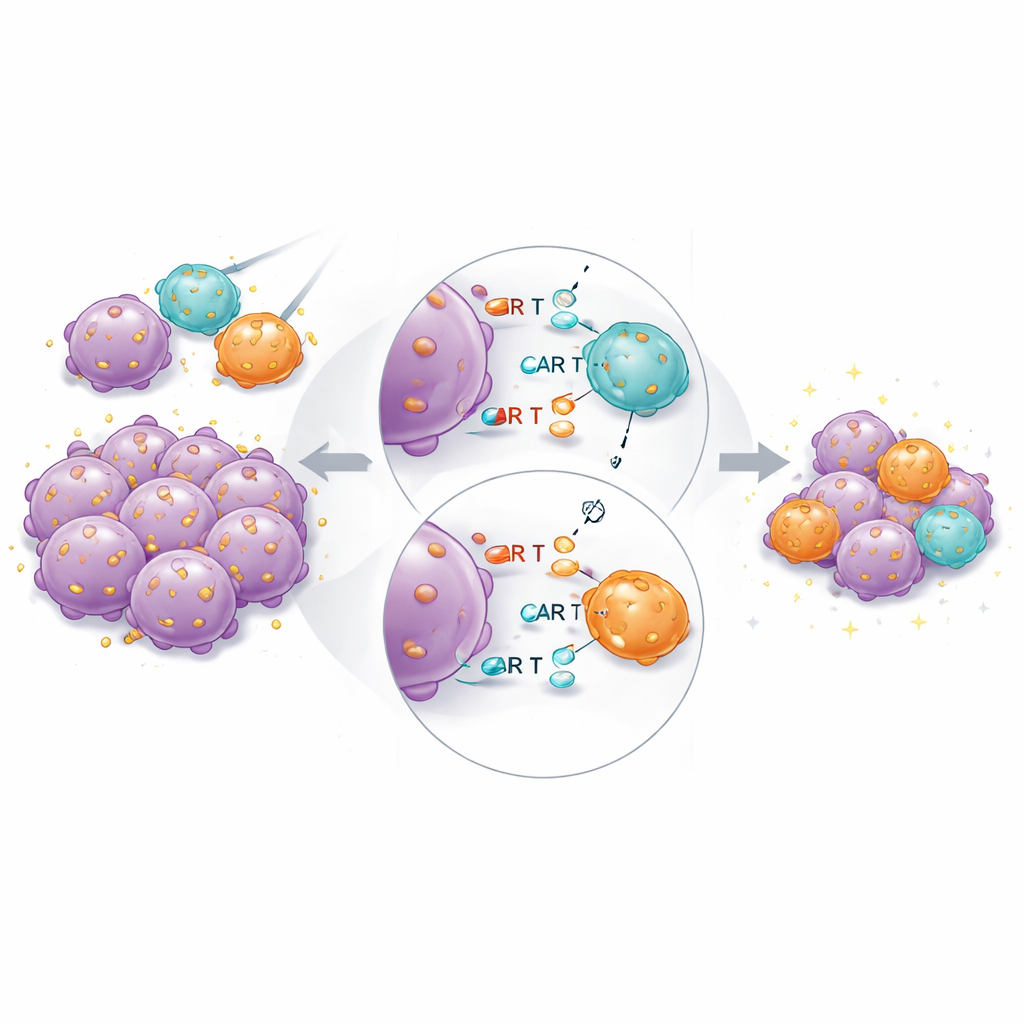
Bu hastalar için ne anlama geliyor
Çalışma, mevcut tasarımlarda bir CAR’ın ne kadar zayıf bağlanabileceğine dair pratik bir alt sınır olduğunu ve tümör öldürmeyi maksimize eden bağlanma gücünün aynı zamanda toksisiteyi ve tükenmeyi de büyütme eğiliminde olduğunu gösteriyor. Tek bir mükemmel afinite aramak yerine, aynı kanser belirtecine farklı bağlanma güçlerine sahip CAR T hücrelerini karıştırmak umut verici bir strateji olarak öne çıkıyor. Bu yaklaşımla yüksek afiniteli hücreler hızlı, güçlü bir saldırı sağlarken, düşük afiniteli hücreler kontrolden çıkan inflamasyonu azaltmaya ve uzun vadeli kontrolü sürdürmeye yardımcı oluyor. Klinik denemelerde doğrulanır ve CD19 dışındaki diğer hedeflere genişletilirse, bu tür afinite-karışımlı CAR T ürünleri tedavi penceresini genişletebilir—hücresel terapileri daha güvenli, daha dayanıklı ve daha geniş bir kanser yelpazesi için uygun hale getirebilir.
Atıf: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Anahtar kelimeler: CAR T hücre tedavisi, CD19, reseptör afinitesi, sitookin salınım sendromu, kanser immünoterapisi