Clear Sky Science · fr
Équilibrer efficacité et sécurité de la thérapie par cellules T à récepteur antigénique chimérique par combinaison d’affinités
Pourquoi cela compte pour les soins oncologiques futurs
Des cellules immunitaires génétiquement modifiées, appelées cellules CAR T, peuvent guérir certains cancers du sang, mais elles peuvent aussi provoquer des effets secondaires dangereux et échouer à long terme. Cette étude pose une question apparemment simple mais aux grandes implications : au lieu de concevoir une seule cellule « ultra‑puissante » chasseuse de cancer, et si on mélangeait délibérément des cellules ayant des affinités plus fortes et plus faibles pour la même cible tumorale afin de mieux équilibrer puissance et sécurité ?
Comment les cellules immunitaires conçues combattent le cancer
Les cellules CAR T sont des lymphocytes T du patient reprogrammés avec un récepteur artificiel leur permettant de se lier à des marqueurs présents sur les cellules cancéreuses et de les détruire. La plupart des thérapies approuvées ciblent une molécule appelée CD19 sur les cellules B et utilisent des récepteurs qui saisissent ce marqueur bien plus fortement que les récepteurs T naturels. Cette liaison très forte facilite la reconnaissance et l’élimination des cellules tumorales, mais provoque aussi une activation très intense. Cela peut entraîner des réactions immunitaires sévères telles que le syndrome de libération de cytokines (CRS), des dommages aux cellules saines, un épuisement précoce des CAR T et des rechutes tumorales lorsque les cellules cancéreuses perdent ou diminuent l’expression de CD19.
Trouver le point d’équilibre de la force de liaison
Pour explorer comment la force de liaison influence le comportement des CAR T, les chercheurs ont comparé un CAR CD19 d’affinité élevée standard (JCAR017) à une version d’affinité plus faible (JCAR021), puis ont conçu un vaste panel d’autres variants, certains ayant une affinité proche de celle d’un récepteur T naturel. En culture, la plupart de ces cellules CAR T apparaissaient étonnamment semblables : tant que le récepteur était correctement affiché à la surface cellulaire, même des liaisons assez faibles pouvaient encore activer la cellule, sécréter des médiateurs immunitaires clés et tuer des cellules cibles CD19‑positives. Seuls les variants très faiblement liants, proches des TCR, montraient une fonction réduite dans des conditions exigeantes, par exemple lorsque les cellules cibles exprimaient très peu de CD19.
Ce qui se passe dans un organisme vivant
Lorsque l’équipe est passée à des modèles murins, les différences entre liants forts et faibles se sont nettement amplifiées. Les CAR T à haute affinité se sont étendus rapidement, ont migré efficacement vers la moelle osseuse où résidaient des lymphomes CD19‑positifs, et ont contrôlé les tumeurs de façon optimale. Les CAR d’affinité plus faible retardaient la croissance tumorale mais égalèrent rarement le meilleur performeur, et les liants ultra‑faibles étaient largement inefficaces. Parallèlement, les liants forts entraînaient une activation plus intense, une différenciation plus rapide des T, et — important dans un modèle murin humanisé avec un système immunitaire reconstitué — des manifestations de type CRS plus graves qui s’aggravaient avec l’augmentation de la dose de CAR T.
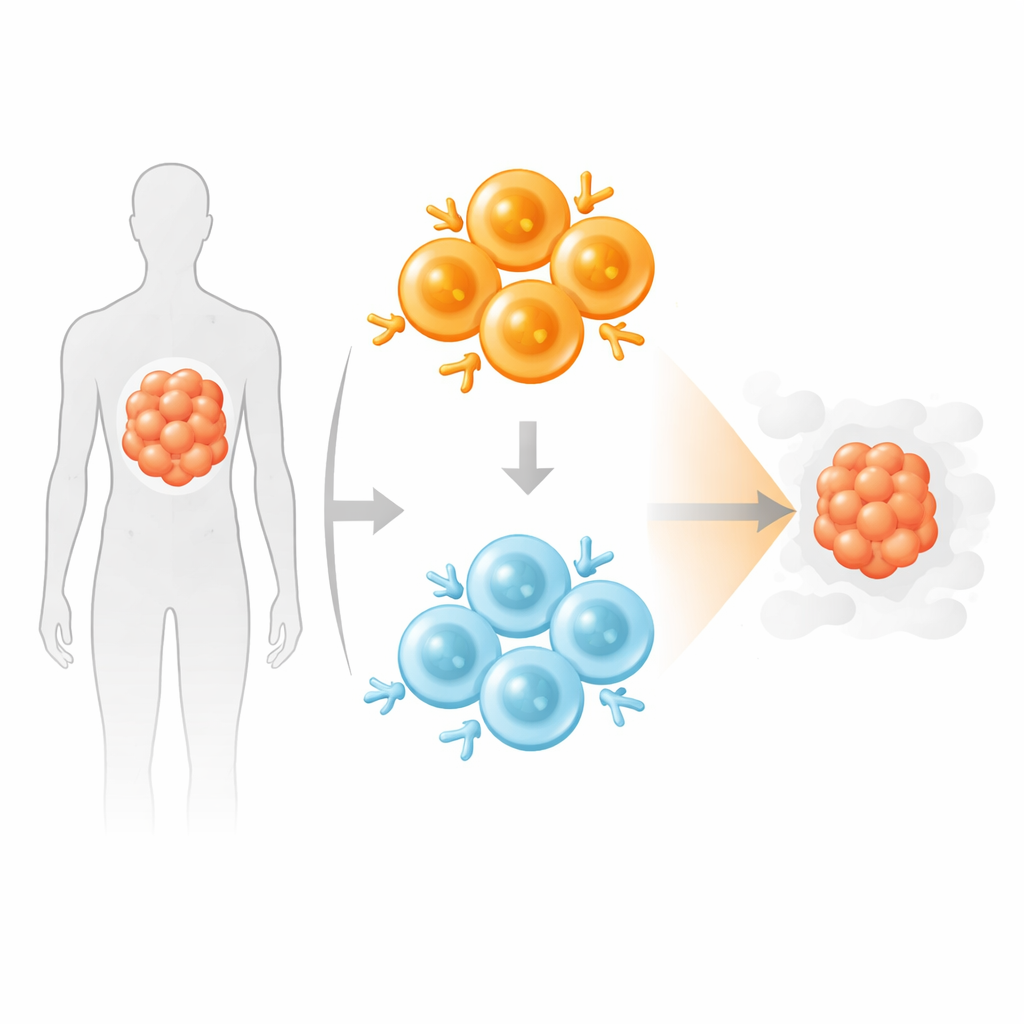
Mélanger chasseurs puissants et plus doux
S’inspirant de la manière dont notre système immunitaire naturel recrute un mélange de lymphocytes T à haute et basse affinité, les auteurs ont testé un produit CAR T « mélangé » combinant des nombres égaux de CAR T CD19 à haute et basse affinité. En co‑cultures avec des cellules cancéreuses et des monocytes humains, ces produits mixtes tuaient les cibles aussi efficacement qu’un produit haute affinité à dose pleine, mais libéraient moins de cytokines inflammatoires, ressemblant au profil d’une demi‑dose de CAR T puissants. Lors d’expositions répétées ou chroniques aux cellules tumorales, les CAR T à basse affinité devenaient progressivement la population dominante dans le mélange, alors que les CAR T à haute affinité seuls présentaient davantage de marqueurs d’épuisement et de stress.
Comment le mélange modifie le comportement à long terme
Chez les souris porteuses de tumeurs, le produit combiné a de nouveau donné les meilleurs résultats globaux. Les CAR T à haute affinité restaient essentiels : les CAR d’affinité plus faible seuls ne pouvaient pas éradiquer complètement les tumeurs, même à des doses plus élevées. Mais lorsque des cellules à haute et basse affinité étaient transférées ensemble à doses totales fixes, les tumeurs régresseaient plus rapidement et plus complètement que pour le même nombre de cellules haute affinité seules. Le séquençage ARN unicellulaire des CAR T récupérés a révélé que, dans les groupes mixtes, les cellules à haute affinité exprimaient moins de gènes liés à l’épuisement et à la différenciation terminale, et davantage de gènes associés à une fonction cytotoxique soutenue et à la résidence tissulaire. Cela suggère que les cellules partenaires à faible affinité contribuent à « partager la charge » de reconnaissance antigénique, limitant la sur‑stimulation des liants les plus puissants.
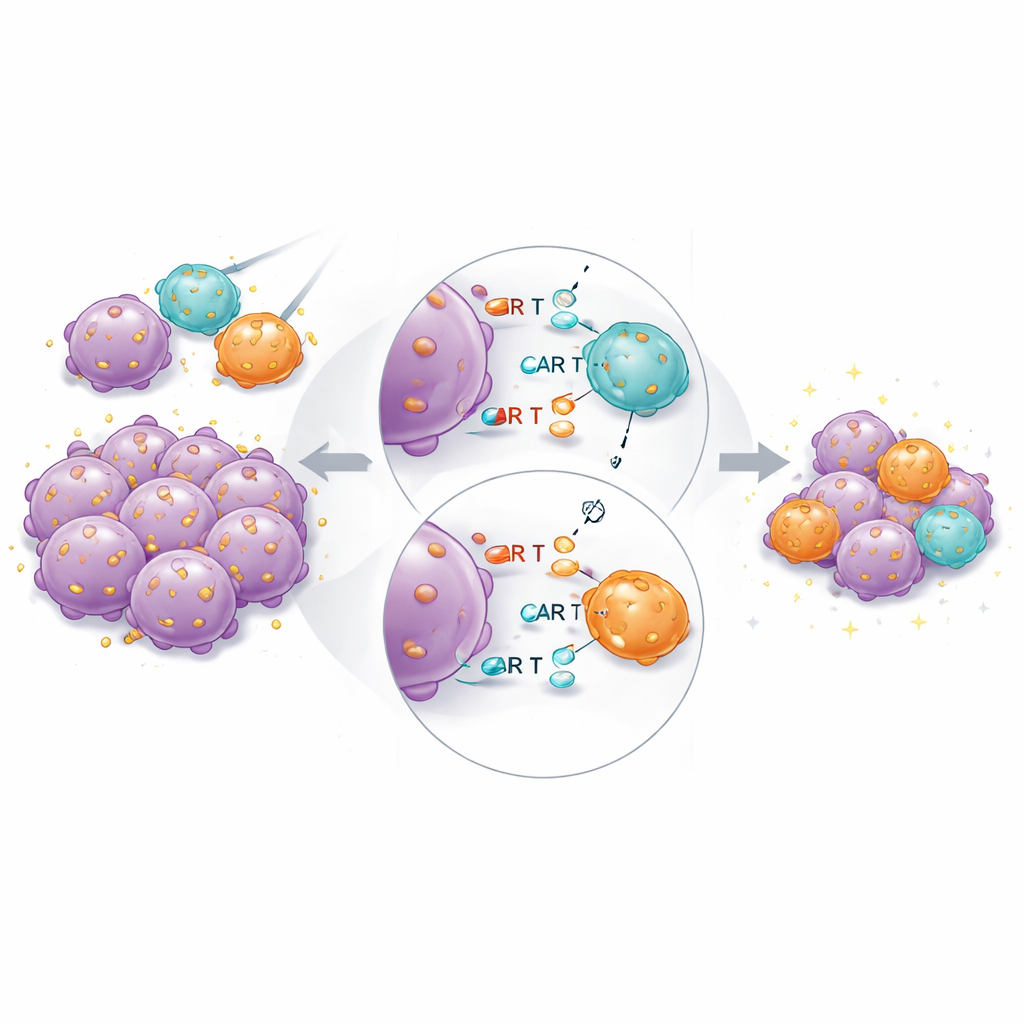
Ce que cela signifie pour les patients
L’étude montre qu’il existe une limite pratique en dessous de laquelle l’affinité d’un CAR devient trop faible pour être efficace dans les conceptions actuelles, et que l’affinité qui maximise la destruction tumorale tend aussi à accroître la toxicité et l’épuisement. Plutôt que de rechercher une affinité unique parfaite, mélanger des cellules CAR T ayant différentes forces de liaison pour le même marqueur tumoral apparaît comme une stratégie prometteuse. Dans ce schéma, les cellules à haute affinité fournissent une attaque rapide et puissante, tandis que les cellules à plus faible affinité aident à tempérer l’inflammation incontrôlée et à maintenir le contrôle à long terme. Si ces résultats sont confirmés en essai clinique et étendus à d’autres cibles au‑delà de CD19, des produits CAR T combinant plusieurs affinités pourraient élargir la fenêtre thérapeutique — rendant les thérapies cellulaires plus sûres, plus durables et adaptées à un plus grand nombre de cancers.
Citation: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Mots-clés: Thérapie par cellules CAR T, CD19, affinité du récepteur, syndrome de libération de cytokines, immunothérapie du cancer