Clear Sky Science · sv
Balansera effektivitet och säkerhet för kirala antigensreceptor (CAR) T-cellsbehandling genom kombination av affinitet
Varför detta spelar roll för framtidens cancerbehandling
Härdade immunceller kallade CAR T-celler kan bota vissa blodcancerformer, men de kan också orsaka farliga biverkningar och ibland misslyckas på längre sikt. Denna studie ställer en till synes enkel fråga med stora konsekvenser: i stället för att bygga en enda ”superstark” cancerjagande cell, vad händer om vi medvetet blandar celler med starkare och svagare bindning till samma cancermål för att bättre balansera kraft och säkerhet?
Hur skräddarsydda immunceller bekämpar cancer
CAR T-celler är vanliga T-celler från en patient som omprogrammeras med en artificiell receptor så att de kan fästa vid markörer på cancerceller och förstöra dem. De flesta godkända behandlingar riktar sig mot ett molekylärt mål kallat CD19 på B-celler och använder receptorer som greppar detta mål mycket starkare än naturliga T-cellreceptorer gör. Det extra starka bindandet hjälper dem att känna igen och döda cancerceller, men det driver också en mycket intensiv aktivering. Detta kan leda till svåra immunreaktioner såsom cytokinstorm (CRS), skada på friska celler, tidig utmattning av CAR T-cellerna och återfall när tumörceller förlorar eller minskar uttrycket av CD19.
Hitta den optimala receptorstyrkan
För att undersöka hur bindningsstyrka formar CAR T-beteende jämförde forskarna en standard högaffinitets CD19 CAR (JCAR017) med en lägreffinitetsvariant (JCAR021) och konstruerade sedan ett stort panel av ytterligare varianter, vissa med bindning som mer liknar en naturlig T-cellreceptor. I laboratorieodlingar såg de flesta av dessa CAR T-celler förvånansvärt lika ut: så länge receptorn visades stabilt på cellens yta kunde även ganska svaga bindare fortfarande aktiveras, utsöndra viktiga immunsignalmolekyler och döda CD19-positiva målceller. Endast de allra svagaste, TCR-liknande varianterna började visa nedsatt funktion under krävande förhållanden, till exempel när målcellerna bar mycket lite CD19.
Vad som händer i levande organismer
När teamet gick vidare till musmodeller blev skillnaderna mellan starka och svaga bindare mycket tydligare. Högaffinitets CAR T-celler expanderade snabbt, tog sig effektivt in i benmärgen där CD19-positiva lymfomceller fanns och kontrollerade tumörerna bäst. Lågaffinitets-CARs fördröjde tumörtillväxt men nådde sällan upp till toppresultatet, och ultrasvaga bindare var till stor del ineffektiva. Samtidigt drev de starka bindarna mer intensiv aktivering, snabbare differentiering av T-celler och — vilket var viktigt i en humaniserad musmodell med ett rekonstituerat immunsystem — mer allvarlig CRS-liknande sjukdom som förvärrades med ökad dos av CAR T-celler.
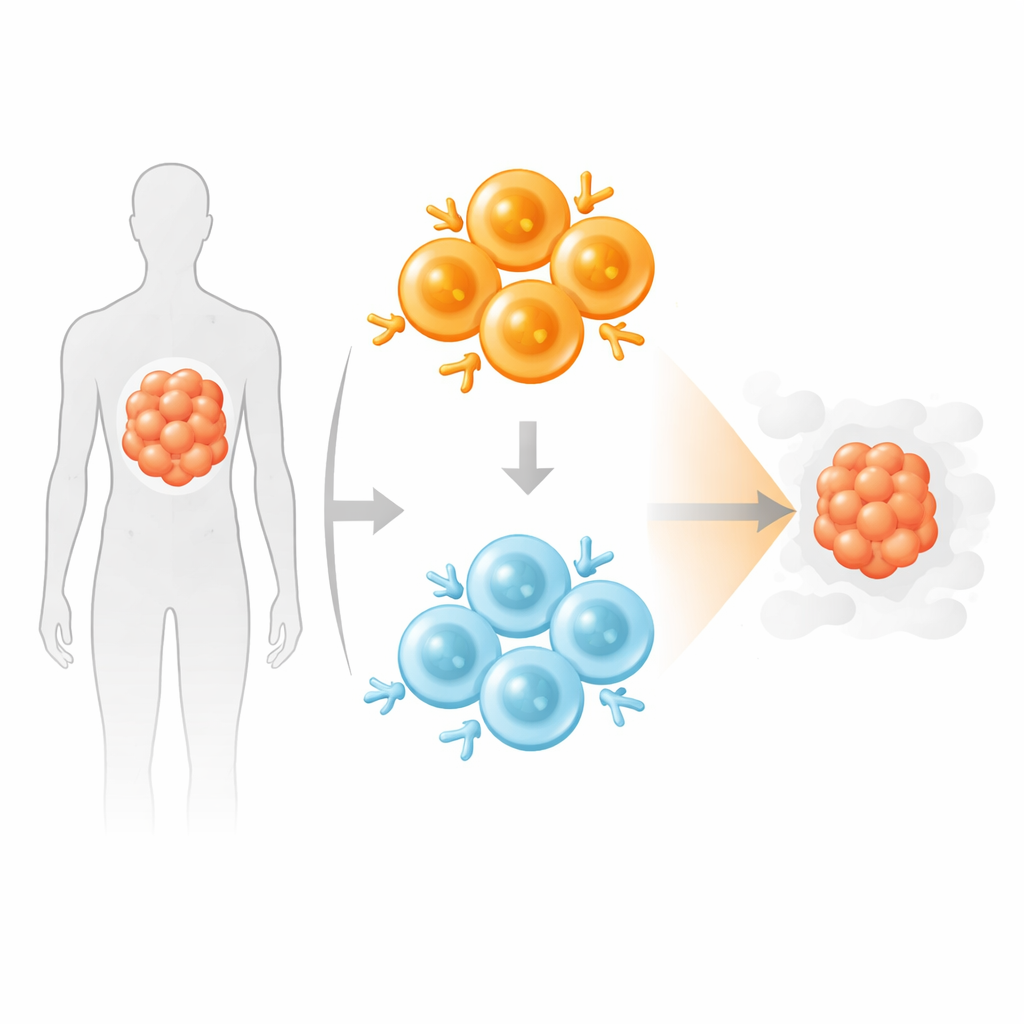
Blanda starka och försiktiga jägare
Inspirerade av hur vårt naturliga immunsystem rekryterar en blandning av hög- och lågaffinitets T-celler testade författarna en ”blandad” CAR T-produkt som kombinerade lika många hög- och lågaffinitets CD19 CAR T-celler. I laboratorieko-kulturer med cancerceller och mänskliga monocyter dödade dessa blandade produkter målen lika effektivt som en full dos högaffinitetsprodukt, men frisatte färre inflammatoriska cytokiner, vilket liknade profilen hos en halvdos starka CAR T-celler. Vid upprepad eller kronisk exponering för cancerceller blev lågaffinitets-CAR T-celler gradvis den dominerande populationen i blandningen, medan högaffinitets-CAR T-celler ensamma visade fler markörer för utmattning och stress.
Hur blandning förändrar långsiktigt beteende
I tumörbärande möss presterade den kombinerade produkten återigen bäst överlag. Högaffinitets-CAR T-celler var fortfarande nödvändiga: lågaffinitets-CARs ensamma kunde inte helt rensa tumörer, även vid högre doser. Men när hög- och lågaffinitetsceller överfördes tillsammans vid fasta totaldoser krympte tumörerna snabbare och mer fullständigt än med samma antal högaffinitetsceller ensam. Enkelcells-RNA-sekvensering av återhämtade CAR T-celler visade att högaffinitetsceller i de blandade grupperna uttryckte färre gener kopplade till utmattning och terminal differentiering, och fler gener associerade med uthållig cytotoxisk funktion och vävnadsresidentitet. Detta tyder på att lågaffinitetspartnerceller hjälper till att ”dela bördan” av antigenigenkänning och därigenom begränsa överstimulering av de starkaste bindarna.
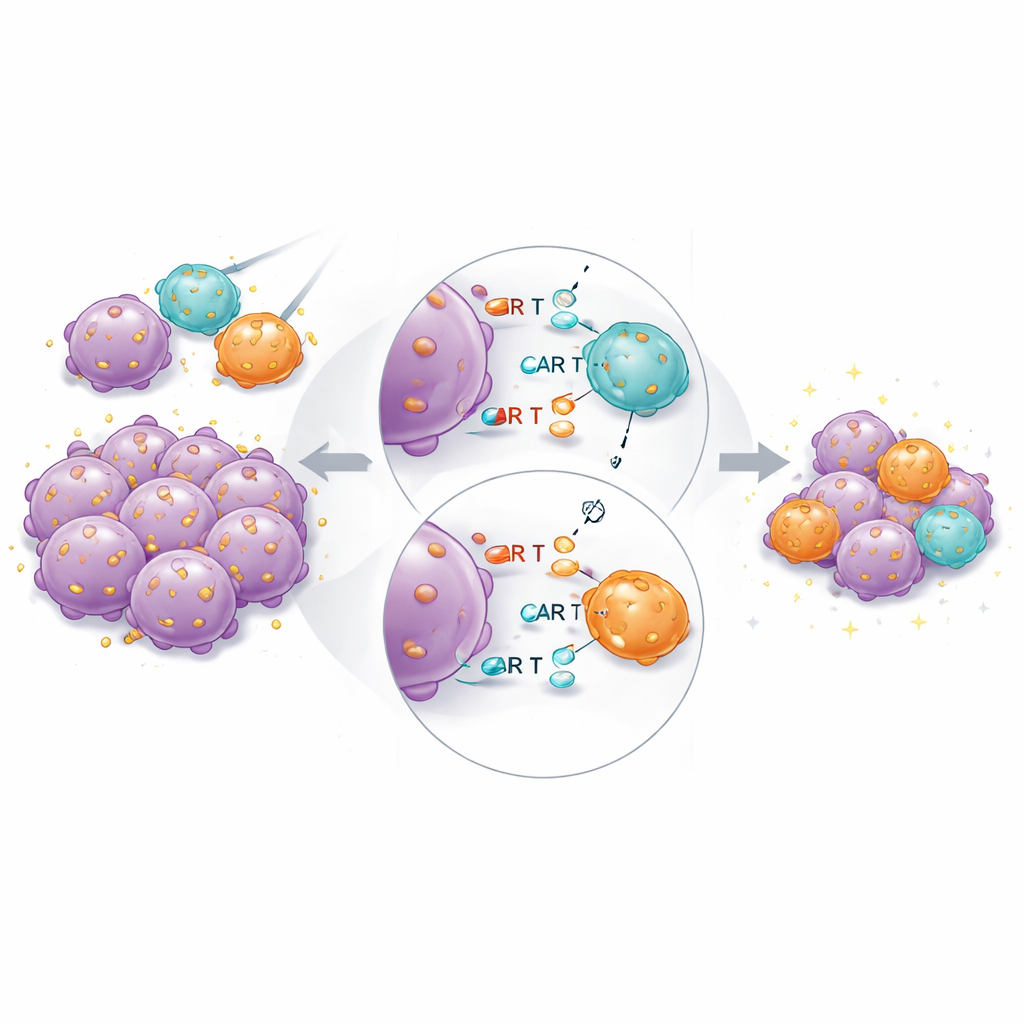
Vad detta betyder för patienter
Studien visar att det finns en praktisk nedre gräns för hur svagt en CAR kan binda och ändå fungera väl i nuvarande konstruktioner, och att bindningsstyrka som maximerar tumördödning också tenderar att förstora toxicitet och utmattning. I stället för att söka efter en enda perfekt affinitet framträder blandning av CAR T-celler med olika bindningsstyrkor mot samma cancermarkör som en lovande strategi. I denna metod ger högaffinitetsceller ett snabbt, kraftfullt angrepp, medan lågaffinitetsceller hjälper till att dämpa okontrollerad inflammation och upprätthålla långsiktig kontroll. Om det bekräftas i kliniska prövningar och utvidgas till andra mål än CD19 kan sådana affinitetskombinerade CAR T-produkter vidga behandlingsfönstret — göra cellterapier säkrare, mer hållbara och lämpade för ett bredare spektrum av cancerformer.
Citering: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Nyckelord: CAR T-cellsbehandling, CD19, receptoraffinitet, cytokinstorm, cancerimmunterapi