Clear Sky Science · es
Equilibrar la eficacia y la seguridad de la terapia CAR-T mediante la combinación de afinidades
Por qué esto importa para la atención futura del cáncer
Las células inmunitarias diseñadas llamadas células CAR-T pueden curar algunos cánceres hematológicos, pero también pueden provocar efectos secundarios peligrosos y, en ocasiones, fracasar a largo plazo. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones: en lugar de construir una sola célula “súper potente” cazadora de cáncer, ¿qué ocurriría si deliberadamente mezcláramos células con mayor y menor capacidad de unión al mismo objetivo tumoral para equilibrar mejor potencia y seguridad?
Cómo las células inmunitarias diseñadas combaten el cáncer
Las células CAR-T son linfocitos T del paciente reprogramados con un receptor artificial para que puedan unirse a marcadores en las células tumorales y destruirlas. La mayoría de las terapias aprobadas se dirigen a una molécula llamada CD19 en células B y usan receptores que se aferran a este marcador mucho más fuertemente que los receptores T naturales. Esa unión extra-fuerte les ayuda a reconocer y matar células cancerosas, pero también provoca una activación muy intensa. Esto puede conducir a reacciones inmunitarias graves como el síndrome de liberación de citocinas (CRS), daño a células sanas, agotamiento prematuro de las células CAR-T y recaídas cuando las células tumorales pierden o reducen CD19.
Encontrar el punto óptimo en la fuerza del receptor
Para explorar cómo la fuerza de unión modela el comportamiento de las CAR-T, los investigadores compararon un CAR CD19 de alta afinidad estándar (JCAR017) con una versión de menor afinidad (JCAR021) y luego diseñaron un amplio panel de variantes adicionales, algunas con unión más parecida a la de un receptor T natural. En cultivos celulares, la mayoría de estas CAR-T se mostraron sorprendentemente similares: siempre que el receptor estuviera estabilamente presente en la superficie celular, incluso los ligandos bastante débiles podían activarse, secretar mensajeros inmunitarios clave y matar células diana positivas para CD19. Solo las variantes más débiles, similares a TCR, empezaron a mostrar una función reducida en condiciones exigentes, como cuando las células objetivo presentaban muy poco CD19.
Qué ocurre en organismos vivos
Cuando el equipo pasó a modelos murinos, las diferencias entre ligandos fuertes y débiles se hicieron mucho más pronunciadas. Las CAR-T de alta afinidad se expandieron rápidamente, migraron eficazmente a la médula ósea donde residían las células linfomatosas CD19-positivas y controlaron mejor los tumores. Las CAR de menor afinidad retrasaron el crecimiento tumoral pero rara vez igualaron al mejor rendimiento, y las de afinidad ultra-baja fueron en gran medida ineficaces. Al mismo tiempo, los ligandos fuertes provocaron una activación más intensa, una diferenciación más rápida de las células T y—de forma importante en un modelo murino humanizado con sistema inmune reconstituido—enfermedad tipo CRS más grave que empeoró al aumentar la dosis de CAR-T.
Mezclar cazadores fuertes y suaves
Inspirados por cómo nuestro sistema inmune natural recluta una mezcla de células T de alta y baja afinidad, los autores probaron un producto CAR-T “mezclado” que combinaba igual número de células CAR-T CD19 de alta y baja afinidad. En cocultivos de laboratorio con células tumorales y monocitos humanos, estos productos mixtos mataron los objetivos tan eficazmente como un producto de alta afinidad a dosis completa, pero liberaron menos citocinas inflamatorias, asemejándose al perfil de media dosis de CAR-T fuertes. Bajo exposición repetida o crónica a células cancerosas, las CAR de baja afinidad se convirtieron gradualmente en la población dominante de la mezcla, mientras que las CAR de alta afinidad en solitario mostraron más marcadores de agotamiento y estrés.
Cómo la mezcla cambia el comportamiento a largo plazo
En ratones con tumores, el producto combinado volvió a rendir mejor en conjunto. Las CAR de alta afinidad siguieron siendo esenciales: las CAR de baja afinidad por sí solas no pudieron eliminar completamente los tumores, ni siquiera a dosis más altas. Pero cuando las células de alta y baja afinidad se transfirieron juntas a dosis totales fijas, los tumores se redujeron más rápido y de forma más completa que con el mismo número de células de alta afinidad en solitario. El análisis de ARN de célula única de las CAR-T recuperadas reveló que las células de alta afinidad en los grupos mixtos expresaban menos genes vinculados al agotamiento y a la diferenciación terminal, y más genes asociados con función citotóxica sostenida y residencia tisular. Esto sugiere que las células socias de baja afinidad ayudan a “compartir la carga” del reconocimiento antigénico, limitando la sobreestimulación de los ligandos más fuertes.
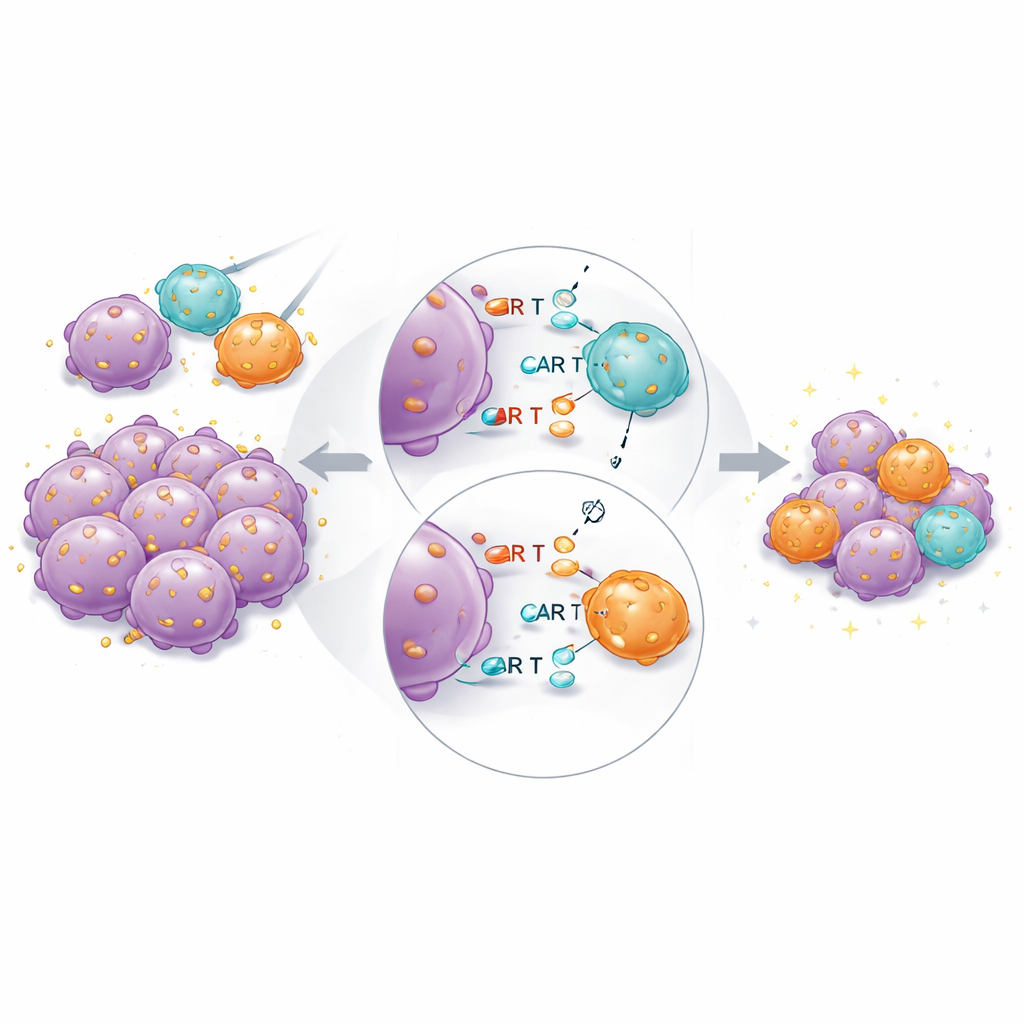
Qué significa esto para los pacientes
El estudio muestra que existe un límite práctico a lo débil que puede ser la unión de un CAR y seguir funcionando bien con los diseños actuales, y que la afinidad que maximiza la eliminación tumoral también tiende a magnificar la toxicidad y el agotamiento. En lugar de buscar una única afinidad perfecta, la mezcla de células CAR-T con distintas fuerzas de unión al mismo marcador tumoral surge como una estrategia prometedora. En este enfoque, las células de alta afinidad proporcionan un ataque rápido y potente, mientras que las de menor afinidad ayudan a amortiguar la inflamación descontrolada y sostener el control a largo plazo. Si se confirma en ensayos clínicos y se amplía a otros objetivos más allá de CD19, dichos productos CAR-T combinados por afinidad podrían ampliar la ventana terapéutica—haciendo las terapias celulares más seguras, duraderas y aptas para una gama más amplia de cánceres.
Cita: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Palabras clave: Terapia CAR-T, CD19, afinidad del receptor, síndrome de liberación de citocinas, inmunoterapia contra el cáncer