Clear Sky Science · it
Bilanciare efficacia e sicurezza della terapia con cellule T CAR attraverso la combinazione di affinità
Perché questo è importante per la cura del cancro futura
Le cellule immunitarie ingegnerizzate, chiamate cellule CAR T, possono curare alcuni tumori del sangue, ma possono anche provocare effetti collaterali pericolosi e talvolta fallire nel lungo periodo. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: invece di costruire una singola cellula “iperdeterminata” per cacciare il cancro, che cosa succederebbe se mescolassimo deliberatamente cellule con affinità più alta e più bassa per lo stesso bersaglio tumorale, per bilanciare meglio potenza e sicurezza?
Come le cellule immunitarie progettate combattono il cancro
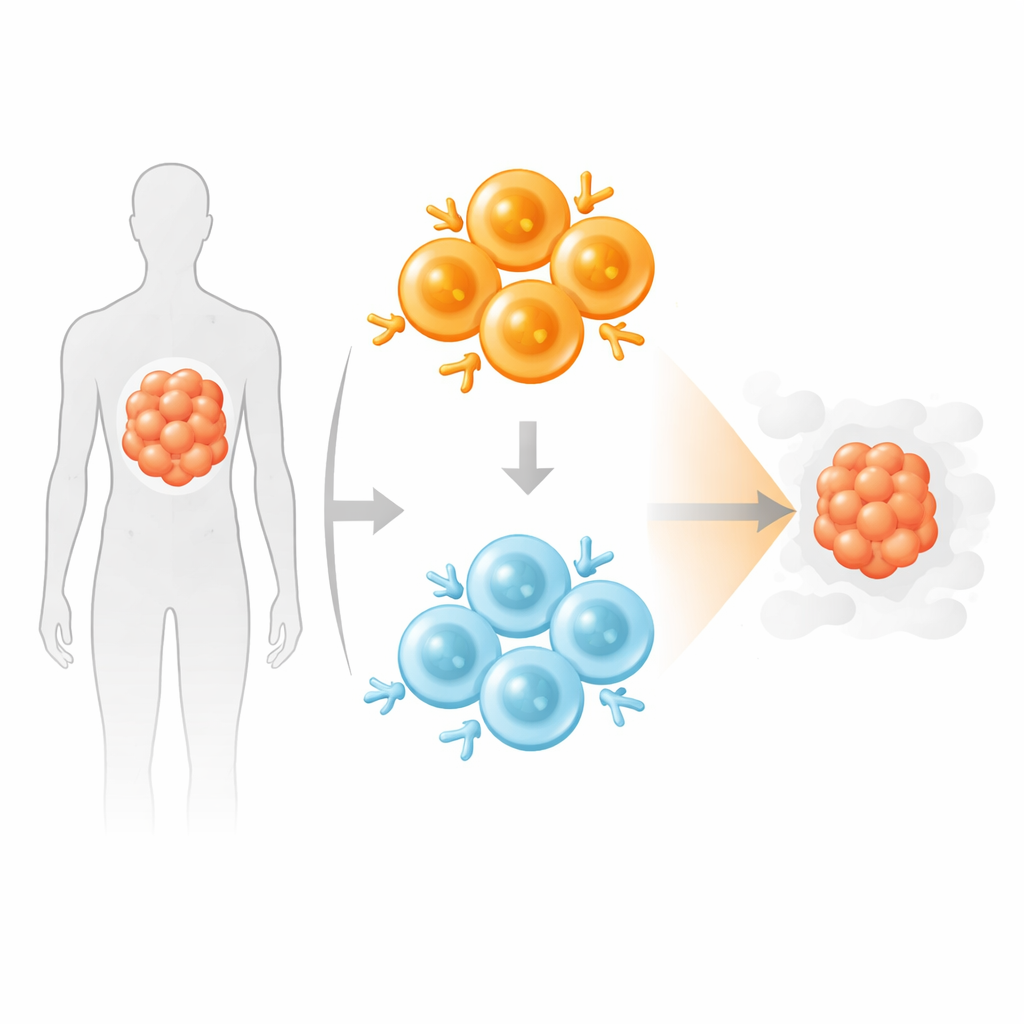
Le cellule CAR T sono normali cellule T prelevate dal paziente e riprogrammate con un recettore artificiale in modo che possano agganciarsi a marcatori sulle cellule tumorali e distruggerle. La maggior parte delle terapie approvate prende di mira una molecola chiamata CD19 sulle cellule B e usa recettori che legano questo marcatore molto più saldamente rispetto ai recettori T naturali. Questo legame extra-forte li aiuta a riconoscere e uccidere le cellule tumorali, ma provoca anche un’attivazione molto intensa. Ciò può portare a reazioni immunitarie severe come la sindrome da rilascio di citochine (CRS), danni alle cellule sane, precoce esaurimento delle cellule CAR T e ricadute tumorali quando le cellule tumorali perdono o riducono CD19.
Trovare il punto ottimale nell’intensità del recettore
Per capire come la forza di legame influenzi il comportamento delle CAR T, i ricercatori hanno confrontato un CAR anti-CD19 a elevata affinità standard (JCAR017) con una versione a bassa affinità (JCAR021) e hanno quindi ingegnerizzato un ampio pannello di varianti aggiuntive, alcune con legame più simile a quello di un recettore T naturale. In colture in provetta, la maggior parte di queste cellule CAR T appariva sorprendentemente simile: finché il recettore era stabilmente esposto sulla superficie cellulare, anche leganti abbastanza deboli potevano comunque attivarsi, secernere i principali messaggeri immunitari e uccidere cellule bersaglio CD19-positive. Solo le varianti molto deboli, simili ai TCR, cominciavano a mostrare una funzione ridotta in condizioni impegnative, come quando le cellule bersaglio esprimevano pochissimo CD19.
Cosa succede negli organismi viventi
Quando il gruppo ha testato le cellule in modelli murini, le differenze tra leganti forti e deboli sono diventate molto più marcate. Le CAR T ad alta affinità si espandevano rapidamente, migravano efficacemente nel midollo osseo dove risiedevano le cellule di linfoma CD19-positive e controllavano meglio i tumori. Le CAR a bassa affinità ritardavano la crescita tumorale ma raramente uguagliavano le prestazioni del miglior esecutore, e gli ultra-leganti deboli erano in gran parte inefficaci. Allo stesso tempo, i leganti forti provocavano un’attivazione più intensa, una differenziazione più rapida delle cellule T e—cosa importante in un modello murino umanizzato con sistema immunitario ricostituito—una malattia simile alla CRS più grave che peggiorava con l’aumentare della dose di CAR T.
Mescolare cacciatori forti e gentili
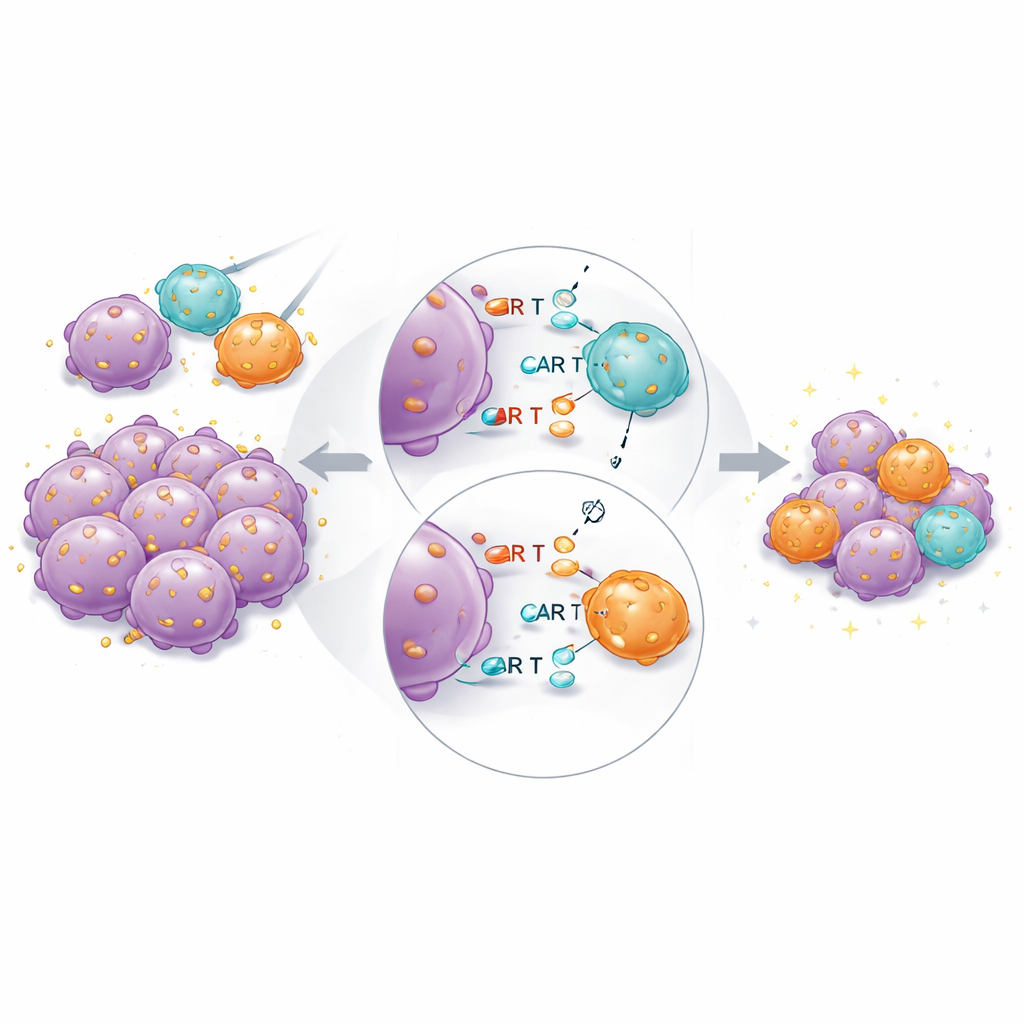
Ispirati da come il nostro sistema immunitario naturale recluta un mix di cellule T ad alta e bassa affinità, gli autori hanno testato un prodotto CAR T “misto” che combinava in egual numero cellule CAR T anti-CD19 ad alta e a bassa affinità. In coculture di laboratorio con cellule tumorali e monociti umani, questi prodotti misti uccidevano i bersagli con la stessa efficacia di un prodotto ad alta affinità a dose piena, ma rilasciavano meno citochine infiammatorie, assomigliando al profilo di mezza dose di CAR T forti. Sotto esposizione ripetuta o cronica alle cellule tumorali, le CAR T a bassa affinità divenivano gradualmente la popolazione dominante nella miscela, mentre le CAR ad alta affinità usate da sole mostravano più marcatori di esaurimento e stress.
Come la miscela cambia il comportamento a lungo termine
Nei topi portatori di tumore, il prodotto combinato ha nuovamente dato le migliori prestazioni complessive. Le CAR T ad alta affinità erano ancora essenziali: le CAR a bassa affinità da sole non riuscivano a eliminare completamente i tumori, nemmeno a dosi più elevate. Ma quando le cellule ad alta e bassa affinità venivano trasferite insieme a dosi totali fisse, i tumori si riducevano più rapidamente e in modo più completo rispetto allo stesso numero di cellule ad alta affinità da sole. Il sequenziamento dell’RNA a singola cellula delle CAR T recuperate ha rivelato che le cellule ad alta affinità nei gruppi misti esprimevano meno geni collegati all’esaurimento e alla differenziazione terminale, e più geni associati a funzione citotossica sostenuta e residenza tissutale. Ciò suggerisce che le cellule partner a bassa affinità aiutano a “condividere il carico” del riconoscimento dell’antigene, limitando la sovra-stimolazione dei leganti più forti.
Cosa significa per i pazienti
Lo studio mostra che esiste un limite pratico a quanto debole un CAR può legare e continuare a funzionare bene nei disegni attuali, e che l’affinità che massimizza l’uccisione tumorale tende anche ad amplificare tossicità e esaurimento. Piuttosto che cercare una singola affinità perfetta, la miscelazione di cellule CAR T con diverse intensità di legame per lo stesso marcatore tumorale emerge come una strategia promettente. In questo approccio, le cellule ad alta affinità forniscono un attacco rapido e potente, mentre le cellule a bassa affinità aiutano a smorzare l’infiammazione incontrollata e a sostenere il controllo a lungo termine. Se confermata in studi clinici e applicata ad altri bersagli oltre a CD19, una tale combinazione di affinità per i prodotti CAR T potrebbe ampliare la finestra terapeutica—rendendo le terapie cellulari più sicure, più durature e adatte a una più ampia gamma di tumori.
Citazione: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Parole chiave: Terapia con cellule CAR T, CD19, affinità del recettore, sindrome da rilascio di citochine, immunoterapia del cancro