Clear Sky Science · pt
Equilibrando eficácia e segurança da terapia CAR-T por combinação de afinidades
Por que isso importa para o futuro do tratamento do câncer
Células imunes geneticamente modificadas, chamadas células CAR T, podem curar alguns cânceres hematológicos, mas também podem causar efeitos colaterais perigosos e às vezes falham a longo prazo. Este estudo faz uma pergunta aparentemente simples, com grandes implicações: em vez de construir uma única célula “superpotente” caçadora de câncer, e se deliberadamente misturarmos células com afinidades mais fortes e mais fracas para o mesmo alvo tumoral para equilibrar melhor potência e segurança?
Como células imunes projetadas combatem o câncer
Células CAR T são linfócitos T do paciente reprogramados com um receptor artificial para que se liguem a marcadores em células tumorais e as destruam. A maioria das terapias aprovadas tem como alvo uma molécula chamada CD19 em células B e usa receptores que se ligam a esse marcador com muito mais força do que os receptores T naturais. Essa ligação extra-forte ajuda a reconhecer e matar células cancerosas, mas também provoca ativação muito intensa. Isso pode levar a reações imunes graves, como síndrome de liberação de citocinas (CRS), dano a células saudáveis, exaustão precoce das células CAR T e recidivas quando as células tumorais perdem ou reduzem a expressão de CD19.
Encontrando o ponto ideal na força do receptor
Para explorar como a força de ligação molda o comportamento das CAR T, os pesquisadores compararam um CAR CD19 padrão de alta afinidade (JCAR017) com uma versão de afinidade mais baixa (JCAR021) e então projetaram um grande painel de variantes adicionais, algumas com afinidade mais próxima à de um receptor T natural. Em culturas de laboratório, a maioria dessas células CAR T parecia surpreendentemente similar: desde que o receptor fosse exibido de forma estável na superfície celular, mesmo ligantes relativamente fracos ainda podiam ativar, secretar mensageiros imunes-chave e eliminar células-alvo CD19-positivas. Apenas as variantes muito fracas, semelhantes a TCR, começaram a mostrar função reduzida em condições exigentes, como quando as células-alvo apresentavam muito pouco CD19.
O que acontece em organismos vivos
Quando a equipe passou para modelos murinos, as diferenças entre ligantes fortes e fracos tornaram-se muito mais pronunciadas. As CAR T de alta afinidade se expandiram rapidamente, migraram eficientemente para a medula óssea onde residiam células linfomatosas CD19-positivas e controlaram melhor os tumores. CARs de afinidade mais baixa retardaram o crescimento tumoral, mas raramente igualaram o melhor desempenho, e os ligantes ultra-fracos foram amplamente ineficazes. Ao mesmo tempo, os ligantes fortes provocaram ativação mais intensa, diferenciação mais rápida das células T e—importante em um modelo murino humanizado com sistema imune reconstituído—doença tipo CRS mais severa que piorava com o aumento da dose de CAR T.
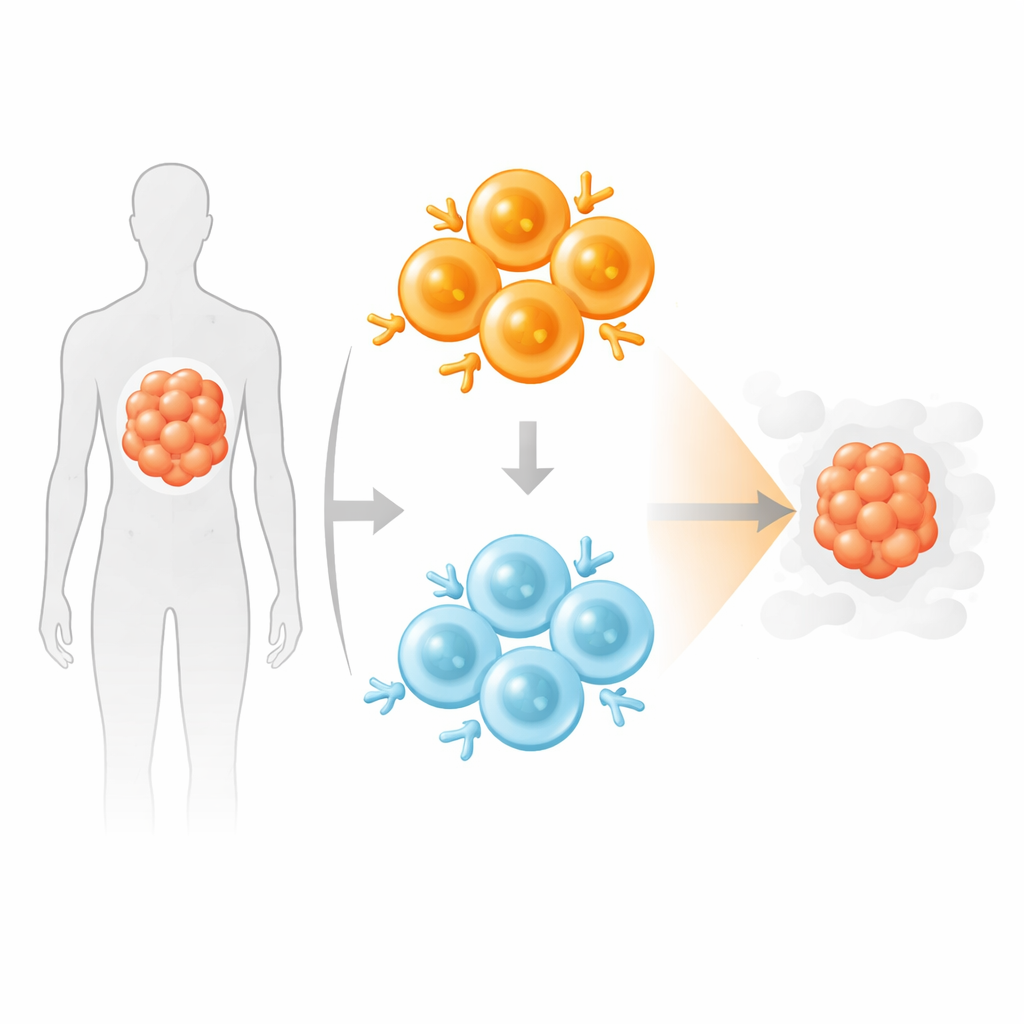
Misturando caçadores fortes e gentis
Inspirados por como nosso sistema imune natural recruta uma mistura de células T de alta e baixa afinidade, os autores testaram um produto CAR T “misturado” que combinava números iguais de CAR T CD19 de alta e baixa afinidade. Em co-culturas laboratoriais com células tumorais e monócitos humanos, esses produtos mistos eliminaram alvos tão efetivamente quanto um produto de alta afinidade em dose completa, mas liberaram menos citocinas inflamatórias, assemelhando-se ao perfil de meia dose do CAR T forte. Sob exposição repetida ou crônica às células tumorais, as CAR T de baixa afinidade gradualmente se tornaram a população dominante na mistura, enquanto as CAR T de alta afinidade isoladas mostraram mais marcadores de exaustão e estresse.
Como a mistura altera o comportamento a longo prazo
Em camundongos portadores de tumor, o produto combinado novamente teve o melhor desempenho geral. CAR T de alta afinidade ainda eram essenciais: CARs de baixa afinidade sozinhas não conseguiam limpar completamente os tumores, mesmo em doses mais altas. Mas quando células de alta e baixa afinidade foram transferidas juntas em doses totais fixas, os tumores encolheram mais rapidamente e de forma mais completa do que com o mesmo número de células de alta afinidade isoladas. Sequenciamento de RNA de célula única das CAR T recuperadas revelou que as células de alta afinidade nos grupos mistos expressavam menos genes associados à exaustão e diferenciação terminal, e mais genes ligados à função citotóxica sustentada e à residência tecidual. Isso sugere que as células parceiras de baixa afinidade ajudam a “compartilhar a carga” do reconhecimento de antígeno, limitando a superestimulação dos ligantes mais fortes.
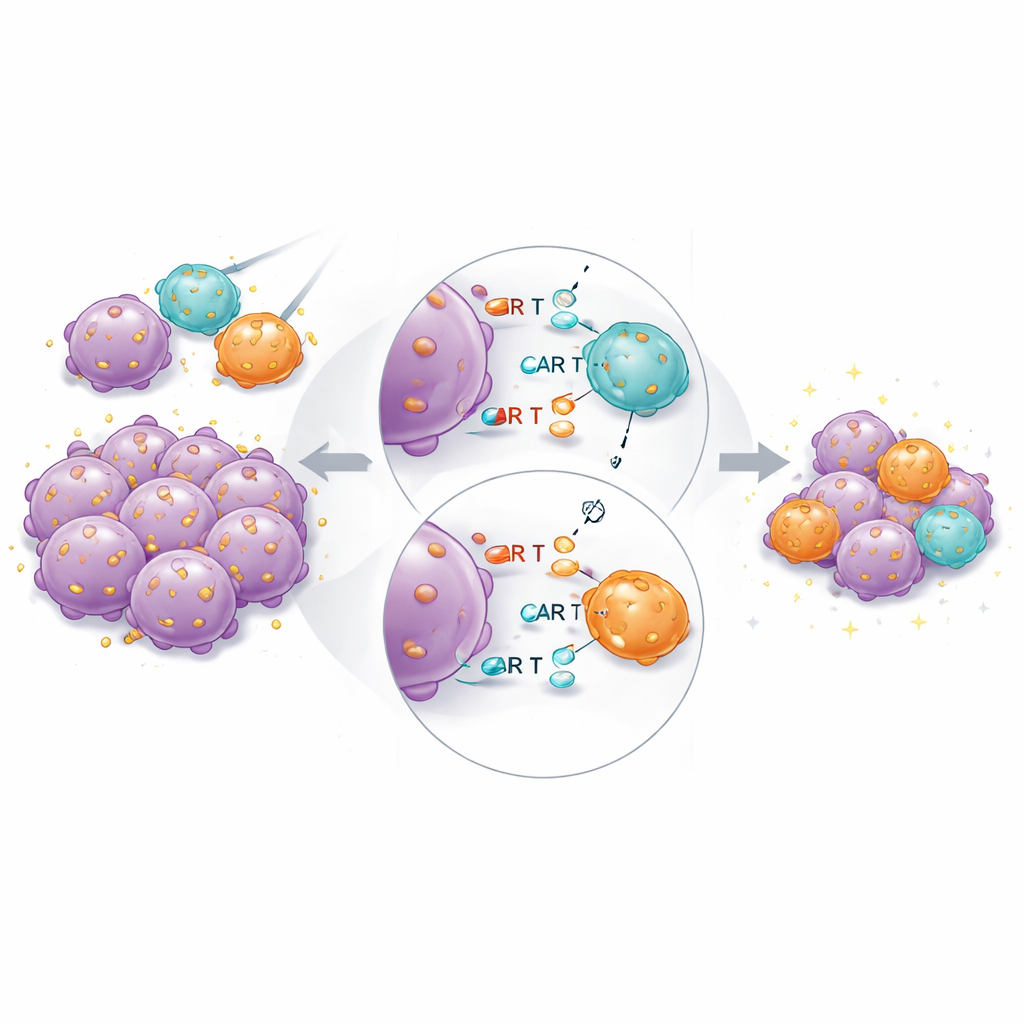
O que isso significa para os pacientes
O estudo demonstra que existe um limite prático para o quão fraco um CAR pode se ligar e ainda funcionar bem nos desenhos atuais, e que a afinidade que maximiza a eliminação tumoral também tende a aumentar toxicidade e exaustão. Em vez de buscar uma única afinidade perfeita, misturar células CAR T com diferentes forças de ligação para o mesmo marcador tumoral surge como uma estratégia promissora. Nessa abordagem, células de alta afinidade proporcionam ataque rápido e potente, enquanto células de baixa afinidade ajudam a reduzir a inflamação descontrolada e a sustentar o controle a longo prazo. Se confirmado em ensaios clínicos e expandido para alvos além do CD19, produtos CAR T combinando afinidades poderiam ampliar a janela terapêutica—tornando as terapias celulares mais seguras, duráveis e adequadas a uma gama mais ampla de cânceres.
Citação: Warmuth, L., Dötsch, S., Trebo, M. et al. Balancing the efficacy and safety of chimeric antigen receptor T-cell therapy by affinity combination. Nat Commun 17, 3413 (2026). https://doi.org/10.1038/s41467-026-71354-7
Palavras-chave: terapia CAR T, CD19, afinidade do receptor, síndrome de liberação de citocinas, imunoterapia contra o câncer