Clear Sky Science · zh
TNFα揭示肠道苹果酸‑天冬氨酸穿梭受损,连接帕金森病与肠道炎症
肠道与帕金森病之间的隐秘联系
许多帕金森病患者在手开始颤抖前很久就先在如厕时察觉异常。便秘和腹胀可能在运动症状出现前数年就出现,这提示肠道的“第二大脑”——肠神经系统——可能在疾病早期就参与其中。本研究提出了一个简单却紧迫的问题:肠道炎症如何扰乱这些肠神经,且这种扰乱是否可能推动帕金森病和其他肠道疾病的发展?
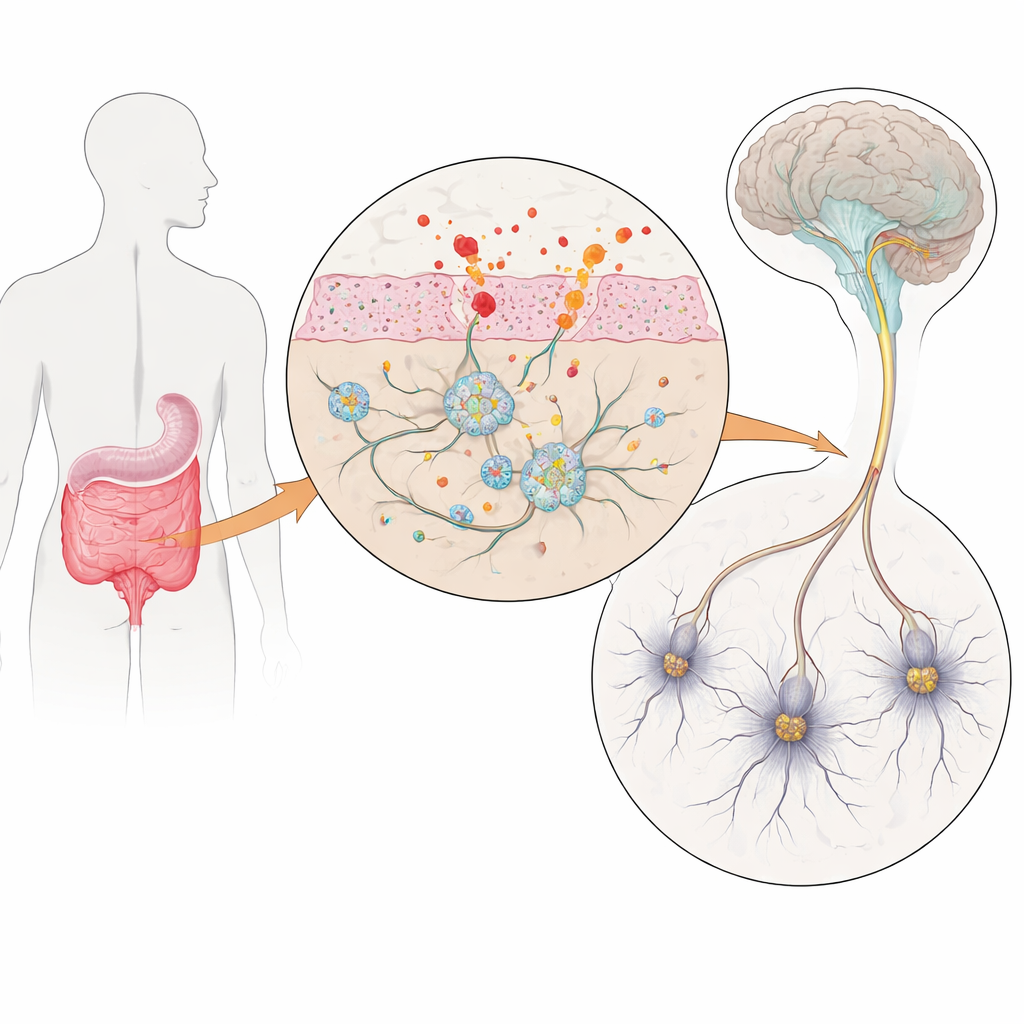
体外培养的肠道神经模型
为探究这一点,研究者利用诱导多能干细胞构建了人类肠道神经的实验模型——将成人细胞重编程回类干细胞状态,再引导其分化为肠神经元及称为胶质细胞的支持细胞。一些干细胞系携带三拷贝的α‑突触核蛋白基因(该蛋白在帕金森病中异常聚集),而匹配的对照细胞系基因剂量正常。经过约十周的定向发育,这些培养物包含了丰富的类肠道神经元和胶质细胞,细胞多样性与真实人类肠道高度相似。关键在于,帕金森样细胞产生了额外的α‑突触核蛋白,创建了一个可控的肠道早期疾病模型。
细胞能量方面的预先脆弱性
即便在加入任何炎症刺激之前,携带额外α‑突触核蛋白的细胞在能量系统方面就显示出广泛的压力迹象。单细胞基因组分析详尽揭示了处理脂类、胆固醇以及细胞燃料关键构件的通路紊乱。显微镜下可见它们的线粒体更少、更小且更易断裂。神经元与胶质细胞之间的通讯也被重连,压力相关的信号通路更为突出。综合这些发现,描绘出一种表面上与健康细胞相似但在能量与抗逆性方面已接近临界的肠道神经细胞状态。
炎症使局势失衡
团队随后引入了肿瘤坏死因子α(TNF),这是一种在帕金森病及溃疡性结肠炎等肠道疾病中升高的主要炎性信号。TNF对两类培养物的影响截然不同。在帕金森样细胞中,TNF使神经元和胶质细胞内的α‑突触核蛋白水平上升,并增加该蛋白与线粒体的物理接触——这种组合与损伤和氧化应激相关。电生理记录显示,健康对照网络在TNF处理后能够提高活动性,而帕金森样网络仍然迟缓,表明其应对炎性挑战的适应能力受损。在分子层面,蛋白质与代谢物测量均指向一个关键能量转运系统:苹果酸‑天冬氨酸穿梭(malate–aspartate shuttle),该系统通常将还原当量输送进线粒体。在TNF作用下,这一穿梭在帕金森样细胞中特异性失灵,耗竭了必需分子,迫使细胞退而求其次,用谷氨酰胺作为应急燃料。
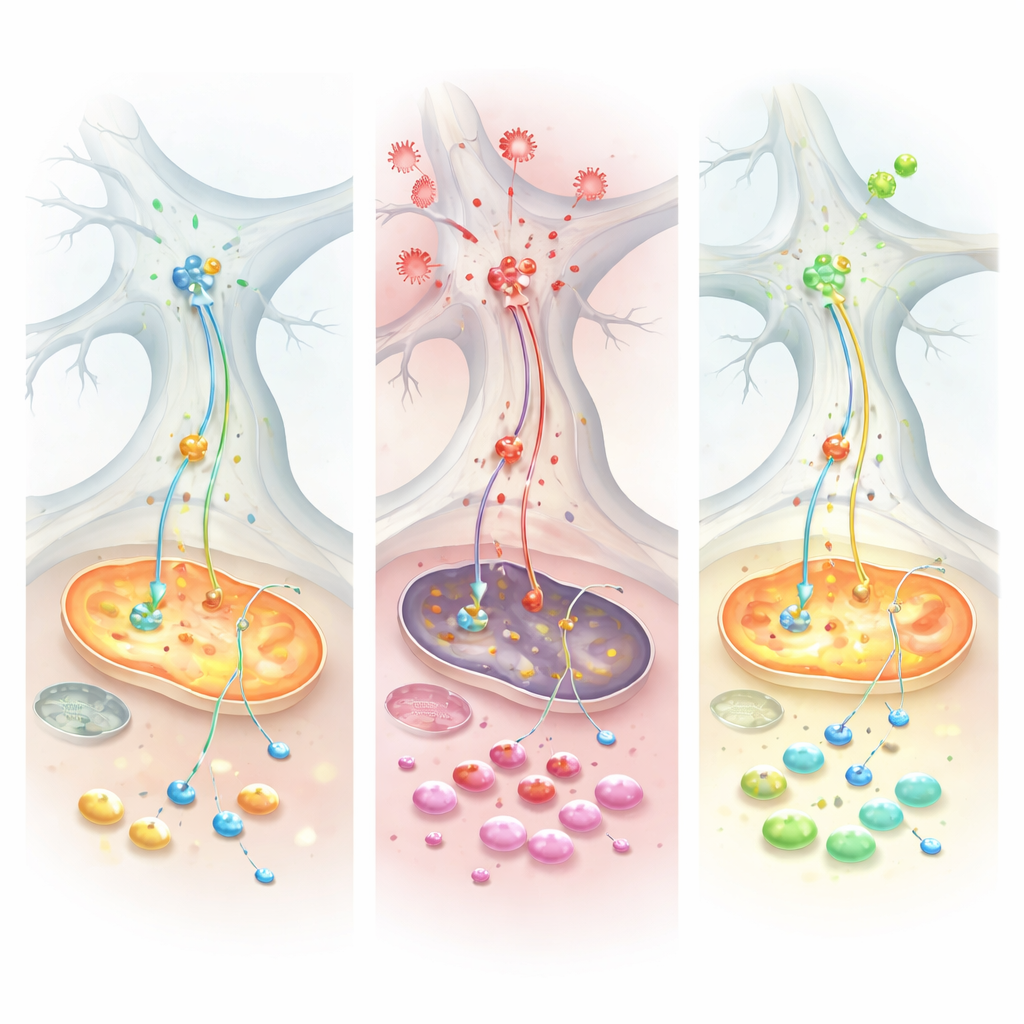
可能的救援方法与患者线索
当研究人员用Chicago‑Sky‑Blue 6B(一种调节谷氨酸处理的化合物)处理这些培养物时,情形发生了变化。该药物恢复了多项线粒体呼吸指标,减少了对谷氨酰胺的异常依赖,并部分正常化了处于压力下细胞的能量平衡。为检验这种代谢特征是否也出现在真实患者中,团队分析了溃疡性结肠炎患者的肠道组织以及大型公共基因表达数据集。在多个队列中,他们发现驱动苹果酸‑天冬氨酸穿梭的酶活性降低,同时发炎肠组织中α‑突触核蛋白增多。对抗TNF治疗反应良好的患者往往恢复了这些能量酶的表达并显示出较低的α‑突触核蛋白水平,这提示培养模型中观察到的炎性‑代谢模式在人体疾病中有镜像对应。
这对患者的意义
简而言之,该研究表明α‑突触核蛋白过载使肠道神经在代谢上变得脆弱,而肠道炎症通过诸如TNF之类的信号利用了这一弱点。通过损害关键的能量穿梭并将细胞推入紧张的备用燃料模式,炎症增加了氧化应激,促使α‑突触核蛋白与线粒体关联,并破坏肠道神经元的正常功能。鉴于在帕金森模型与发炎的人类肠道中都可见类似特征,这项工作指向了一个共享的代谢薄弱点,可成为未来治疗的靶点。正如本研究中Chicago‑Sky‑Blue 6B所示,调节谷氨酸与谷氨酰胺代谢可能是保护肠道神经系统的有希望策略,或有助缓解便秘等症状,并可能减缓帕金森病及其他炎性肠病的早期进程。
引用: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
关键词: 帕金森病, 肠神经系统, 肠道炎症, 线粒体代谢, α‑突触核蛋白