Clear Sky Science · es
El TNF alfa revela la disfunción del transporte malato‑aspártico entérico que conecta la enfermedad de Parkinson y la inflamación intestinal
El vínculo oculto entre el intestino y el Parkinson
Muchas personas con enfermedad de Parkinson notan problemas en el baño mucho antes de que sus manos comiencen a temblar. El estreñimiento y la distensión abdominal pueden aparecer años antes de los problemas de movimiento, lo que sugiere que el “segundo cerebro” del intestino —el sistema nervioso entérico— puede verse implicado en las etapas tempranas de la enfermedad. Este estudio plantea una pregunta sencilla pero urgente: ¿cómo altera la inflamación intestinal estos nervios del intestino, y podría esa alteración contribuir al desarrollo del Parkinson y de otros trastornos intestinales?
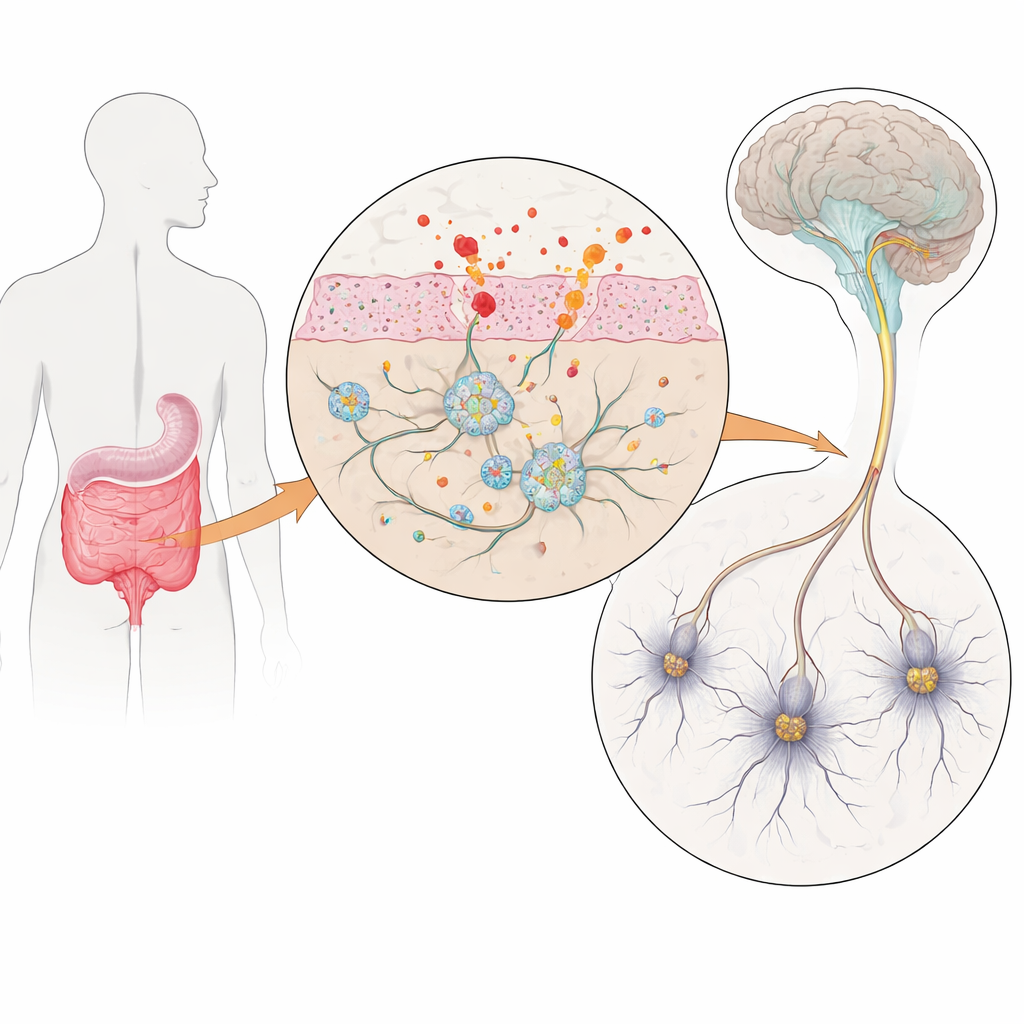
Nervios intestinales en placa
Para investigar esto, los autores construyeron un modelo de laboratorio de los nervios intestinales humanos usando células madre pluripotentes inducidas —células adultas reprogramadas a un estado similar al de las células madre y luego dirigidas para convertirse en neuronas entéricas y células gliales de soporte—. Algunas líneas de células madre portaban tres copias del gen de la alfa‑sinucleína, una proteína que se agrupa de forma anómala en la enfermedad de Parkinson, mientras que las líneas de control emparejadas tenían la dosis genética normal. Tras unas diez semanas de desarrollo dirigido, estos cultivos contenían una mezcla rica de neuronas y glía con características intestinales que se asemejaban estrechamente a la diversidad celular encontrada en intestinos humanos reales. De manera crucial, las células con carácter parecido al Parkinson producían alfa‑sinucleína en exceso, creando un modelo controlable de enfermedad temprana en el intestino.
Una vulnerabilidad preexistente en la energía celular
Aún antes de añadir inflamación, las células con exceso de alfa‑sinucleína mostraron signos generalizados de tensión en sus sistemas energéticos. Un perfil detallado de genes a nivel de célula única reveló alteraciones en vías que manejan grasas, colesterol y bloques constructores clave para el combustible celular. La microscopía mostró que sus mitocondrias —las pequeñas centrales energéticas dentro de las células— eran menos numerosas, más pequeñas y más fragmentadas. La comunicación entre neuronas y glía también estaba reorganizada, con vías de señalización relacionadas con el estrés volviéndose más prominentes. En conjunto, estos hallazgos dibujan el retrato de células nerviosas intestinales que parecen externamente similares a las sanas pero que ya viven al límite en términos de energía y resiliencia.
La inflamación desequilibra la balanza
El equipo introdujo entonces factor de necrosis tumoral alfa (TNF), una señal inflamatoria importante que está elevada tanto en la enfermedad de Parkinson como en trastornos intestinales como la colitis ulcerosa. El TNF tuvo un impacto notablemente diferente en los dos tipos de cultivos. En las células tipo Parkinson, el TNF elevó los niveles de alfa‑sinucleína dentro de neuronas y glía e incrementó el contacto físico de la proteína con las mitocondrias, una combinación asociada con daño y estrés oxidativo. Registros eléctricos mostraron que las redes de control sanas podían aumentar su actividad tras TNF, pero las redes tipo Parkinson permanecieron apagadas, revelando una capacidad reducida para adaptarse al desafío inflamatorio. A nivel molecular, las medidas de proteínas y metabolitos convergieron en un sistema clave de transferencia de energía llamado transporte malato–aspártico, que normalmente traslada poder reductor hacia las mitocondrias. Bajo TNF, este transporte falló específicamente en las células tipo Parkinson, agotando moléculas esenciales y obligando a las células a recurrir a la quema de glutamina como combustible de emergencia.
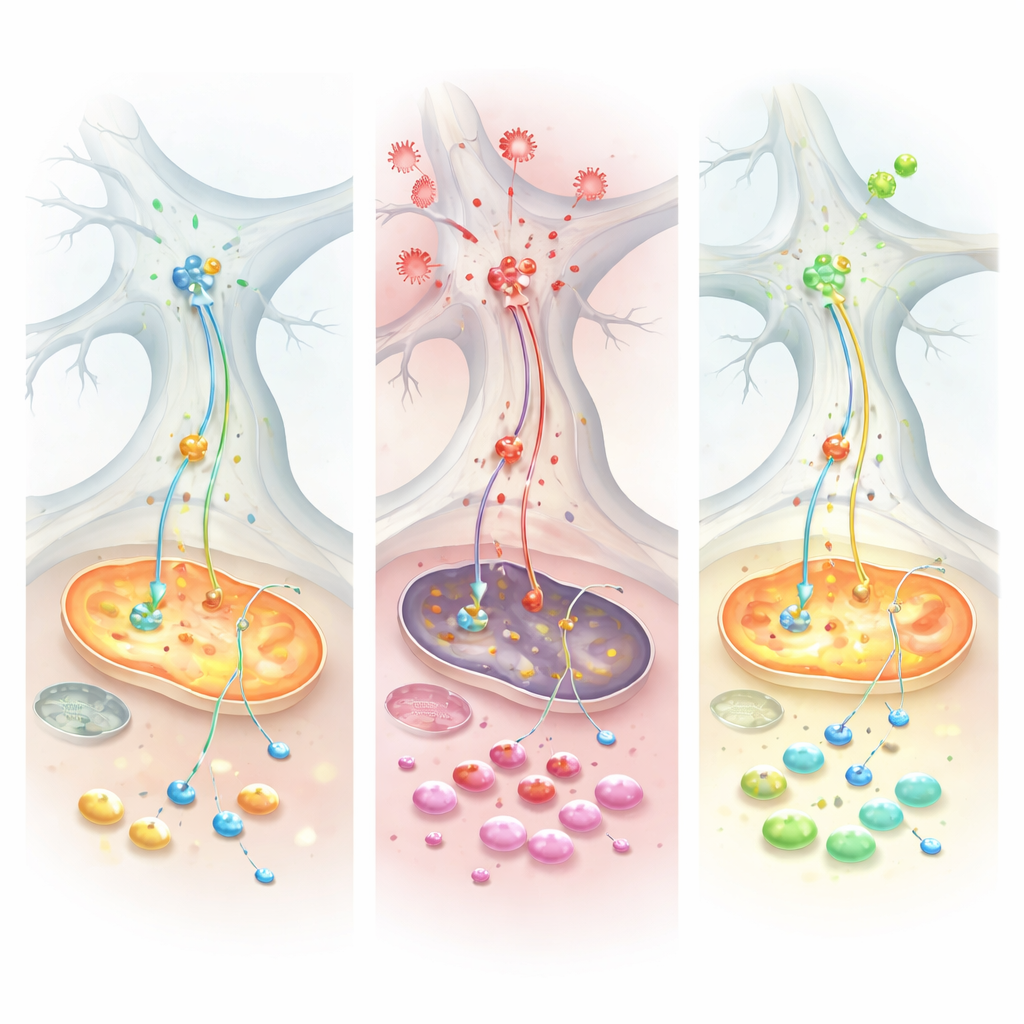
Una posible rescate y pistas en pacientes
Cuando los investigadores trataron los cultivos con Chicago‑Sky‑Blue 6B, un compuesto que modula el manejo del glutamato, el panorama cambió. El fármaco restauró varias medidas de la respiración mitocondrial, redujo la dependencia anómala de la glutamina y normalizó parcialmente el equilibrio energético en las células estresadas. Para comprobar si el mismo tema metabólico aparece en personas reales, el equipo analizó tejido intestinal de pacientes con colitis ulcerosa y grandes conjuntos de datos públicos de expresión génica. En múltiples cohortes, hallaron una actividad reducida de enzimas que alimentan el transporte malato–aspártico, junto con un aumento de alfa‑sinucleína en tejido intestinal inflamado. Los pacientes que respondieron bien a la terapia anti‑TNF tendieron a recuperar la expresión de estas enzimas energéticas y mostraron niveles más bajos de alfa‑sinucleína, lo que sugiere que el patrón inflamatorio‑metabólico observado en los cultivos de laboratorio se refleja en la enfermedad humana.
Por qué importa esto para los pacientes
En términos sencillos, el estudio sugiere que la sobrecarga de alfa‑sinucleína vuelve a los nervios intestinales frágiles desde el punto de vista metabólico, y la inflamación intestinal, a través de señales como el TNF, explota esa debilidad. Al dañar un transporte energético clave y empujar a las células a un modo de combustible de reserva, la inflamación aumenta el estrés oxidativo, favorece la asociación de alfa‑sinucleína con las mitocondrias y socava la función normal de las neuronas intestinales. Dado que firmas similares se observan tanto en modelos de Parkinson como en intestinos humanos inflamados, el trabajo apunta a un punto débil metabólico compartido que podría ser atacado por futuras terapias. Modular el metabolismo del glutamato y la glutamina —como hace Chicago‑Sky‑Blue 6B en este estudio— surge como una estrategia prometedora para proteger el sistema nervioso intestinal, aliviar potencialmente síntomas como el estreñimiento y quizá frenar las etapas más tempranas del Parkinson y de otras condiciones intestinales inflamatorias.
Cita: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Palabras clave: Enfermedad de Parkinson, sistema nervioso entérico, inflamación intestinal, metabolismo mitocondrial, alfa‑sinucleína