Clear Sky Science · it
TNF alfa svela una disfunzione dello shuttle malato‑aspartato enterico che collega il morbo di Parkinson e l’infiammazione intestinale
Il legame nascosto tra intestino e Parkinson
Molte persone con morbo di Parkinson avvertono per prime difficoltà in bagno molto prima che inizino i tremori alle mani. Stitichezza e gonfiore possono comparire anni prima dei problemi motori, suggerendo che il "secondo cervello" dell’intestino – il sistema nervoso enterico – possa essere coinvolto precocemente nella malattia. Questo studio pone una domanda semplice ma urgente: come l’infiammazione intestinale altera questi nervi enterici, e quella perturbazione potrebbe contribuire a guidare il Parkinson e altri disturbi intestinali?
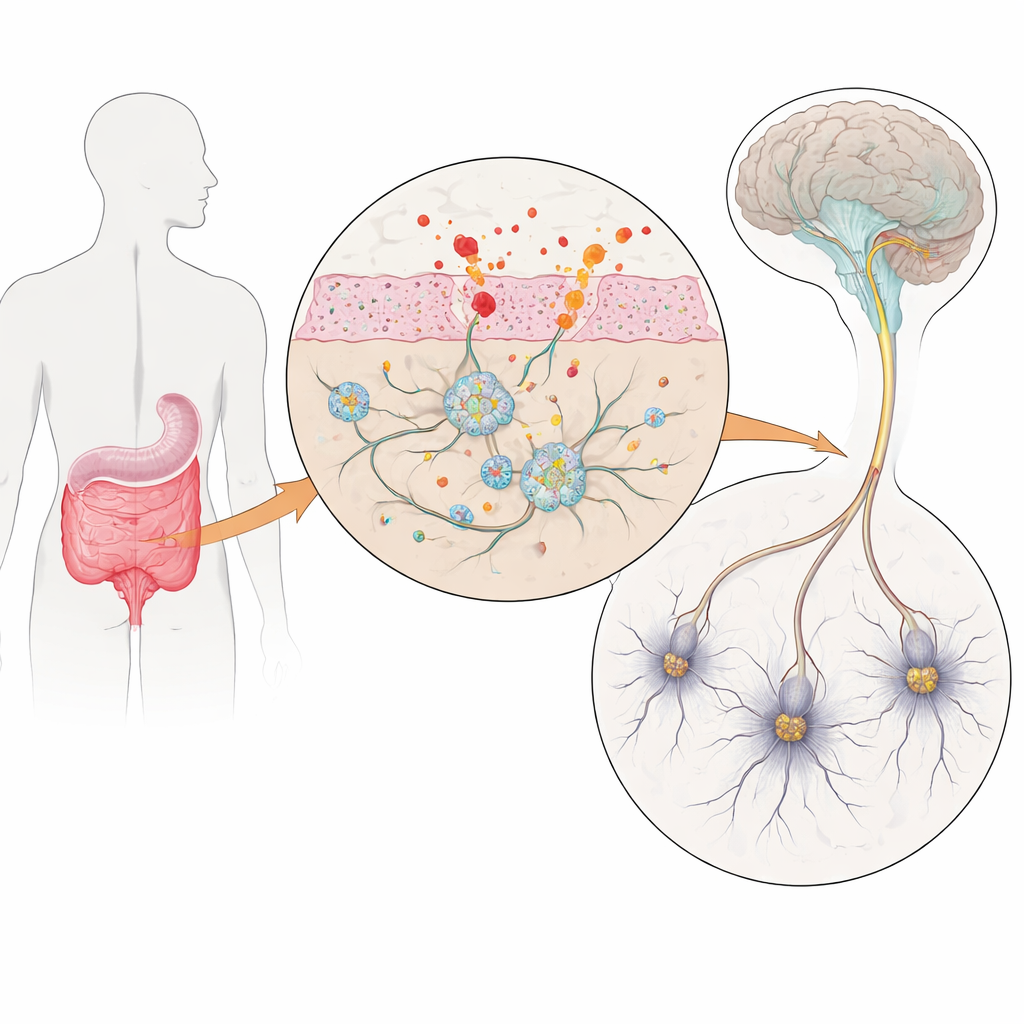
Nervi intestinali in coltura
Per esplorare la questione, i ricercatori hanno costruito un modello di laboratorio dei nervi intestinali umani usando cellule pluripotenti indotte – cellule adulte riprogrammate in uno stato simile a quello staminale e poi indirizzate a diventare neuroni enterici e cellule di supporto chiamate glia. Alcune linee cellulari derivavano da individui con tre copie del gene per l’alfa‑sinucleina, una proteina che si aggrega in modo anomalo nella malattia di Parkinson, mentre linee di controllo corrispondenti avevano una dose genica normale. Dopo circa dieci settimane di sviluppo guidato, queste colture contenevano un ricco mix di neuroni e glia intestinali che somigliavano molto alla diversità cellulare presente nei veri intestini umani. Crucialmente, le cellule con fenotipo Parkinson prodotte maggiori quantità di alfa‑sinucleina, creando un modello controllabile delle fasi precoci della malattia nell’intestino.
Una vulnerabilità energetica preesistente
Anche prima di aggiungere qualsiasi infiammazione, le cellule con eccesso di alfa‑sinucleina mostravano segnali diffusi di stress nei loro sistemi energetici. Un profilo genico dettagliato a livello di singola cellula ha rivelato alterazioni in vie che gestiscono grassi, colesterolo e precursori chiave del carburante cellulare. La microscopia ha mostrato che i loro mitocondri – le piccole centrali energetiche dentro le cellule – erano meno numerosi, più piccoli e più frammentati. Anche la comunicazione tra neuroni e glia risultava riorganizzata, con percorsi di segnalazione legati allo stress che diventavano più prominenti. Nel complesso, questi risultati ritraggono cellule nervose intestinali che esternamente somigliano a cellule sane ma che vivono già ai limiti in termini di energia e resilienza.
L’infiammazione fa pendere la bilancia
Il team ha quindi introdotto il fattore di necrosi tumorale alfa (TNF), un importante segnale infiammatorio elevato sia nella malattia di Parkinson sia in disturbi intestinali come la colite ulcerosa. Il TNF ha avuto un impatto nettamente diverso sui due tipi di colture. Nelle cellule con fenotipo Parkinson, il TNF ha aumentato i livelli di alfa‑sinucleina sia nei neuroni sia nelle glia e ha incrementato il contatto fisico della proteina con i mitocondri, una combinazione associata a danno e stress ossidativo. Le registrazioni elettriche hanno mostrato che le reti di controllo sane potevano aumentare la loro attività dopo il TNF, mentre le reti Parkinson‑like restavano svogliate, rivelando un’incapacità di adattarsi alla sfida infiammatoria. A livello molecolare, misure di proteine e metaboliti convergevano su un sistema chiave per il trasferimento di energia chiamato shuttle malato–aspartato, che normalmente trasporta potere riducente nei mitocondri. Sotto TNF, questo shuttle falliva in modo specifico nelle cellule con fenotipo Parkinson, esaurendo molecole essenziali e costringendo le cellule a ricorrere al consumo di glutamina come carburante d’emergenza.
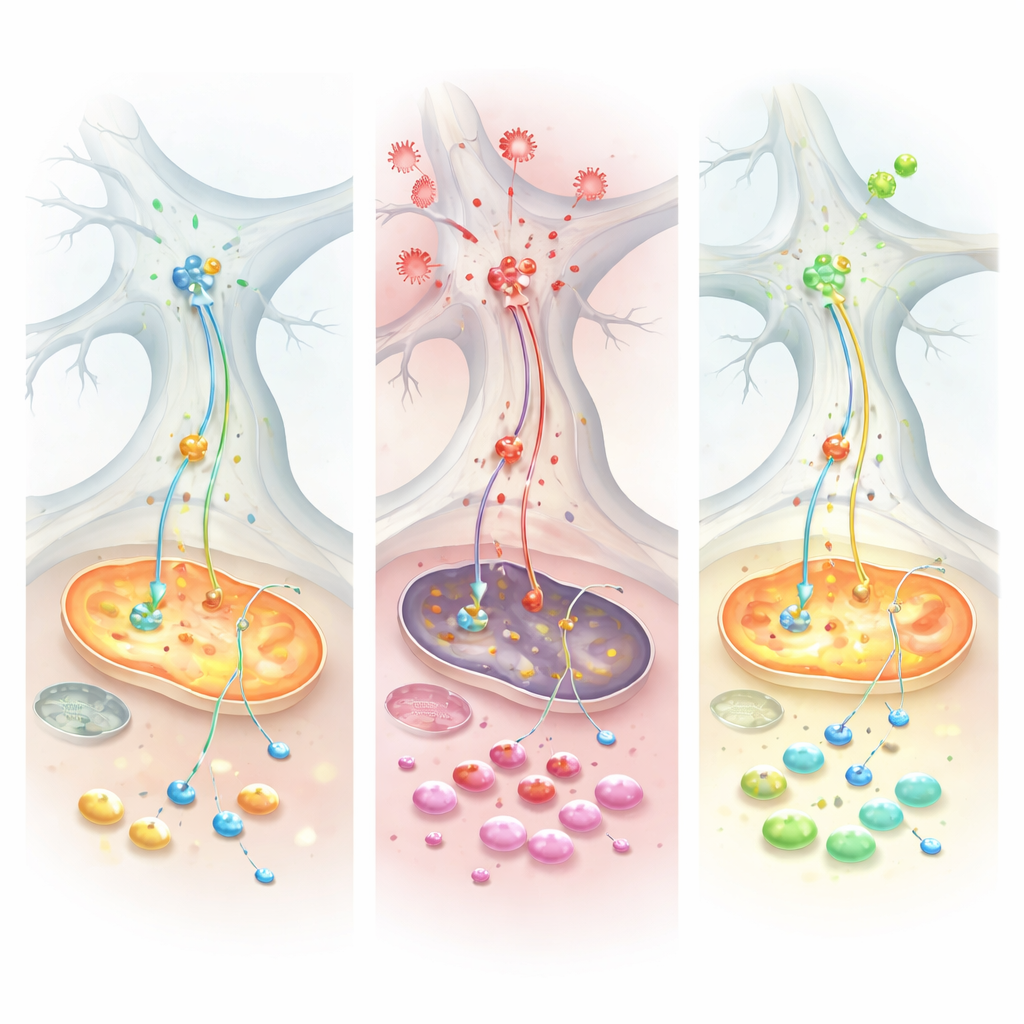
Una potenziale via di salvataggio e indizi dai pazienti
Quando i ricercatori hanno trattato le colture con Chicago‑Sky‑Blue 6B, un composto che modula la gestione del glutammato, lo scenario è cambiato. Il farmaco ha ripristinato diverse misure della respirazione mitocondriale, ha ridotto la dipendenza anomala dalla glutamina e ha parzialmente normalizzato l’equilibrio energetico nelle cellule sotto stress. Per verificare se lo stesso tema metabolico appare nelle persone reali, il team ha analizzato tessuto intestinale di pazienti con colite ulcerosa e grandi dataset pubblici di espressione genica. In più coorti, hanno riscontrato una ridotta attività di enzimi che alimentano lo shuttle malato–aspartato, insieme a un aumento dell’alfa‑sinucleina nei tessuti intestinali infiammati. I pazienti che rispondevano bene alla terapia anti‑TNF tendevano a recuperare l’espressione di questi enzimi energetici e mostravano livelli più bassi di alfa‑sinucleina, suggerendo che lo schema infiammatorio‑metabolico osservato nelle colture in laboratorio si rispecchia nella malattia umana.
Perché questo è importante per i pazienti
In termini semplici, lo studio suggerisce che il sovraccarico di alfa‑sinucleina rende i nervi intestinali metabolicamente fragili, e l’infiammazione intestinale, tramite segnali come il TNF, sfrutta questa debolezza. Compromettendo uno shuttle energetico chiave e spingendo le cellule in una modalità di carburante di riserva stressata, l’infiammazione aumenta lo stress ossidativo, favorisce l’associazione dell’alfa‑sinucleina con i mitocondri e indebolisce la funzione normale dei neuroni intestinali. Poiché segnature simili sono osservate sia nei modelli del Parkinson sia negli intestini umani infiammati, il lavoro indica un punto debole metabolico condiviso che potrebbe essere bersaglio di terapie future. Modulare il metabolismo del glutammato e della glutamina — come fa Chicago‑Sky‑Blue 6B in questo studio — emerge come una strategia promettente per proteggere il sistema nervoso dell’intestino, alleviare potenzialmente sintomi come la stitichezza e forse rallentare le fasi più precoci del Parkinson e di altre condizioni intestinali infiammatorie.
Citazione: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Parole chiave: Malattia di Parkinson, sistema nervoso enterico, infiammazione intestinale, metabolismo mitocondriale, alfa‑sinucleina